造血器腫瘍 ~治療ガイドライン
ガイドライン文中の文献番号から,該当する文献リストへリンクされます
II.リンパ腫
悪性リンパ腫 総論
わが国における悪性リンパ腫の新規罹患者者は,2005 年で16,991 人とされている。罹患率は,1985 年,1995 年,2005 年で人口10 万人あたりそれぞれ5.5 人,8.9 人,13.3 人と,年々増加傾向にある。男女比は約3:2 と男性に多く,65~74 歳が発症のピークである1)。
組織学的にホジキンリンパ腫(Hodgkin lymphoma:HL)と非ホジキンリンパ腫(non Hodgkin lymphoma:NHL)に大別されるが大半がNHL であり,わが国におけるHL の頻度は全悪性リンパ腫のうち5~10%程度とされている。
1.診断に必要な事項
1)病歴
問診により,既往症,治療中の疾患,合併症,初発症状,症状の出現時期,全身症状(発熱,体重減少,盗汗など)の有無,必要があれば出生地を記録する。
2)身体所見
診察により以下の所見を記録する。
- 身長,体重,体温,血圧,脈拍
- Performance Status
- 貧血,黄疸の有無,皮疹の有無,胸部・腹部の聴診・打診,腫大リンパ節の有無〔有りの場合,部位(リンパ節領域名,左右),個数,サイズ(最大長径とそれに直行する短径の二方向で測定し,単位はcm を用いる),性状(硬さ,可動性の有無など)〕,触知可能な肝腫大・脾腫大の有無,浮腫の有無
- 運動神経麻痺・異常知覚・髄膜刺激症状の有無
3)一般検査
以下の検査を行う。
- 末梢血血球算定(白血球数,好中球数,リンパ球数,腫瘍細胞数,赤血球数,ヘモグロビン値,血小板数,血液像)
- 生化学検査(TP,Alb,ALT,AST,LDH,ALP,γ-GTP,Na,K,Cl,Ca,P,BUN, Cr,FBS,UA)
- 血清学的検査(CRP,IgG,IgA,IgM,タンパク分画,可溶性IL-2R,β2 ミクログロブリン)
- ウイルス検査(HBs 抗原,HBs 抗体,HBc 抗体,HCV 抗体,HIV 抗体,HTLV-1 抗体)
- 尿検査(糖,タンパク,潜血,沈渣)
- 画像・その他の検査〔胸部X 線検査,十二誘導心電図,頸部・胸部・腹部・骨盤Computed Tomography(CT),(必要に応じ)上部・下部消化管内視鏡,骨髄穿刺・生検,心エコー,必要時にはPositron Emission Tomography(PET),頭部CT・Magnetic Resonance Imaging(MRI),髄液検査,動脈血ガス分析〕
4)病理組織診断
悪性リンパ腫の診断のためには生検による組織病理検査は必須であり,治療前に適切な病変より生検を行う。鼠径リンパ節や腋窩リンパ節は反応性腫大をきたすことがあるため,全身にリンパ節腫脹が認められる場合には頸部リンパ節の生検を行うことが望ましい。開放生検が困難な場合を除いて,針生検のみの病理組織検査は診断には不十分である。
生検により得られた検体はホルマリン固定パラフィンブロックから薄切標本を作製し,ヘマトキシリン・エオジン染色を行う。その他にも以下のような免疫組織化学検査を行う。
- CD3,細胞質内CD3ε,CD5,CD45
- CD20,CD79a,CD10,免疫グロブリン(細胞質内免疫グロブリン)
- CD56
- CD15,CD30,cyclin D1,bcl-2,bcl-6,MIB1(Ki-67),EBER など
5)その他の検査
可能な限り検体より細胞を分離し,以下の検査を行う。
- フローサイトメトリー
- 染色体分析
- 遺伝子解析
- in situ hybridization
2.病型分類
悪性リンパ腫の分類としては,WHO 分類(2008)が広く用いられている。悪性リンパ腫が含ま れるリンパ系腫瘍は以下の通りに分類されている2)。
前駆リンパ系腫瘍
B 細胞リンパ芽球性白血病/リンパ腫(B lymphoblastic leukemia/lymphoma)
T 細胞リンパ芽球性白血病/リンパ腫(T lymphoblastic leukemia/lymphoma)
成熟B 細胞腫瘍
慢性リンパ性白血病/小リンパ球性リンパ腫(Chronic lymphocytic leukemia/small lymphocytic lymphoma)
B 細胞前リンパ球性白血病(B-cell prolymphocytic leukemia)
脾B 細胞辺縁帯リンパ腫(Splenic B-cell marginal zone lymphoma)
有毛細胞白血病(Hairy cell leukemia)
リンパ形質細胞性リンパ腫(Lymphoplasmacytic lymphoma)
重鎖病(Heavy chain disease)
形質細胞腫瘍(Plasma cell neoplasms)
粘膜関連リンパ組織型節外性辺縁帯リンパ腫(MALT リンパ腫)(Extranodal marginal zone lymphoma of mucosa-associated lymphoid tissue)
節性辺縁帯リンパ腫(Nodal marginal zone lymphoma)
濾胞性リンパ腫(Follicular lymphoma)
マントル細胞リンパ腫(Mantle cell lymphoma)
びまん性大細胞型B 細胞リンパ腫(Diffuse large B-cell lymphoma)
バーキットリンパ腫(Burkitt lymphoma)
成熟T 細胞およびNK 細胞腫瘍
T 細胞前リンパ球性白血病(T-cell prolymphocytic leukemia)
T 細胞大顆粒リンパ球性白血病(T-cell large granular lymphocytic leukemia)
アグレッシブNK 細胞白血病(Aggressive NK-cell leukemia)
成人T 細胞白血病/ リンパ腫(Adult T-cell leukemia/lymphoma)
節外性鼻型NK/T 細胞リンパ腫(Extranodal NK/T-cell lymphoma, nasal type)
腸管症関連T 細胞リンパ腫(Enteropathy-associated T-cell lymphoma)
肝脾T 細胞リンパ腫(Hepatosplenic T-cell lymphoma)
皮下脂肪組織炎様T 細胞リンパ腫(Subcutaneous panniculitis-like T-cell lymphoma)
菌状息肉症(Mycosis fungoides)
セザリー症候群(Sézary syndrome)
原発性皮膚CD30 陽性T 細胞リンパ増殖異常症(Primary cutaneous CD30 positive T-cell lymphoproliferative disorders)
原発性皮膚γδ細胞リンパ腫(Primary cutaneous gamma-delta T-cell lymphoma)
末梢性T 細胞リンパ腫,非特定型(Peripheral T-cell lymphoma, NOS)
血管免疫芽球性T 細胞リンパ腫(Angioimmunoblastic T-cell lymphoma)
未分化大細胞リンパ腫(Anaplastic large cell lymphoma)
ホジキンリンパ腫
結節性リンパ球優位型ホジキンリンパ腫(Nodular lymphocyte predominant Hodgkin lymphoma)
古典的ホジキンリンパ腫(Classical Hodgkin lymphoma)
結節性硬化型(Nodular sclerosis)
混合細胞型(Mixed cellularity)
リンパ球豊富型(Lymphocyte-rich)
リンパ球減少型(Lymphocyte depletion)
3.臨床分類
1982 年に提唱されたWorking Formulation 分類では,病型分類の他にNHL の自然史に基づき,無治療での予後が年単位で進行する低悪性度,月単位で進行する中悪性度,週単位で進行する高悪性度というように悪性度による分類がなされた。1989 年にはアメリカのNational Cancer Institute より,悪性度による分類に加えて疾患の悪性度,活動性や侵攻性といったaggressiveness の程度を考慮し,低悪性度をインドレント リンパ腫(indolent lymphoma),中悪性度をアグレッシブ リンパ腫(aggressive lymphoma),高悪性度を高度アグレッシブ リンパ腫(highly aggressive lymphoma)に分類した臨床分類が提唱され,この分類が臨床試験で広く用いられてきた。
WHO 分類における臨床分類は,以下の通りとされている。また,5 年以上の生存が期待できる疾患群をインドレント リンパ腫,5 年以下の生存しか期待できない疾患群をアグレッシブ リンパ腫とする臨床分類も提唱されている3)。
1)WHO 分類を基にした臨床分類
インドレント リンパ腫およびリンパ性白血病
B 細胞
慢性リンパ性白血病/ 小リンパ球性リンパ腫
リンパ形質細胞性リンパ腫
脾B 細胞辺縁帯リンパ腫
有毛細胞性白血病
粘膜関連リンパ組織型節外性辺縁帯リンパ腫(MALT リンパ腫)
節性辺縁帯リンパ腫
濾胞性リンパ腫(Grade 1, 2)
T 細胞
T 細胞大顆粒リンパ球性白血病
成人T 細胞白血病/リンパ腫(くすぶり型)
菌状息肉症/セザリー症候群
中等度アグレッシブ リンパ腫およびリンパ性白血病
B 細胞
B 細胞前リンパ球性白血病
マントル細胞リンパ腫
濾胞性リンパ腫(Grade 3)
T 細胞
T 細胞前リンパ球性白血病
成人T 細胞白血病/リンパ腫(慢性型)
節外性鼻型NK/T 細胞リンパ腫
血管免疫芽球性T 細胞リンパ腫
アグレッシブ リンパ腫
B 細胞
びまん性大細胞型B 細胞リンパ腫
T 細胞
末梢性T 細胞リンパ腫,非特定型
腸管症関連T 細胞リンパ腫
未分化大細胞リンパ腫
肝脾T 細胞リンパ腫
高度アグレッシブ リンパ腫およびリンパ性白血病
B 細胞
B 細胞リンパ芽球性白血病/リンパ腫
バーキットリンパ腫/白血病
T 細胞
T 細胞リンパ芽球性白血病/リンパ腫
成人T 細胞白血病/リンパ腫(急性型,リンパ腫型)
NK 細胞
(芽球性NK 細胞リンパ腫)
アグレッシブNK 細胞白血病
2)生存割合でインドレント/アグレッシブ リンパ腫とする臨床分類
インドレント リンパ腫
B 細胞
慢性リンパ性白血病/小リンパ球性リンパ腫
リンパ形質細胞性リンパ腫
B 細胞前リンパ球性白血病
脾B 細胞辺縁帯リンパ腫
粘膜関連リンパ組織型節外性辺縁帯リンパ腫(MALT リンパ腫)
節性辺縁帯リンパ腫
濾胞性リンパ腫(Grade 1, 2)
T 細胞
成人T 細胞性白血病/リンパ腫(くすぶり型)
菌状息肉症/セザリー症候群
アグレッシブリンパ腫
B 細胞
マントル細胞リンパ腫
濾胞性リンパ腫(Grade 3)
びまん性大細胞型B 細胞リンパ腫
バーキットリンパ腫
B 細胞リンパ芽球性白血病/リンパ腫
T 細胞
末梢性T 細胞リンパ腫, 非特定型
腸管症関連T 細胞リンパ腫
未分化大細胞リンパ腫
肝脾T 細胞リンパ腫
T 細胞リンパ芽球性白血病/リンパ腫
成人T 細胞白血病/リンパ腫(急性型,リンパ腫型)
NK 細胞
(芽球性NK 細胞リンパ腫)
アグレッシブNK 細胞白血病
4.病期分類
悪性リンパ腫の病変の広がりは治療選択,予後予測に大きく影響するため,病期を正確に把握することは極めて重要である。悪性リンパ腫に対する病期分類は,HL に対して開発されたAnnArbor 分類4)がNHL に対しても用いられている。悪性リンパ腫の基本的な病期決定には,病歴と理学所見,血球算定,生化学検査,胸部X 線検査,頸部・胸部・腹部・骨盤CT,(必要に応じ)上部・下部消化管内視鏡,骨髄穿刺または生検にて行う。
かつては悪性リンパ腫の病期診断にガリウムシンチが用いられていたが,近年,FDG-PET が感度,特異度とも勝っていることより,ガリウムシンチに代わる検査となった。FDG uptake の程度は悪性リンパ腫の組織型により異なるため,FDG-PET を治療の効果判定に用いる場合には,より正確に判定するために治療前の病期診断時にもFDG-PET を,可能であれば病変の意義をより正確に評価するためにPET-CT を行うことが望ましい。
消化管原発の悪性リンパ腫は節外病変が主病変であるため,Ann Arbor 分類では病期の進展と乖離することが多い。よって,消化管原発の悪性リンパ腫では,Ann Arbor 分類に加えて国際悪性リンパ腫会議で作成された,いわゆるLugano 分類5)が病期分類として用いられている。
| Ⅰ期 | 単独リンパ節領域の病変(Ⅰ)。 またはリンパ節病変を欠く単独リンパ外臓器または部位の限局性病変(ⅠE)。 |
|---|---|
| Ⅱ期 | 横隔膜の同側にある2 つ以上のリンパ節領域の病変(Ⅱ)。 または所属リンパ節病変と関連している単独リンパ外臓器または部位の限局性病変で,横隔膜の同側にあるその他のリンパ節領域の病変はあってもなくてもよい(ⅡE)。 病変のある領域の数は下付きで,例えばⅡ3 のように表してもよい。 |
| Ⅲ期 | 横隔膜の両側にあるリンパ節領域の病変(Ⅲ)。それはさらに隣接するリンパ節病変と関連しているリンパ外進展を伴ったり(ⅢE),または脾臓病変を伴ったり(ⅢS),あるいはその両者(ⅢES)を伴ってもよい。 |
| Ⅳ期 | 1 つ以上のリンパ外臓器のびまん性または播種性病変で,関連するリンパ節病変の有無を問わない。または隣接する所属リンパ節病変を欠く孤立したリンパ外臓器病変であるが,離れた部位の病変を併せ持つ場合。 |
| A およびB 分類(症状) 各病期は以下のように定義される全身症状の有無に従って,A またはB のいずれかに分類される。
|
|
| Ⅰ期 | 消化管に限局した腫瘍
単発または多発(非連続性) |
|---|---|
| Ⅱ期 | 消化管の原発部位から腫瘍が腹腔へ進展
リンパ節浸潤 Ⅱ1:限局性(胃のリンパ腫の場合は胃周囲,腸管の場合は腸管周囲) |
| ⅡE期 | 近接の臓器または組織へ進展する漿膜の浸潤(実際の浸潤部位。例:ⅡE[膵臓],ⅡE[大腸],ⅡE[後腹膜]) リンパ節浸潤と近接臓器へ浸潤する進展の両方がある場合は,病期は下付きの1 または2 とE の両方が記載されるべきである。例:Ⅱ1E[膵臓] |
| Ⅳ期 | リンパ外への播種性浸潤または消化管病変に横隔膜を越えたリンパ節病変を伴う。 |
5.予後因子
悪性リンパ腫は,その組織型により低悪性度,中~高悪性度と大きく二つの予後グループに分けられる。組織学的な予後の分類の他にも,分子遺伝学的な区別や,病期や全身状態などの患者個々の状態によるさまざまな因子が知られている。アグレッシブ リンパ腫における予後予測モデルとしては国際予後指標(International Prognostic Index:IPI)6)が,濾胞性リンパ腫では濾胞性リンパ腫国際予後指標(Follicular Lymphoma International Prognostic Index:FLIPI)7),進行期のホジキンリンパ腫に対しては国際予後スコア(International Prognostic Score:IPS)8)が用いられている。
アグレッシブリンパ腫
| IPI での予後因子 | 予後不良因子 |
|---|---|
|
年齢 |
61 歳以上 |
| 年齢調整IPI での予後因子 | 予後不良因子 |
|---|---|
|
血清LDH |
正常上限を越える |
IPI,年齢調整IPI とも予後因子の数によって以下の4 つのリスクグループに分類する。
- IPI
予後因子0 または1:低リスク(Low risk)
予後因子2:低中間リスク(Low-Intermediate risk)
予後因子3:高中間リスク(High-Intermediate risk)
予後因子4 または5:高リスク(High risk) - 年齢調整IPI
予後因子0:低リスク(Low risk)
予後因子1:低中間リスク(Low-Intermediate risk)
予後因子2:高中間リスク(High-Intermediate risk)
予後因子3:高リスク(High risk)
※年齢調整IPI は,自家造血幹細胞移植のように,若年者のみで高齢者は対象とならない治 療や,高齢者のみを対象とした治療の臨床研究への適応に用いられている。
濾胞性リンパ腫
| FLIPI での予後因子 | 予後不良因子 |
|---|---|
|
年齢 |
61 歳以上 |
予後因子の数により,以下の3 つのリスクグループに分類する。
予後因子数0 または1:低リスク(Low risk)
予後因子2:中間リスク(Intermediate risk)
予後因子3 以上:高リスク(Poor risk)
FLIPI は,リツキシマブ(R)が導入される以前の時代の,後方視的な検討に基づいて作成された予後予測モデルであった。その後,R 時代に行われた前方視的試験の対象を基にFLIPI2 が作成された9)。
| FLIPI2 での予後因子 | 予後不良因子 |
|---|---|
|
年齢 |
61 歳以上 |
予後因子の数により,以下の3 つのリスクグループに分類する。
予後因子数0:低リスク(Low risk)
予後因子1 または2:中間リスク(Intermediate risk)
予後因子3 以上:高リスク(High risk)
進行期ホジキンリンパ腫
| IPS での予後因子 | 予後不良因子 |
|---|---|
|
血清アルブミン値 |
4 g/dL 未満 |
5 年の予測無増悪割合(freedom from progression of disease)割合は,予後因子の数が0 個で 84%,1 個で77%,2 個で67%,3 個で60%,4 個で51%,5 個以上で42%とされている。
6.効果判定規準
悪性リンパ腫に対する治療の効果判定には,1999 年に公表された「NHL の効果判定規準の標準化国際ワークショップレポート」10)が広く用いられている。効果判定には通常はCT が用いられるが,近年のFDG-PET の普及度と有用性を示唆する検討結果を受けて,効果判定へFDG-PET を導入した「改訂版NHL の効果判定規準の標準化国際ワークショップレポート」が2007 年に公表された11)。これらの効果判定規準は臨床試験の評価を国際的に統一する目的で作成されたものであるが,FDG-PET を用いた効果判定はCT のみで行う効果判定よりも正確に治療効果を反映している12)ため,日常診療における治療の効果判定にも有用である。
7.治療後の追跡
治療後の追跡・評価の方法は,病型や,臨床試験のもとの診療か日常診療かなどにより異なる。血球算定,生化学検査や画像検査を適切に行い,注意深い病歴の聴取や診察を行うことが,適切な臨床的な判断に重要である。
追跡の頻度,期間に関する明確な指標を示すエビデンスは存在しないが,ホジキンリンパ腫や治癒の可能性があるアグレッシブ リンパ腫では,完全奏効が得られた場合は治療後の2 年間は2~3カ月毎,その後は最低でも3~6 カ月毎の追跡を3 年間は行うことが推奨される。治癒が困難と考えられるインドレント リンパ腫では,治療後の1 年間は2~3 カ月,その後は3~6 カ月毎の追跡が推奨される。
悪性リンパ腫の再発は,8 割以上が臨床症状の出現により発見されるとされている13)14)。定期的にCT を行うことで臨床症状が出現する前に再発が発見される場合もあるが,早期発見が予後改善につながるかは明確ではない15)。よって定期的なCT による追跡は,コストを含めた患者利益を十分に検討した上で行うことが望ましい。定期的なPET による追跡は有用性を示す根拠はなく,推奨されない16)17)。
| 総合効果 | 標的病変の正常化 ならびにSPD |
非標的病変 | 肝腫大 脾腫 腎腫大 |
腫瘍関連 症状と 腫瘍関連 検査値異常 |
骨髄浸潤 | 新病変 | ||
|---|---|---|---|---|---|---|---|---|
| 節性 | 節外性 | 節性 | 節外性 | |||||
| CR | 正常 | 消失 | 正常 | 消失 | 消失 | 正常 | 陰性 | なし |
| CRu | 正常 | 消失 | 正常 | 消失 | 消失 | 正常 | 不確定 | なし |
| 75%以上縮小 | 正常 | 消失 | 消失 | 正常 | 陰性or 不確定 |
なし | ||
| PR | 75%以上縮小 | 正常 | 消失 | 消失 | 正常 | 陽性 | なし | |
| 50%以上縮小 | 正常or 非増大 |
消失or 非増大 |
消失or 非増悪 |
正常 | 問わない (未検可) |
なし | ||
| SD | 50%未満の縮小 かつ 50%未満の増大 |
正常or 非増大 |
消失or 非増大 |
消失or 非増悪 |
正常or 非増悪 |
問わない (未検可) |
なし | |
| PD | 50% 以上増大 |
50% 以上増大 | 増大 | 増大 | 増悪 | 増悪 | 陰性化後 の陽性 |
あり |
| RD | 再腫大 | 再腫大 | 再出現 | 再出現 | 再出現 | |||
CT:Computed Tomography, PET:Positron Emission Tomography, SPD:Sum of the Products of the Greatest Diameters,
CR:Complete Response, CRu:Complete Response/unconfirmed, PR:Partial Response, SD:Stable Disease,
PD:Progressive Disease, RD:Relapsed Disease
| 総合効果 | 標的病変のSPD | 非標的病変 | 骨髄浸潤 | PET | 新病変 | ||
|---|---|---|---|---|---|---|---|
| 節性 | 節外性 | 節性 | 節外性 | ||||
| CR | SPD の変化は問わない(未検は不可) | 陰性 | 陰性 | なし | |||
| PR | SPD の変化は問わない(未検は不可) | 陽性 | 陰性 | なし | |||
| 50%以上縮小 | 正常or 非増大 |
消失or 非増大 |
問わない (未検可) |
陽性 | なし | ||
| SD | 50%未満の縮小 かつ 50%未満の増大 |
正常or 非増大 |
消失or 非増大 |
問わない (未検可) |
陽性 | なし | |
| PD | 50%以上増大 | 増大 | 増大 | 陽性化 | 陽性 | あり | |
| RD | 再腫大 | 再出現 | 再腫大 | 再出現 | |||
CT:Computed Tomography, PET:Positron Emission Tomography, SPD:Sum of the Products of the Greatest Diameters,
CR:Complete Response, CRu:Complete Response/unconfirmed, PR:Partial Response,
SD:Stable Disease, PD:Progressive Disease, RD:Relapsed Disease
【参考文献】
1) 独立行政法人国立がん研究センターがん対策情報センター
がん情報サービス ganjoho.jp http://ganjoho.jp/public/statistics/index.html
2) Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008.
3) Armitage JO, et al. New approach to classifying non-Hodgkin’s lymphomas : clinical features of the major histologic subtypes. Non-Hodgkin’s Lymphoma Classification Project. J Clin Oncol. 1998 ; 16(8) : 2780-95.
4) Carbone PP, et al. Report of the committee on Hodgkin’s disease staging classification. Cancer Res. 1971 ; 31(11) : 1860-1.
5) Rohatiner A, et al. Report on a workshop convened to discuss the pathological and staging classifications of gastrointestinal tract lymphoma. Ann Oncol. 1994 ; 5(5) : 397-400.
6) A predictive model for aggressive non-Hodgkin’s lymphoma. The International Non-Hodgkin’s Lymphoma Prognostic Factors Project. N Engl J Med. 1993 ; 329(14) : 987-94.(3iA)
7) Solal-Céligny P, et al. Follicular lymphoma international prognostic index. Blood. 2004 ; 104(5) : 1258-65.(3iA)
8) Hasenclever D, et al. A prognostic score for advanced Hodgkin’s disease. International Prognostic Factors Project on Advanced Hodgkin’s Disease. N Engl J Med. 1998 ; 339(21) : 1506-14.(3iiiDiii)
9) Federico M, et al. Follicular lymphoma international prognostic index 2 : a new prognostic index for follicular lymphoma developed by the international follicular lymphoma prognostic factor project. J Clin Oncol. 2009 ; 27(27) : 4555-62.(3iDiii)
10) Cheson BD, et al. Report of an International Workshop to standardize response criteria for non-Hodgkin’s lymphomas. J Clin Oncol. 1999 ; 17(4) : 1244-53.
11) Cheson BD, et al. Revised response criteria for malignant lymphoma. J Clin Oncol. 2007 ; 25(5) : 579-86.
12) Juweid ME, et al. Response assessment of aggressive non-Hodgkin’s lymphoma by integrated International Workshop criteria(IWC) and 18F-fluorodeoxyglucose positron emission tomography(PET). J Clin Oncol. 2005 ; 23(21) : 4652-61.(3iiiDiii)
13) Weeks JC, et al. Value of follow-up procedures in patients with large-cell lymphoma who achieve a complete remission. J Clin Oncol. 1991 ; 9(7) : 1196-203.(3iiiD)
14) Oh YK, et al. Stages Ⅰ-Ⅲ follicular lymphoma : role of CT of the abdomen and pelvis in follow-up studies. Radiology. 1999 ; 210(2) : 483-6.(3iiiD)
15) Liedtke M, et al. Surveillance imaging during remission identifies a group of patients with more favorable aggressive NHL at time of relapse : a retrospective analysis of a uniformly-treated patient population. Ann Oncol. 2006 ; 17(6) : 909-13.(3iiiA)
16) Jerusalem G, et al. Early detection of relapse by whole-body positron emission tomography in the followup of patients with Hodgkin’s disease. Ann Oncol. 2003 ; 14(1) : 123-30.(3iiiD)
17) Zinzani PL, et al. Role of Fluorodeoxyglucose Positron Emission Tomography Scan in the Follow-Up of Lymphoma. J Clin Oncol. 2009 ; 27(11) : 1781-7.(3iiiD)
1
濾胞性リンパ腫
(follicular lymphoma:FL)
(follicular lymphoma:FL)
◆総論
濾胞性リンパ腫(follicular lymphoma:FL)は代表的な低悪性度B 細胞リンパ腫であり,非ホジキンリンパ腫に占める頻度は7~15%である1)2)。しかし,最近は増加しつつある。本項では消化管あるいは皮膚に発生する稀な節外性FL は治療に関するエビデンスが乏しいことから対象としない。経過が緩徐であり,進行期症例であってもリツキシマブ(R)登場以前のデータでは,生存期間中央値は7~10 年と長い。しかし,ほとんどの進行期症例は組織学的進展(histologic transformation)などによって化学療法抵抗性となり治癒困難な疾患群である。診断時75~90%の症例が臨床病期Ⅲ・Ⅳの進行期であり,骨髄浸潤を高率に認める3)。1980 年代の報告ではあるが,FL は再発率が高く,寛解期間は平均24 カ月で,無増悪生存割合(progression-free survival:PFS)は5 年後で30~40%,10 年後で25%とされている3)。全生存割合(overall survival:OS)を中・高悪性度非ホジキンリンパ腫と比べると,最初の10 年では35% vs 60%と高い一方,15 年では33%vs 26%とむしろ低い3)。このように寛解維持が困難で長期にわたって再発・再燃がみられるのは,FL の腫瘍細胞が中・高悪性度非ホジキンリンパ腫の腫瘍細胞に比し,化学療法剤に抵抗性であることによる。近年ではR の導入によって予後が改善している。
FL における病期分類はAnn Arbor 分類が用いられる。予後予測モデルとしては元来アグレッシブ リンパ腫の予後指標として開発された,国際予後指標(international prognostic index:IPI)4)が,FL をはじめとする低悪性度リンパ腫においても有用であることが報告された5)6)。しかしその後,濾胞性リンパ腫国際予後指標(Follicular Lymphoma International Prognostic Index:FLIPI)が,病型特異的予後予測モデルとして提唱された7)。さらに,FLIPI2 が提唱された8)。
【参考文献】
1) Lymphoma Study Group of Japanese Pathologists : The World Health Organization classification of malignant lymphomas in Japan : Incidence of recently recognized entities. Pathol Int. 2000 ; 50(9) : 696-702.
2) Izumo T, et al. Practical Utility of the revised European-American classification of lymphoid neoplasms for Japanese non-Hodgkin’s lymphomas. Jpn J Cancer Res. 2000 ; 91(3) : 351-60.
3) Rosenberg SA. Karnofsky memorial lecture. The low-grade non-Hodgkin’s lymphomas : challenges and opportunities. J Clin Oncol. 1985 ; 3(3) : 299-310.(3iA)
4) A predictive model for aggressive non-Hodgkin’s lymphoma. The International Non-Hodgkin’s Lymphoma Prognostic Factors Project. N Engl J Med. 1993 ; 329(14) : 987-94.(3iA)
5) López-Guillermo A, et al. Applicability of the International Index for aggressive lymphomas to patients with low-grade lymphoma. J Clin Oncol. 1994 ; 12(7) : 1343-8.(3iA)
6) Hermans J, et al. International Prognostic Index for aggressive non-Hodgkin’s lymphoma is valid for all malignancy grades. Blood. 1995 ; 86(4) : 1460-3.(3iA)
7) Solal-Céligny P, et al. Follicular lymphoma international prognostic index. Blood. 2004 ; 104(5) : 1258-65.(3iA)
8) Federico M, et al. Follicular lymphoma international prognostic index 2 : a new prognostic index for follicular lymphoma developed by the international follicular lymphoma prognostic factor project. J Clin Oncol. 2009 ; 27(27) : 4555-62.(3iDiii)
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
略語
RT:Radiotherapy
R:Rituximab
RIT:Radioimmunotherapy
RIC:Reduced-intensity conditioning
CMT:Combined modality therapy
現在国内適応外治療
R 維持療法(CQ4)
Ⅰ期ないし隣接するⅡ期の限局期では,エビデンスレベルは決して高いものではないが,すべての病巣が照射野内に含まれる限り,放射線治療は再発が少なく根治率は比較的高いとされる。したがって総線量30~36 Gy の放射線治療が一般的な治療選択であり,40%以上の症例に10 年以上の無病生存が得られるとの報告がある1)。
Ⅲ・Ⅳ期すなわち進行期における治癒指向的治療,あるいは生存期間を延長する標準治療はこれまでのところ存在しないが,近年有用性を示す治療法が開発されてきた。全身症状・巨大病変がなく,診断までの経過が緩慢な症例では,診断後直ちに治療を開始した群に生存期間が劣らないという観点より,病勢の進行あるいは症状が出現した際に適切な薬物療法を開始することを前提として,診断後病勢進行まで無治療経過観察(watchful wait)という選択肢が取られることもある2)。治療法としては,アルキル化剤単独,ドキソルビシン(DXR)を含まない併用化学療法,DXR を含む併用化学療法,化学療法とインターフェロンαの併用,自家あるいは同種造血幹細胞移植併用大量化学・放射線療法など,多種多様な治療法が行われてきた。しかし,これら治療間の優劣は明らかでなかった。化学療法剤に抵抗性であることから,化学療法と放射線療法を併用する複合療法も行われてきた。また,再発・再燃を繰り返す間にアルキル化剤や放射線治療が頻用され,自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)後には,治療関連骨髄異形成症候群または急性骨髄性白血病(treatment-related myelodysplastic syndrome or acute myeloid leukemia:tMDS/tAML)が自家移植5年後で12%の頻度で発生したとの報告がある3)。
キメラ型抗CD20 モノクローナル抗体リツキシマブ(R)が登場し,化学療法との併用で高い奏効割合が得られ,微小残存病変の消失まで得られることが報告されている。そして,従来の併用化学療法単独よりもR を併用した化学療法が,全生存期間の延長に寄与することが報告されている。さらに,放射性同位元素をマウス・モノクローナル抗CD20 抗体に結合させることにより,リンパ腫細胞を標的とした放射線治療が可能となった4)。
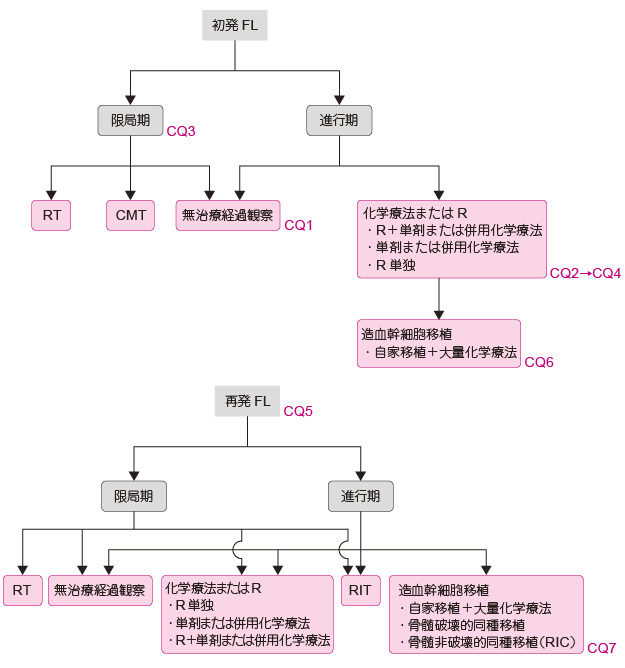
初発例では限局期のみ放射線治療の適応となる(CQ3)。進行期では初発例でも再発例でも①無治療経過観察(CQ1, CQ2)から,②単剤または併用化学療法,③ R 単独,④ ②と③の併用療法,(CQ2)などの治療方法から選択される。ただし,初発例に対してはR +化学療法のほうが化学療法単独よりも推奨される(カテゴリー1)。造血幹細胞移植療法は,初回治療後第一寛解期には推奨されない(CQ6)(カテゴリー4)が,再発進行期に検討され得る一つの治療選択肢である(CQ7)。CQ4 とCQ5 で言及する治療法は国内適応外である。
【参考文献】
1) Mac Manus MP, et al. Is radiotherapy curative for stage Ⅰ and Ⅱ low-grade follicular lymphoma? Results of a long-term follow-up study of patients treated at Stanford University. J Clin Oncol. 1996 ; 14(4) : 1282-90.(3iA)
2) Horning SJ, et al. The natural history of initially untreated low-grade non-Hodgkin’s lymphomas. N Engl J Med. 1984 ; 311(23) : 1471-5.(3iA)
3) Apostolidis J, et al. High-dose therapy with autologous bone marrow support as consolidation of remission in follicular lymphoma : long-term clinical and molecular follow-up. J Clin Oncol. 2000 ; 18 (3) : 527-36.(3iA)
4) Buchegger F, et al. Radiolabeled and native antibodies and the prospect of cure of follicular lymphoma. Oncologist. 2008 ; 13(6) : 657-67.(レビュー)
| CQ1 | 初発進行期(ⅢまたはⅣ期)FL に対してどのような場合に無治療経過観察とし,どのような場合に治療を開始するか |
|---|
-
推奨グレードなし
【解 説】
治療開始規準あるいは低腫瘍量の規準として国際的に統一されたものはない。海外の臨床試験グループで主な臨床試験に用いられてきた代表的な規準を以下に列挙する。
注)無治療経過観察は考慮されるべき方法であるが,明確な規準をもって示し得るような臨床試験のエビデンスがないため,推奨レベルをなしとした。実臨床においては,ここに挙げる規準を参照し,治療方針を決定することを推奨する。
1.BNLI(British National Lymphoma Investigation)1)(レビュー2)に引用)(カテゴリー2B)
以下のいずれも認めない場合,無治療経過観察とする。
- (1)B 症状または痒疹
- (2)急激な全身への病勢進行
- (3)骨髄機能障害(Hb≦10 g/dL,白血球<3,000/μL,または血小板<100,000/μL)
- (4)生命を脅かす臓器浸潤
- (5)腎浸潤
- (6)骨病変
- (7)肝浸潤
2.GELF(Grouped' Etude des Lymphomes Folliculaires)3)4)(レビュー2)に引用)(カテゴリー2B)
以下のいずれにも該当する(低腫瘍量の定義)場合,無治療経過観察とする。
- (1)節性病変,節外病変にかかわらず最大長径<7 cm
- (2)長径3 cm 以上の腫大リンパ節が3 つ未満
- (3)全身症状(B 症状)なし
- (4)下縁が臍線より下の脾腫(CT 上<16 cm)
- (5)胸水または腹水がない(細胞内容にかかわらず)
- (6)局所(硬膜,尿管,眼窩,胃腸などの)の圧迫症状の危険性なし
- (7)白血化(リンパ腫細胞>5,000/mm3)なし
- (8)骨髄機能障害(Hb<10 g/dL,好中球< 1,000/μL,血小板<100,000/μL)なし
- (9)LDH, β2 ミクログロブリン正常
3.GLSG(German Low-Grade Lymphoma Study Group)での臨床試験適格規準中の治療介入判断規準5)(カテゴリー2B)
以下のいずれかを認めるもの。
- (1)B 症状あり
- (2)Bulky(長径:縦隔では>7.5 cm,その他の部位>5 cm)
- (3)正常造血の障害
- (4)急速な病勢進行
【参考文献】
1) Ardeshna KM, et al. Long-term effect of a watch and wait policy versus immediate systemic treatment for asymptomatic advanced-stage non-Hodgkin lymphoma : a randomised controlled trial. Lancet. 2003 ; 362(9383) : 516-22.(1iiA)
2) Gribben JG. How I treat indolent lymphoma. Blood. 2007 ; 109(11) : 4617-26.(レビュー)
3) Brice P, et al. Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa : a randomized study from the Groupe d’Etude des Lymphomes Folliculaires. Groupe d’Etude des Lymphomes de l’Adulte. J Clin Oncol. 1997 ; 15 (3) : 1110-7.(1iiA/1iiDiii)
4) Solal-Céligny P, et al. Doxorubicin-containing regimen with or without interferon alfa-2b for advanced follicular lymphomas : final analysis of survival and toxicity in the Groupe d’Etude des Lymphomes Folliculaires 86 Trial. J Clin Oncol. 1998 ; 16(7) : 2332-8.
5) Hiddemann W, et al. Frontline therapy with rituximab added to the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone(CHOP) significantly improves the outcome for patients with advanced-stage follicular lymphoma compared with therapy with CHOP alone : results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood. 2005 ; 106 (12) : 3725-32.(1iiA)
| CQ2 | 初発進行期(ⅢまたはⅣ期)FL における標準治療は何が勧められるか |
|---|
標準治療は未確立ではあるが,いくつかの患者集団では高いエビデンスが示されている治療法があるため,列挙する。
-
推奨グレードカテゴリー1
- リツキシマブを併用した化学療法が従来の併用化学療法単独よりも全生存期間延長に寄与する。
【解 説】
リツキシマブ(R)を併用した化学療法が従来の化学療法単独よりも生存期間延長に寄与する1)~4)ことが報告されている。具体的な化学療法のレジメンとしてR-CVP 療法(R, CPA, VCR, PSL)2)やR-CHOP 療法(R, CPA, DXR, VCR, PSL)1)4)が挙げられる。R 登場以前にはアントラサイクリンは生存期間延長には寄与しないとされていたが,R-CHOP 療法とR-CVP 療法を比較したランダム化比較試験結果の論文報告はなく,現在最適なR 併用化学療法は明らかでない。また多剤併用療法の適応がない患者では,経口アルキル化剤(シクロホスファミドなど)単独治療5)(R 時代の現在に応用するなら単剤化学療法剤とそのR 併用があり得る)も候補となる。
-
推奨グレードカテゴリー1
- 無症候性の患者では,注意深い観察のもとに治療開始を延期することも考慮されるべきである。
【解 説】
エビデンスレベルの高い複数の臨床試験の結果6)7)から,無症候性の患者においては,注意深い観察のもとに治療開始を延期することも考慮されるべきである。無治療経過観察から最初の全身治療が必要になるまでの期間の中央値は2.6~3 年と報告された6)。
-
推奨グレードカテゴリー2A
- 低腫瘍量(CQ1:2. GELF 参照)の患者にはR 単独を初期治療として考慮してもよい。
【解 説】
低腫瘍量の患者にはR 単独を初期治療として考慮してもよい8)9)。しかし,この根拠となった第Ⅱ相試験9)において増悪までの期間の中央値は2.2 年であった。一部高腫瘍量の患者を含むため治療成績が低くなっている可能性は否定できないことを考慮しても,上記の無治療経過観察の治療開始までの期間を凌ぐものではなく,低腫瘍量において早期から治療開始したほうがよいことを支持するものではない。また,低腫瘍量でもR 併用化学療法を行っても構わない。
【参考文献】
1) Hiddemann W, et al. Frontline therapy with rituximab added to the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone(CHOP) significantly improves the outcome for patients with advanced- stage follicular lymphoma compared with therapy with CHOP alone : results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood. 2005 ; 106(12) : 3725-32.(1iiA)
2) Marcus R, et al. Phase Ⅲ study of R-CVP compared with cyclophosphamide, vincristine, and prednisone alone in patients with previously untreated advanced follicular lymphoma. J Clin Oncol. 2008 ; 26(28) : 4579-86.(1iiA/1iiDiii)
3) Schulz H, et al. Immunochemotherapy with rituximab and overall survival in patients with indolent or mantle cell lymphoma : a systematic review and meta-analysis. J Natl Cancer Inst. 2007 ; 99(9) : 706-14.(1iiA)
4) Fisher RI, et al. New treatment options have changed the survival of patients with follicular lymphoma. J Clin Oncol. 2005 ; 23(33) : 8447-52.(3iiiA)
5) Peterson BA, et al. Prolonged single-agent versus combination chemotherapy in indolent follicular lymphomas : a study of the cancer and leukemia group B. J Clin Oncol. 2003 ; 21(1) : 5-15.(1iiA)
6) Ardeshna KM, et al. Long-term effect of a watch and wait policy versus immediate systemic treatment for asymptomatic advanced-stage non-Hodgkin lymphoma : a randomised controlled trial. Lancet. 2003 ; 362(9383) : 516-22.(1iiA)
7) Brice P, et al. Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa : a randomized study from the Groupe d’Etude des Lymphomes Folliculaires. Groupe d’Etude des Lymphomes de l’Adulte. J Clin Oncol. 1997 ; 15(3) : 1110-7.(1iiA/1iiDiii)
8) Colombat P, et al. Rituximab (anti-CD20 monoclonal antibody) as single first-line therapy for patients with follicular lymphoma with a low tumor burden : clinical and molecular evaluation. Blood. 2001 ; 97(1) : 101-6.(3iiiDiv)
9) Witzig TE, et al. Rituximab therapy for patients with newly diagnosed, advanced-stage, follicular grade Ⅰ non-Hodgkin’s lymphoma : a phase II trial in the North Central Cancer Treatment Group. J Clin Oncol. 2005 ; 23(6) : 1103-8.(3iiiDiv)
| CQ3 | 初発限局期FL の標準治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- Ⅰ期または隣接するⅡ期の場合,病巣部放射線治療が推奨される。
-
推奨グレードカテゴリー3
- 放射線療法への化学療法の追加は推奨されない。
-
推奨グレードカテゴリー2B
- 多剤併用化学療法とのcombined modality therapy は考慮され得る。
-
推奨グレードカテゴリー2B
- 放射線治療が回避されるべき場合,無症候性の患者には無治療経過観察が考慮され得る。
【解 説】
未治療限局期FL でⅠ期または隣接するⅡ期の場合,病巣部放射線療法が推奨される1)2)。しかし,疾患全体に占める割合が少ないこともあり,エビデンスレベルは高くない。FL を含むindolent B-cell lymphoma に対する放射線療法では,局所制御に必要な照射線量は30~36 Gy で十分であるとの国際的な放射線腫瘍医のコンセンサスがある2)3)。
放射線療法への単剤あるいは多剤併用化学療法の追加が再発を少なくするという証拠はない4)。一方,多剤併用化学療法とのcombined modality therapy がhistorical control の放射線療法単独よりも成績が良いとの報告もある3)が,照射野内も含めた二次がんが14%も出現したのは問題である3)。
放射線療法が回避されるべき場合,無症候性の患者には無治療経過観察が考慮され得る5)。
【参考文献】
1) Pugh TJ, et al. Improved survival in patients with early stage low-grade follicular lymphoma treated with radiation : a Surveillance, Epidemiology, and End Results database analysis. Cancer. 2010 ; 116(16) : 3843-51.(2A)
2) Pendlebury S, et al. Radiotherapy results in early stage low grade nodal non-Hodgkin’s lymphoma. Radiother Oncol. 1995 ; 36(3) : 167-71.(3iA)
3) Seymour JF, et al. Long-term follow-up of a prospective study of combined modality therapy for stage Ⅰ-Ⅱ indolent non-Hodgkin’s lymphoma. J Clin Oncol. 2003 ; 21(11) : 2115-22.(3iiiA)
4) Kelsey SM, et al. A British National Lymphoma Investigation randomised trial of single agent chlorambucil plus radiotherapy versus radiotherapy alone in low grade, localised non-Hodgkins lymphoma. Med Oncol. 1994 ; 11(1) : 19-25.(1iiA)
5) Advani R, et al. Stage I and II follicular non-Hodgkin’s lymphoma : long-term follow-up of no initial therapy. J Clin Oncol. 2004 ; 22(8) : 1454-9.(3iiiA)
| CQ4 | 高腫瘍量の初発進行期FL に対してリツキシマブ維持療法を実施すべきか |
|---|
-
推奨グレードカテゴリー1
- GELF(Groupe d’Etude des Lymphomes Folliculaires)規準による高腫瘍量に対してのみ,リツキシマブ維持療法は無増悪生存期間の延長がみられる(ただし,国内適応外)。
【解 説】
リツキシマブ(R)維持療法はGELF 規準による高腫瘍量[①bulky 病変(≦7 cm),②長径3 cm 以上の別々の3 リンパ節,③症候性の脾腫,④腫瘍による臓器圧迫,⑤胸水または腹水,⑥血清LDH またはβ2 ミクログロブリンの上昇,⑦ B 症状あり,のいずれかを持つもの]のみ無増悪生存期間(PFS)を延長させるエビデンスがある1)。ただし,高腫瘍量に対しても,全生存期間(OS)を延長する証拠は示されていない。低腫瘍量の初発進行期FL に対してR 併用化学療法後のR 維持療法の意義を評価した臨床試験の報告はない。さらに現時点では,わが国ではR の維持療法はいかなる腫瘍量に対しても保険適用外である。
【参考文献】
1) Salles G, et al. Rituximab maintenance for 2 years in patients with high tumour burden follicular lymphoma responding to rituximab plus chemotherapy(PRIMA) : a phase 3, randomised controlled trial. Lancet. 2011 ; 377(9759) : 42-51.(1iiDiii)
| CQ5 | FL 初回再発時の治療選択としては何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 治療選択肢としてさまざまな方法があり,その優劣については比較検討した第Ⅲ相試験で論文として公表されたものは存在しない。
【解 説】
FL の初回再発時の治療選択肢は優劣が不明であるが,以下に示すものが挙げられる。
- ①無治療経過観察
- ②低腫瘍量の患者ではリツキシマブ(R)単独1)
- ③R 抵抗例ではベンダムスチン単独2)3)。あるいはR +ベンダムスチン4)
- ④R +フルダラビン(FLU)5)。FLU を含む多剤併用化学療法におけるR 併用の有無の比較試験で,マントル細胞リンパ腫では全生存で差がみられたのに対し,FL では全生存では差がなく無増悪生存でのみ化学療法単独との有意差があった5)。
- ⑤先行治療がアントラサイクリンを含まないレジメンの場合,R-CHOP 療法6)
- ⑥R を併用したその他の併用化学療法
- ⑦限局再発で照射可能である場合,放射線治療
- ⑧Radioimmunotherapy(RIT)7)。初回再発時のほうが,それ以降の再発時よりも,より良い完全奏効割合・奏効期間が期待される8)。なお,R を併用しない化学療法後の完全奏効・部分奏効が得られた例にのみRIT による地固め療法の有効性を示唆するエビデンスがある9)が,R を併用した化学療法による初回治療後では,その有用性は示されていない。RIT は本邦では再発・再燃例でのみ適応があり,初回治療に対する奏効後,引続いて地固め療法として用いる適応はない。
【参考文献】
1) McLaughlin P, et al. Rituximab chimeric anti-CD20 monoclonal antibody therapy for relapsed indolent lymphoma : half of patients respond to a four-dose treatment program. J Clin Oncol. 1998 ; 16(8) : 2825-33.(3iiiDiv)
2) Friedberg JW, et al. Bendamustine in patients with rituximab-refractory indolent and transformed non-Hodgkin’s lymphoma : results from a phase Ⅱ multicenter, single-agent study. J Clin Oncol. 2008 ; 26(2): 204-10.(3iiiDiv)
3) Kahl BS, et al. Bendamustine is effective therapy in patients with rituximab-refractory, indolent B-cell non-Hodgkin lymphoma : results from a Multicenter Study. Cancer. 2010 ; 116(1) : 106-14.(3iiiDiv)
4) Rummel MJ, et al. Bendamustine Plus Rituximab Versus Fludarabine Plus Rituximab In Patients with Relapsed Follicular, Indolent and Mantle Cell Lymphomas-Final Results of the Randomized Phase Ⅲ Study NHL 2-2003 on Behalf of the StiL(Study Group Indolent Lymphomas, Germany). Blood. 2010 ; 116 : abstract856.(1iiDiii)
5) Forstpointner R, et al. The addition of rituximab to a combination of fludarabine, cyclophosphamide, mitoxantrone(FCM) significantly increases the response rate and prolongs survival as compared with FCM alone in patients with relapsed and refractory follicular and mantle cell lymphomas : results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood. 2004 ; 104(10) : 3064-71.(1iiDiv/1iiDiii)
6) van Oers MH, et al. Rituximab maintenance improves clinical outcome of relapsed/resistant follicular non-Hodgkin lymphoma in patients both with and without rituximab during induction : results of a prospective randomized phase 3 intergroup trial. Blood. 2006 ; 108(10) : 3295-301.(1iiDiv)
7) Kaminski MS, et al. Radioimmunotherapy with iodine(131)I tositumomab for relapsed or refractory B-cell non-Hodgkin lymphoma : updated results and long-term follow-up of the University of Michigan experience. Blood. 2000 ; 96(4) : 1259-66.(3iiiDiv)
8) Emmanouilides C, et al. Treatment with yttrium 90 ibritumomab tiuxetan at early relapse is safe and effective in patients with previously treated B-cell non-Hodgkin’s lymphoma. Leuk Lymphoma. 2006 ; 47(4) : 629-36.(3iiiDiv)
9) Morschhauser F, et al. Phase Ⅲ trial of consolidation therapy with yttrium-90-ibritumomab tiuxetan compared with no additional therapy after first remission in advanced follicular lymphoma. J Clin Oncol. 2008 ; 26(32) : 5156-64.(1iiDiii)
| CQ6 | FL における自家移植の適応はup-front で行うべきか |
|---|
-
推奨グレードカテゴリー4
- FL において,自家移植は初回治療に奏効した後に引続きup-front で行うべきではない。
【解 説】
初回治療に奏効した後に引続きup-front で行うべきではない1)~5)。その理由として,二次がんの発生が増加することが報告されている2)4)5)。リツキシマブ(R)導入後の現在において,自家移植を何度目の再発時に施行すべきかは不明である。
R 導入以前には,再発例に対して,通常量の化学療法に比較して大量化学療法(high-dose chemotherapy:HDC)が全生存期間(OR)を延長するとされたが,R の導入により自家移植以外の再発後の治療成績も向上した6)(カテゴリー2A)。ただし,この結果はR を含まない化学療法が初回治療として行われた患者に基づく結果で,またOS は再発時を起点としており,診断時からのOS ではなかった6)。また,初回治療中にR の投与を受けた患者においても,再発時にR を併用した自家移植が再発以後のOS を延長することが示された7)。現時点では自家移植は再発FL 例の無増悪生存期間(PFS)を延長する治療選択肢の一つと考えられる。
【参考文献】
1) Sebban C, et al. Standard chemotherapy with interferon compared with CHOP followed by high-dose therapy with autologous stem cell transplantation in untreated patients with advanced follicular lymphoma : the GELF-94 randomized study from the Groupe d’Etude des Lymphomes de l’Adulte (GELA). Blood. 2006 ; 108(8) : 2540-4.(1iiA/1iiDiii)
2) Deconinck E, et al. High-dose therapy followed by autologous purged stem-cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma : a randomized multicenter study by GOELAMS. Blood. 2005 ; 105(10) : 3817-23.(1iiA/1iiDiii)
3) Lenz G, et al. Myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission prolongs progression-free survival in follicular lymphoma : results of a prospective, randomized trial of the German Low-Grade Lymphoma Study Group. Blood. 2004 ; 104(9) : 2667-74.(1iiA/1iiDiii)
4) Ladetto M, et al. Prospective, multicenter randomized GITMO/IIL trial comparing intensive(R-HDS) versus conventional(CHOP-R) chemoimmunotherapy in high-risk follicular lymphoma at diagnosis : the superior disease control of R-HDS does not translate into an overall survival advantage. Blood. 2008 ; 111(8) : 4004-13.(1iiA/1iiDiii)
5) Gyan E, et al. High-dose therapy followed by autologous purged stem cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma : a randomized multicenter study by the GOELAMS with final results after a median follow-up of 9 years. Blood. 2009 ; 113(5) : 995-1001.(1iiA/1iiDiii)
6) Sebban C, et al. Impact of rituximab and/or high-dose therapy with autotransplant at time of relapse in patients with follicular lymphoma : a GELA study. J Clin Oncol. 2008 ; 26(21) : 3614-20.(3iA)
7) Le Gouill S, et al. Impact of the use of autologous stem cell transplantation at first relapse both in naive and previously rituximab exposed follicular lymphoma patients treated in the GELA/GOELAMS FL2000 study. Haematologica. 2011 ; 96(8) : 1128-35.(3iA)
| CQ7 | 再発FL に対して自家移植と同種造血幹細胞移植はそれぞれ妥当な治療選択肢であるか |
|---|
-
推奨グレードカテゴリー2A
- 自家移植と同種移植では後者のほうが治療関連死亡は高いが再発が少ない。このため両治療間で生存においては差がなく,両者とも選択肢となり得る。
【解 説】
自家移植と同種移植では後者のほうが治療関連死亡(TRM)は高いが再発が少ない。このため両治療間で生存においては差がない1)~4)。従来再発が比較的多いとされてきた自家移植例でも最近生存曲線のプラトーが示されるようになった5)6)。しかし,二次がん特にtMDS/AML の増加が問題とされている。いずれもシクロホスファミド大量+全身照射が前処置に用いられていた5)6)。
骨髄非破壊的(Reduced-intensity conditioning:RIC)造血幹細胞移植の導入により,TRM が減少した7)結果,自家移植よりも同種移植のほうが良いとの報告がある8)(カテゴリー2B)。しかしこれは,ヒト主要組織適合性抗原(human leukocyte antigen:HLA)一致同胞がいる場合には同種,いない場合には自家移植を受けた比較試験で,患者集積ペースが遅く早期中止となった臨床試験のデータである。RIC が同種移植の中で標準治療になりつつあるが,Center for IBMTR のレジストリー・データの多変量解析により,RIC に比べ骨髄破壊的造血幹細胞移植の方がより再発が少ないという報告がある9)(カテゴリー2B)。ただし,両者間で無増悪生存期間,全生存期間とも統計学的に有意差はなく,RIC 群では比較的高齢者が多く,診断から移植までの期間が長かった9)ことから,両者間の優劣の判断は困難である。
European Group for Blood and Marrow Transplantation(EBMT)のレジストリー・データから,HLA 適合非血縁者間の同種移植では3 年全生存割合51%,3 年無増悪生存割合47%,1 年次の無再発死亡率は30%と報告された10)(カテゴリー2B)。以上より,同種移植は若年者で,再発を繰り返す患者,奏効期間の短い患者での治療選択肢のひとつと考えられている。
【参考文献】
1) van Besien K, et al. Comparison of autologous and allogeneic hematopoietic stem cell transplantation for follicular lymphoma. Blood. 2003 ; 102(10) : 3521-9.(3iA)
2) Bierman PJ, et al. Syngeneic hematopoietic stem-cell transplantation for non-Hodgkin’s lymphoma : a comparison with allogeneic and autologous transplantation--The Lymphoma Working Committee of the International Bone Marrow Transplant Registry and the European Group for Blood and Marrow Transplantation. J Clin Oncol. 2003 ; 21(20) : 3744-53.(3iA/3iDi)
3) Ingram W, et al. Outcome of BEAM-autologous and BEAM-alemtuzumab allogeneic transplantation in relapsed advanced stage follicular lymphoma. Br J Haematol. 2008 ; 141(2) : 235-43.(3iA)
4) Hosing C, et al. Long-term results favor allogeneic over autologous hematopoietic stem cell transplantation in patients with refractory or recurrent indolent non-Hodgkin’s lymphoma. Ann Oncol. 2003 ; 14(5) : 737-44.(3iA)
5) Gyan E, et al. High-dose therapy followed by autologous purged stem cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma : a randomized multicenter study by the GOELAMS with final results after a median follow-up of 9 years. Blood. 2009 ; 113(5) : 995-1001.(1iiA/1iiDiii)
6) Rohatiner AZ, et al. Myeloablative therapy with autologous bone marrow transplantation for follicular lymphoma at the time of second or subsequent remission : long-term follow-up. J Clin Oncol. 2007 ; 25(18) : 2554-9.(3iA)
7) Khouri IF, et al. Nonablative allogenic hematopoietic transplantation as adoptive immunotherapy for indolent lymphoma : low incidence of toxicity, acute graft-versus-host disease, and treatment-related mortality. Blood. 2001 ; 98(13) : 3595-9.(3iA/3iDiv)
8) Tomblyn MR, et al. Autologous versus reduced-intensity allogeneic hematopoietic cell transplantation for patients with chemosensitive follicular non-Hodgkin lymphoma beyond first complete response or first partial response. Biol Blood Marrow Transplant. 2011 ; 17(7) : 1051-7.(2A/2Diii)
9) Hari P, et al. Allogeneic transplants in follicular lymphoma : higher risk of disease progression after reduced-intensity compared to myeloablative conditioning. Biol Blood Marrow Transplant. 2008 ; 14 (2) : 236-45.(3iB)
10) Avivi I, et al. Matched unrelated donor stem cell transplant in 131 patients with follicular lymphoma : an analysis from the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. Br J Haematol. 2009 ; 147(5) : 719-28.(3iA)
2
MALT リンパ腫/辺縁帯リンパ腫
(acute promylocytic leukemia:APL)
(acute promylocytic leukemia:APL)
◆総論
MALT(Mucosa associated lymphoid tissue)リンパ腫/粘膜関連リンパ組織型節外性辺縁帯リンパ腫(節外性辺縁帯リンパ腫)は,WHO 分類(2008)によると,胚中心細胞類似細胞(centrocyte-like cell),単球様B 細胞(monocytoid B cell),小型リンパ球,および,大型芽球様細胞など形態的に多彩な細胞が混在し,主に濾胞辺縁帯(marginal zone)から濾胞間に浸潤・増殖するリンパ腫と定義される1)2)。一部は,形質細胞への分化を認めたり,上皮内に浸潤しlymphoepithelial lesion(LEL)を形成したりする。発生部位により,粘膜関連リンパ組織型節外性辺縁帯リンパ腫(MALT リンパ腫),節性辺縁帯リンパ腫,脾B 細胞辺縁帯リンパ腫に分類される。また,MALT リンパ腫は,臨床的にgastric とnon-gastric とに分類する。
辺縁帯リンパ腫の病因の一部には,感染症・炎症が関係していると考えられており3),胃MALT リンパ腫でHelicobacter pylori の感染頻度は50~100%である4)。そのほかCampylobacter jejuni が小腸,Borrelia burgdorferi が皮膚,Chlamydia psittaci が眼附属器のMALT リンパ腫に関連していることが報告されている。脾B 細胞辺縁帯リンパ腫ではC 型肝炎ウイルスとの関連が示唆されている。唾液腺,甲状腺のMALT リンパ腫は自己免疫疾患に関係しており,それぞれシェーグレン症候群,橋本病などの自己免疫疾患に比較的高頻度に合併するMALT リンパ腫に認められる。特有な染色体異常として,t (11;18)(q21;q21),t (1;14)(p22;q32),t (14;18)(q32;q21),t (3;14)(p14.1;q32),6q23欠失が知られている。これらの責任遺伝子産物は,t (3;14)(p14.1;q32) を除いて,NF-κB の恒常的活性化につながっており,炎症がこの腫瘍の成因に関連している証左となっている。
胃MALT リンパ腫は胃悪性リンパ腫の約40%を占める。病理組織学的検索と同時に多くの患者で認められるH. pylori の有無を調べることが重要である5)6)。病期決定のための頸部~鼠径部CT,骨髄検査などを必ず実施する。超音波内視鏡により病変の深達度,所属リンパ節への浸潤有無の診断が可能である。病期分類は,Lugano 病期分類が使用されることが多く,Ann Arbor 病期分類での病期Ⅲ期がなく,Ⅳ期と扱われる(悪性リンパ腫総論参照)。また,深達度などを明確にしたTNM 分類が欧米では用いられることがある。
胃以外の節外臓器に発生するMALT リンパ腫は,大腸,肺,甲状腺,唾液腺,乳腺,眼科領域などに発生するものがある。これらは,低悪性度B 細胞リンパ腫に準じて治療方針が決定される。注意深い経過観察は,症状がなく,慎重に腫瘍の消長をみることができる部位であれば選択肢の一つとなり得る。
節性辺縁帯リンパ腫は極めて稀であり,節外性辺縁帯リンパ腫(MALT リンパ腫)病変がないかどうかを慎重に評価する7)。
脾B 細胞辺縁帯リンパ腫はCD5 が陰性であること,CD20 が強陽性であることがCLL とは異なる。CD23 の発現程度はさまざまである。特徴的な絨毛が診断の契機となることがある。脾腫,汎血球減少が特徴的とされるが,認めないこともある8)。C 型肝炎合併例を認めることがあり,その場合には,C 型肝炎治療で奏効を得た報告例がある9)10)。脾摘は,脾腫による症状や汎血球減少がある場合に,診断を兼ねて行われる。
【参考文献】
1) Isaacson PG, et al. Extranodal marginal zone lymphoma of mucosa-associated lymphoid tissue (MALT lymphoma). Swerdlow SH, et al, eds. WHO Classification of Tumours of Haematopoietic and Lymphoid tissues, Lyon, IARC ; 2008 : pp214-9.
2) Campo E, et al. Nodal marginal zone lymphoma. Swerdlow SH, et al, eds. WHO Classification of Tumours of Haematopoietic and Lmphoid Tissues, Lyon, IARC ; 2008 : pp218-9.
3) Guidoboni M, et al. Infectious agents in mucosa-associated lymphoid tissue-type lymphomas : pathogenic role and therapeutic perspectives. Clin Lymphoma Myeloma. 2006 ; 6(4) : 289-300.(レビュー)
4) Asenjo LM, Gisbert JP. [Prevalence of Helicobacter pylori infection in gastric MALT lymphoma : a systematic review] Rev Esp Enferm Dig. 2007 ; 99(7) : 398-404.(レビュー)
5) Wotherspoon AC, et al. Helicobacter pylori-associated gastritis and primary B-cell gastric lymphoma. Lancet. 1991 ; 338(8776) : 1175-6.(レビュー)
6) Cohen SM, et al. Non-Hodgkin’s lymphoma of mucosa-associated lymphoid tissue. Oncologist. 2006 ; 11(10) : 1100-17.(レビュー)
7) Tsimberidou AM, et al. Outcomes in patients with splenic marginal zone lymphoma and marginal zone lymphoma treated with rituximab with or without chemotherapy or chemotherapy alone. Cancer. 2006 ; 107(1) : 125-35.(3iiiA)
8) Franco V, et al. Splenic marginal zone lymphoma. Blood. 2003 ; 101(7) : 2464-72.(レビュー)
9) Weng WK, et al. Hepatitis C virus(HCV) and lymphomagenesis. Leuk Lymphoma. 2003 ; 44(7) : 1113-20.(レビュー)
10) Hermine O, et al. Regression of splenic lymphoma with villous lymphocytes after treatment of hepatitis C virus infection. N Engl J Med. 2002 ; 347(2) : 89-94.(3iiiDiv)
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
アルゴリズム 1
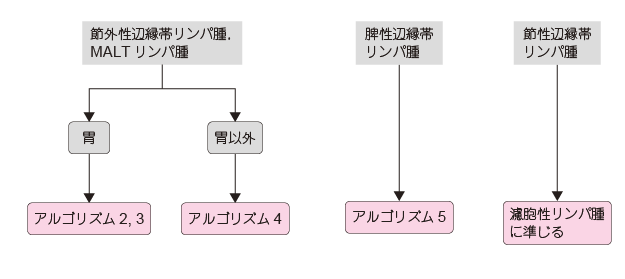
疾患の位置づけを示す。胃MALT リンパ腫はアルゴリズム2 で示し,進展期,無効の場合はア ルゴリズム3 で示した。胃以外のMALT リンパ腫はアルゴリズム4 参照。節性辺縁帯リンパ腫は FL に準じる。脾B 細胞辺縁帯リンパ腫ではアルゴリズム5 を参照。
アルゴリズム 2
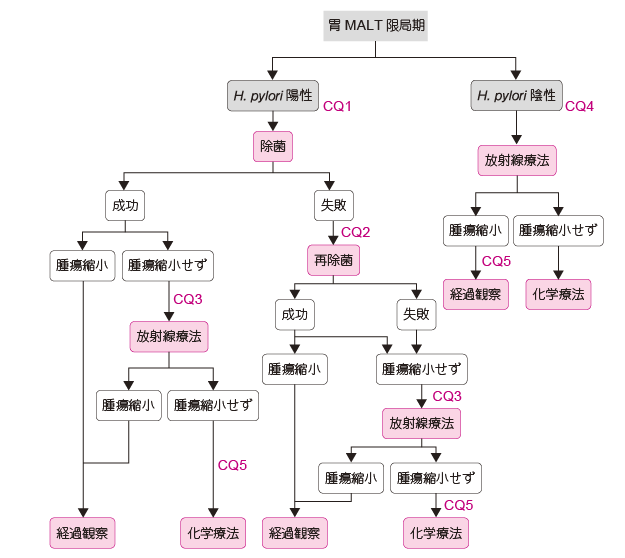
胃MALT リンパ腫の治療アルゴリズムを示す。H. pylori 陽性例は50~100%と報告されており,除菌療法は,90%以上で成功する。除菌療法が成功すれば,MALT リンパ腫に対しても高率に奏効が得られ(50~80%)1),60~100%で長期完全奏効が得られる2)。完全奏効に至るまでの時間は数カ月から1 年の例もあり,長期に経過を観察することが重要である3)。
抗がん薬を追加するメリットは認められてない4)。
一次除菌失敗例では,二次治療を実施する。除菌療法で奏効が得られない場合には,放射線療法が推奨される5)。厚生労働省がん研究助成金「消化管悪性リンパ腫に対する非外科的治療の適応と有効性の評価に関する研究班」によると,除菌療法無効例に対する放射線療法単独療法の第Ⅱ相試験では,90%以上で組織学的消失を認めている6)。
胃MALT リンパ腫のうち,H. pylori 陰性例は10~40%と報告されている7)。H. pylori 陰性かつ限局期(Lugano 分類でII1 期以下)の場合には,放射線療法8)を検討する。リツキシマブ(R)単剤治療の報告もある9)。H. pylori 陰性でも抗生物質を投与した場合に一定の割合で有効例が得られることが知られており,進行が緩徐であって胃に限局している場合には除菌療法を試みることがある10)。
アルゴリズム 3
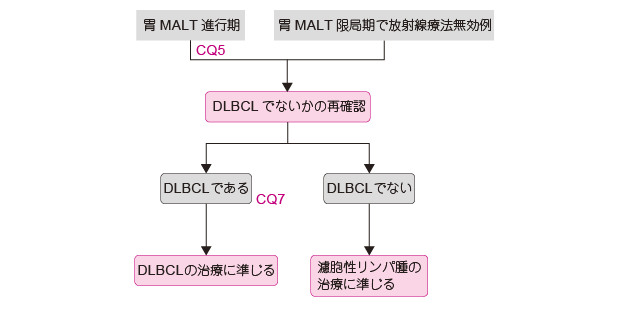
胃のMALT リンパ腫の進展期の場合は,まず,全身化学療法を直ちに実施すべきか否かを判断する。症状を有する場合,臓器障害(出血など)を認める場合,巨大腫瘤を有する場合,確実に進行を認める場合などが化学療法の適応となる。化学療法を行うのであれば,低悪性度B 細胞リンパ腫の代表的疾患である濾胞性リンパ腫(follicular lymphoma:FL)に準じた治療が行われる。アントラサイクリンを含んだ併用療法を初回から行うことは少なく,トランスフォームした可能性のある場合やbulky disease に対しては考慮すべきである。
再発時には,まず,その組織診断を実施することが必須である。初発診断時の病理組織が,必ずしも全体像を反映していなかった可能性[びまん性大細胞型B 細胞リンパ腫(diffuse large B cell lymphoma:DLBCL)の混在]やトランスフォームする可能性があるため,再生検は必須である。再生検の結果,DLBCL と診断された場合には,胃原発DLBCL として治療する。留意すべきことは,経過観察中の患者で胃がんの発生が認められた例があることである。これは,放射線による直接的影響なのか,H. pylori 感染者では胃がん発症リスクが高いためなのかは明らかではない11)12)。
アルゴリズム 4
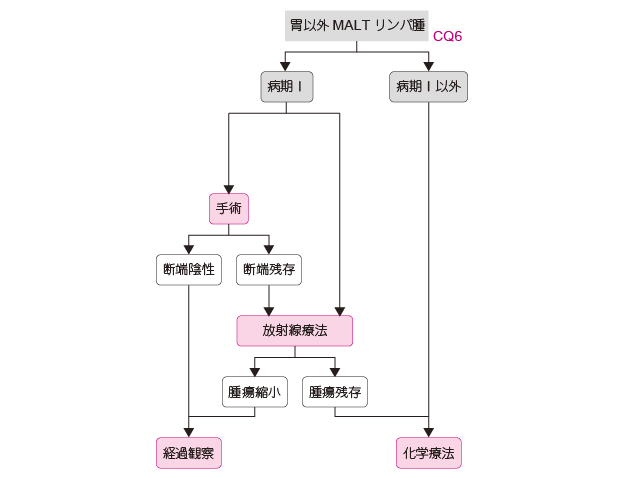
胃以外のMALT リンパ腫で限局期の場合には,注意深い経過観察以外に,放射線療法や外科的摘出が考慮される。また,外科的に摘出された後で診断された場合には,完全に摘除されたか残存しているかの判定が重要である。残存があるようなら,放射線療法を考慮する。また,限局期再発の場合にも放射線療法は選択肢の一つとなる。
進行期の場合は,注意深い経過観察に加えて,化学療法も考慮される。化学療法はFL に代表される低悪性度B 細胞リンパ腫に準じた治療方針が推奨される。大型細胞が混じる組織型の場合には,DLBCL に準じた治療方針が推奨される13)。
アルゴリズム 5
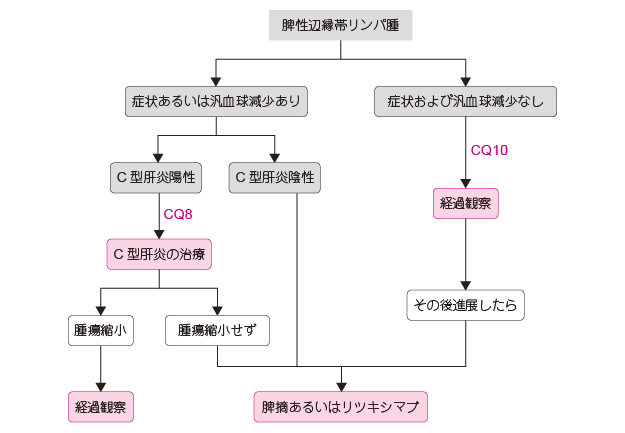
C 型肝炎合併の場合,C 型肝炎治療で奏効を得た報告例がある14)。脾摘は,脾腫による症状や汎血球減少がある場合に,診断を兼ねて行われる。脾B 細胞辺縁帯リンパ腫の薬物療法を行う場合には,まずR 単剤治療を考慮する。これにより長期の奏効が得られた例がある。これらの治療でも進行,再燃した場合にFL に準じた治療が行われる。
参考文献
1) Cohen SM, et al. Non-Hodgkin’s lymphoma of mucosa-associated lymphoid tissue. Oncologist, 2006 ; 11(10) : 1100-17.(レビュー)
2) Nakamura S, et al. Helicobacter pylori-negative gastric mucosa-associated lymphoid tissue lymphoma : a clinicopathologic and molecular study with reference to antibiotic treatment. Cancer. 2006 ; 107 (12) :2770-8.(3iiiDiv)
3) Fischbach W, et al. Most patients with minimal histological residuals of gastric MALT lymphoma after successful eradication of Helicobacter pylori can be managed safely by a watch and wait strategy : experience from a large international series. Gut. 2007 ; 56(12) : 1685-7.(3iiiDiii)
4) Levy M, et al. Conservative treatment of primary gastric low-grade B-cell lymphoma of mucosa-associated lymphoid tissue : predictive factors of response and outcome. Am J Gastroenterol. 2002 ; 97(2) : 292-7. (3iiiDiv)
5) Goda JS, et al. Long-term outcome in localized extranodal mucosa-associated lymphoid tissue lymphomas treated with radiotherapy. Cancer. 2010 ; 116(16) : 3815-24.(3iiiA)
6) 大津 敦.消化管悪性リンパ腫に対する非外科的治療の適応と有効性の評価に関する研究.平成10 年厚生労働省がん研究助成金による報告書.1998425-456.(3iiiDiv)
7) Ye H, et al. High incidence of t(11;18)(q21;q21) in Helicobacter pylori-negative gastric MALT lymphoma. Blood. 2003 ; 101(7) : 2547-50.(3iiiDiii)
8) Schechter NR, et al. Treatment of mucosa-associated lymphoid tissue lymphoma of the stomach with radiation alone. J Clin Oncol. 1998 ; 16(5) : 1916-21.(3iiDi)
9) Martinelli G, et al. Clinical activity of rituximab in gastric marginal zone non-Hodgkin’s lymphoma resistant to or not eligible for anti-Helicobacter pylori therapy. J Clin Oncol. 2005 ; 23(9) : 1979-83.(3iiiDiv)
10) Raderer M, et al. Successful antibiotic treatment of Helicobacter pylori negative gastric mucosa associated lymphoid tissue lymphomas. Gut. 2006 ; 55(5) : 616-8.(3iiiDiv)
11) Suenaga M, et al. Colliding gastric and intestinal phenotype well-differentiated adenocarcinoma of the stomach developing in an area of MALT-type lymphoma. Gastric cancer : official journal of the International Gastric Cancer Association and the Japanese Gastric Cancer Association. 2003 ; 6 (4) : 270-6.(3iiiDiv)
12) Raderer M, et al. Early cancer of the stomach arising after successful treatment of gastric MALT lymphoma in patients with autoimmune disease. Scand J Gastroenterol. 2003 ; 38(3) : 294-7.(3iiiDiv)
13) Ghesquières H, et al. Clinicopathologic characteristics and outcome of diffuse large B-cell lymphomas presenting with an associated low-grade component at diagnosis. J Clin Oncol. 2006 ; 24 (33) : 5234-41.(3iiDiii)
14) Hermine O, et al. Regression of splenic lymphoma with villous lymphocytes after treatment of hepatitis C virus infection. N Engl J Med. 2002 ; 347(2) : 89-94.(3iiiDiv)
| CQ1 | H. pylori 陽性限局期胃MALT リンパ腫の初期治療方針は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- H. pylori 陽性限局期MALT リンパ腫には,H. pylori 除菌療法が推奨される。
【解 説】
胃MALT リンパ腫患者におけるH. pylori の感染頻度は50~100%以上であると報告されている1),H. pylori 感染の有無の確認が治療方針の決定において重要である。H. pylori 陽性限局期MALTリンパ腫においては,H. pylori 除菌療法が,第一選択となる。除菌療法による奏効割合は50~80%で2)~4),90%以上の長期生存割合が得られている。除菌療法成功後,MALT リンパ腫が消失するまでの期間は中央値で数カ月であるが,数年かかることもある。除菌により奏効が得られた症例の再発割合は,3%である3)。一方,除菌失敗例のうち,リンパ腫の進展を認めた割合は27%である4)。したがって,リンパ腫病変が残存しても,除菌が成功した場合には,リンパ腫の進展がなければ,定期的な内視鏡検査と生検により経過観察を行う5)。t (11;18)/API2-MALT1 を有する場合には,除菌療法の成功率は低い5)。
【参考文献】
1) Asenjo LM, Gisbert JP. [Prevalence of Helicobacter pylori infection in gastric MALT lymphoma : a systematic review] Rev Esp Enferm Dig. 2007 ; 99(7) : 398-404.(レビュー)
2) Bertoni F, et al. Molecular follow-up in gastric mucosa-associated lymphoid tissue lymphomas : early analysis of the LY03 cooperative trial. Blood. 2002 ; 99(7) : 2541-4.(3iiDi)
3) Nakamura S, et al. Long-term clinical outcome of gastric MALT lymphoma after eradication of Helicobacter pylori : a multicentre cohort follow-up study of 420 patients in Japan. Gut. 2012 ; 61 (4) : 507-13.(3iiiA)
4) Thiede C, et al. Long-term persistence of monoclonal B cells after cure of Helicobacter pylori infection and complete histologic remission in gastric mucosa-associated lymphoid tissue B-cell lymphoma. J Clin Oncol. 2001 ; 19(6) : 1600-9.(3iiiDiii)
5) Ye H, et al. High incidence of t(11;18)(q21;q21) in Helicobacter pylori-negative gastric MALT lymphoma. Blood. 2003 ; 101(7) : 2547-50.(3iiiDiii)
| CQ2 | H. pylori 陽性限局期胃MALT リンパ腫で除菌失敗の時の治療法は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- H. pylori 陽性限局期MALT リンパ腫で除菌失敗の時は,再度のH. pylori 除菌療法が推奨される。
【解 説】
わが国では,プロトンポンプ阻害薬+アモキシシリン+クラリスロマイシンを1 週間投与する3 剤併用療法が一次除菌治療として行われる1)。80~90%の除菌率であり,除菌不成功の最大の原因はクラリスロマイシン耐性菌である。日本ヘリコバクター学会の耐性菌サーベイランス委員会の報告で2000 年には7%程度であったクラリスロマイシン耐性率が,2005 年には30%近くまで上昇している。一次除菌で不成功であった症例に対して,二次除菌として,クラリスロマイシンをメトロニダゾールに変えたレジメンで除菌を行う1)。
【参考文献】
1) 浅香正博ほか.H. pylori 感染の診断と治療のガイドライン2009 年改訂版. Japanese Journal of Helicobacter Research. 2009 ; 10(Supple) : 1-25.(ガイドライン)
| CQ3 | 除菌後にリンパ腫の残存がみられる場合の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2B
- リンパ腫の残存がみられる場合には放射線療法またはリツキシマブ単剤か免疫化学療法を考慮する。
【解 説】
リンパ腫が残存する場合やリンパ腫による症状を認める場合には,放射線療法1)~4)またはリツキシマブ(R)単剤5)か免疫化学療法を考慮する6)。ただし,免疫化学療法に比べて,放射線療法の奏効割合の方が高い5)。t (11;18)/API2-MALT1 を有する症例は除菌療法に抵抗性であり7),除菌以外の治療を考慮する。いずれの場合でも,リンパ腫の残存が認められる場合には,MALT リンパ腫の残存のほか,DLBCL への進展を確認するため,繰り返し生検を実施することが重要である。DLBCL への進展は約3%で,再発または除菌失敗例に限れば,約25%であった8)。除菌により奏効が得られた場合に追加の化学療法をしても,再発は防止できないので,経過観察をする9)。除菌が成功し,胃MALT リンパ腫の奏効が得られても,遅発性再発が生じ得るため,長期の経過観察が必要である10)。
【参考文献】
1) Fung CY, et al. Mucosa-associated lymphoid tissue lymphoma of the stomach : long term outcome after local treatment. Cancer. 1999 ; 85(1) : 9-17.(3iiiA)
2) Tsang RW, et al. Localized mucosa-associated lymphoid tissue lymphoma treated with radiation therapy has excellent clinical outcome. J Clin Oncol. 2003 ; 21(22) : 4157-64.(3iiiA)
3) Vrieling C, et al. Long-term results of stomach-conserving therapy in gastric MALT lymphoma. Radiother Oncol. 2008 ; 87(3) : 405-11.(3iiDi)
4) Schechter NR, et al. Treatment of mucosa-associated lymphoid tissue lymphoma of the stomach with radiation alone. J Clin Oncol. 1998 ; 16(5) : 1916-21.(3iiDi)
5) Raderer M, et al. Rituximab for treatment of advanced extranodal marginal zone B cell lymphoma of the mucosa-associated lymphoid tissue lymphoma. Oncology. 2003 ; 65(4) : 306-10.(3iiiDiv)
6) Zullo A, et al. Treatment of low-grade gastric MALT-lymphoma unresponsive to Helicobacter pylori therapy : a pooled-data analysis. Med Oncol. 2010 ; 27(2) : 291-5.(3iiiDiv)
7) Ye H, et al. High incidence of t (11;18)(q21;q21) in Helicobacter pylori-negative gastric MALT lymphoma. Blood. 2003 ; 101(7) : 2547-50.(3iiiDiii)
8) Thiede C, et al. Long-term persistence of monoclonal B cells after cure of Helicobacter pylori infection and complete histologic remission in gastric mucosa-associated lymphoid tissue B-cell lymphoma. J Clin Oncol. 2001 ; 19(6) : 1600-9.(3iiiDiii)
9) Hancock BW, et al. Chlorambucil versus observation after anti-Helicobacter therapy in gastric MALT lymphomas : results of the international randomised LY03 trial. Br J Haematol. 2009 ; 144 (3) : 367-75.(1iiDiii)
10)Wündisch T, et al. Long-term follow-up of gastric MALT lymphoma after Helicobacter pylori eradication. J Clin Oncol. 2005 ; 23(31) : 8018-24.(3iiiDiii)
| CQ4 | H. pylori 陰性限局期胃MALT リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2B
- H. pylori 陰性限局期胃MALT リンパ腫には,放射線療法が推奨される。
【解 説】
MALT リンパ腫において,報告例をまとめると20%前後の症例がH. pylori の感染を認めない1)。H. pylori 陰性胃MALT リンパ腫には,t (11;18)/API2-MALT1 の頻度が高い2)。この転座の有無にかかわらずH. pylori 陰性限局期MALT リンパ腫においては,放射線療法を考慮する3)~5)。ごく少数例でのみ除菌療法での有効例がある6)。
【参考文献】
1) Asenjo LM, Gisbert JP. [Prevalence of Helicobacter pylori infection in gastric MALT lymphoma : a systematic review] Rev Esp Enferm Dig. 2007 ; 99(7) : 398-404.(レビュー)
2) Ye H, et al. High incidence of t (11;18)(q21;q21) in Helicobacter pylori-negative gastric MALT lymphoma. Blood. 2003 ; 101(7) : 2547-50.(3iiiDiii)
3) Fung CY, et al. Mucosa-associated lymphoid tissue lymphoma of the stomach : long term outcome after local treatment. Cancer. 1999 ; 85(1) : 9-17.(3iiiA)
4) Tsang RW, et al. Localized mucosa-associated lymphoid tissue lymphoma treated with radiation therapy has excellent clinical outcome. J Clin Oncol. 2003 ; 21(22) : 4157-64.(3iiiA)
5) Vrieling C, et al. Long-term results of stomach-conserving therapy in gastric MALT lymphoma. Radiother Oncol. 2008 ; 87(3) : 405-11.(3iiDi)
6) Raderer M, et al. Successful antibiotic treatment of Helicobacter pylori negative gastric mucosa associated lymphoid tissue lymphomas. Gut. 2006 ; 55(5) : 616-8.(3iiiDiv)
| CQ5 | 進行期胃MALT リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 進行期胃MALT リンパ腫では,低悪性度B 細胞リンパ腫(FL など)に準じて,リツキシマブ±化学療法もしくは慎重な経過観察が推奨される。
【解 説】
進行期胃MALT リンパ腫は,診断時から進展している場合と限局期から進展する場合の両者が考えられる。いずれの場合も,疾患の頻度が低く大規模な臨床試験実施が困難であるため,至適な治療方針は未確立である。進行期の場合は,症状を有する場合,臓器障害(消化管出血など)を認める場合,巨大腫瘤を有する場合,確実に進行を認める場合,患者の希望などが化学療法の適応となる。シクロホスファミド(CPA)などのアルキル化剤単独療法1),フルダラビン(FLU)やクラドリビン(2-CdA)などのプリンアナログ剤単独療法2)3),リツキシマブ(R)単剤4)の有効性が報告されているが,いずれの治療法が優れているかを比較した臨床試験の報告はない。プリンアナログでの二次性造血器腫瘍発症リスクの増加の可能性に注意が必要である5)。アントラサイクリンを含んだ併用療法は,再発例でも有効であったとの報告がある6)。
疾患の頻度が低く大規模な臨床試験が困難であり,十分なエビデンスレベルは得られていないものの,低悪性度B 細胞リンパ腫(FL など)に準じた治療方針が選択されている6)7)。
【参考文献】
1) Hammel P, et al. Efficacy of single-agent chemotherapy in low-grade B-cell mucosa-associated lymphoid tissue lymphoma with prominent gastric expression. J Clin Oncol. 1995 ; 13(10) : 2524-9.(3iiDii)
2) Zinzani PL, et al. Fludarabine-containing chemotherapy as frontline treatment of nongastrointestinal mucosa-associated lymphoid tissue lymphoma. Cancer. 2004 ; 100(10) : 2190-4.(3iiiA)
3) Jäger G, et al. Treatment of extranodal marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue type with cladribine : a phase Ⅱ study. J Clin Oncol. 2002 ; 20(18) : 3872-7.(3iiiDiv)
4) Martinelli G, et al. Clinical activity of rituximab in gastric marginal zone non-Hodgkin’s lymphoma resistant to or not eligible for anti-Helicobacter pylori therapy. J Clin Oncol. 2005 ; 23(9) : 1979-83.(3iiiDiv)
5) Jäger G, et al. Occurrence of a myelodysplastic syndrome (MDS) during first-line 2-chloro-deoxyadenosine(2-CDA) treatment of a low-grade gastrointestinal MALT lymphoma. Case report and review of the literature. Haematologica. 2004 ; 89(4) : ECR01.(3iiiDiv)
6) Raderer M, et al. Activity of rituximab plus cyclophosphamide, doxorubicin/mitoxantrone, vincristine and prednisone in patients with relapsed MALT lymphoma. Oncology. 2006 ; 70(6) : 411-7.(3iiiDiv)
7) Kahl B, et al. Marginal zone lymphomas : management of nodal, splenic, and MALT NHL. Hematology Am Soc Hematol Educ Program. 2008 : 359-64.(レビュー)
| CQ6 | 胃原発以外のMALT リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2B
- 限局期の場合には,放射線治療,外科切除,慎重な経過観察などが推奨される。進行期の場合には,FL に準じて,リツキシマブ±化学療法や慎重な経過観察が推奨される。
【解 説】
疾患の頻度が低く,大規模な臨床試験実施が困難であるため,胃原発以外の節外臓器に発生したMALT リンパ腫の至適治療方針は確立されていない。各患者の病変部位,病期,臨床症状を考慮して治療方針を決定する。治療方法として,放射線療法,外科切除,抗体療法を含めた化学療法などが考慮されるが,どの方法を選択しても,5 年全生存割合(OS)は90%,10 年OS は80%と良好な予後が報告されている1)2)。また,慎重な経過観察も選択肢の一つとなり得る。
限局期の場合には,放射線療法1)~4),外科切除1)2)による局所治療が主体となる。MALT リンパ腫は放射線感受性が高く,35 Gy までの放射線療法で良好なコントロールが可能であり,大部分の眼付属器発症例では25 Gy で,その他の部位でも30 Gy でコントロールされていた3)。日本でもおおむね30 Gy でコントロールされることが確認された5)。診断を兼ねて切除された場合には,残存がなければ経過観察も許容され,残存がある場合には局所放射線治療を考慮する。症状がない場合には慎重な経過観察も選択肢の一つである。しかし,これらの優劣を比較した試験はない。
一方,進行期として診断される患者は,約半数である6)。進行期に対しては,FL の治療方針に準じた方針が推奨される1)。すなわち,リツキシマブ(R)単剤治療,または,R 併用化学療法を考慮する。R 単剤治療の奏効割合は約75%である1)。症状がない場合には慎重な経過観察も選択肢の一つである。
【参考文献】
1) Thieblemont C. Clinical presentation and management of marginal zone lymphomas. Hematology Am Soc Hematol Educ Program. 2005 : 307-13.(レビュー)
2) Zucca E, et al. Nongastric marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue. Blood. 2003 ; 101(7) : 2489-95.(レビュー)
3) Goda JS, et al. Long-term outcome in localized extranodal mucosa-associated lymphoid tissue lymphomas treated with radiotherapy. Cancer. 2010 ; 116(16) : 3815-24.(3iiiA)
4) Fung CY, et al. Mucosa-associated lymphoid tissue lymphoma of the stomach : long term outcome after local treatment. Cancer. 1999 ; 85(1) : 9-17.(3iiiA)
5) Isobe K, et al. A Multicenter Phase Ⅱ Study of Local Radiation Therapy for Stage IEA Mucosa-Associated Lymphoid Tissue Lymphomas : A Preliminary Report From the Japan Radiation Oncology Group(JAROG). Int J Radiation Oncology Biol Physics 2007 ; 69(4) : 1181-6.(3iiA)
6) Thieblemont C, et al. Mucosa-associated lymphoid tissue lymphoma is a disseminated disease in one third of 158 patients analyzed. Blood. 2000 ; 95(3) : 802-6.(3iiiDiii)
| CQ7 | DLBCL との境界病変の場合の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- DLBCL に準じた治療方針が推奨される。
【解 説】
従来,high grade MALT リンパ腫といわれたものが含まれる1)。臨床的経過もびまん性大細胞型B 細胞リンパ腫(DLBCL)と同様と考えられている2)。疾患の頻度が低く大規模な臨床試験が実施困難であり,十分なエビデンスは得られていないものの,大型細胞成分のシート状または充実性増殖を認めるMALT リンパ腫,および大細胞型へ組織学的進展したMALT リンパ腫においては,DLBCL に準じた治療が行われた報告がある3)。
【参考文献】
1) Conconi A, et al. Clinical activity of rituximab in extranodal marginal zone B-cell lymphoma of MALT type. Blood. 2003 ; 102(8) : 2741-5.(3iiDiv)
2) de Jong D, et al. Histological grading with clinical relevance in gastric mucosa-associated lymphoid tissue(MALT) lymphoma. Recent Results Cancer Res. 2000 ; 156 : 27-32.(3iiiDiii)
3) Ghesquières H, et al. Clinicopathologic characteristics and outcome of diffuse large B-cell lymphomas presenting with an associated low-grade component at diagnosis. J Clin Oncol. 2006 ; 24(33) : 5234-41.(3iiDiii)
| CQ8 | 節性辺縁帯リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 節性辺縁帯リンパ腫の治療方針は,FL に代表される低悪性度B 細胞リンパ腫の治療選択が推奨される。
【解 説】
疾患の頻度が低く,節性辺縁帯リンパ腫に限定した大規模な臨床試験の実施が困難であり,十分なエビデンスは得られていない。一般的に,FL に代表される低悪性度B 細胞リンパ腫に準じた治療が推奨される1)2)。
限局期の場合には,注意深い経過観察や放射線療法が考慮される。進行期で症状がなく腫瘍量が少ない場合には,注意深い経過観察やリツキシマブ単剤治療を考慮する。症状がある場合,腫瘍による圧迫や浸潤による臓器障害を認める場合,もしくは腫瘍量が多い場合には,リツキシマブ(R)併用化学療法を考慮する。化学療法の内容としては,R-CVP 療法(R, CPA, VCR, PSL),R-CHOP 療法(R, CPA, DXR, VCR, PSL)が挙げられる。第Ⅱ相試験ではフルダラビン(FLU)などのプリンアナログも使用されている3)が,初発例に対しては本邦では保険適用外である。
【参考文献】
1) Thieblemont C. Clinical presentation and management of marginal zone lymphomas. Hematology Am Soc Hematol Educ Program. 2005 : 307-13.(レビュー)
2) Zucca E, et al. Nongastric marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue. Blood. 2003 ; 101(7) : 2489-95.(レビュー)
3) Brown JR, et al. A phase 2 study of concurrent fludarabine and rituximab for the treatment of marginal zone lymphomas. Br J Haematol. 2009 ; 145(6) : 741-8.(3iiiDiv)
| CQ9 | C 型肝炎ウイルス陽性の場合の脾B 細胞辺縁帯リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 無症状の場合には経過観察を行う。C 型肝炎ウイルス(HCV)陽性で,治療適応があれば,HCV に対する抗ウイルス療法を考慮する。
【解 説】
脾腫や血球減少などのない無症状のC 型肝炎ウイルス(HCV)陽性脾B 細胞辺縁帯リンパ腫では経過観察が行われる。治療を行わなくとも経過には影響しない1)~4)。HCV の治療の適応があれば,HCV の治療を行う。脾腫を認めるHCV 陽性脾B 細胞辺縁帯リンパ腫は,HCV の治療を実施する。HCV 陽性脾B 細胞辺縁帯リンパ腫をインターフェロンα(IFNα)±ribavirine の治療により,HCV-RNA が陰性化した後に,脾B 細胞辺縁帯リンパ腫の奏効が観察された5)。一方,HCV 陰性の患者はIFNαに対する奏効を認めていない。
【参考文献】
1) Berger F, et al. Non-MALT marginal zone B-cell lymphomas : a description of clinical presentation and outcome in 124 patients. Blood. 2000 ; 95(6) : 1950-6.(3iiiDiii)
2) Chacón JI, et al. Splenic marginal zone lymphoma : clinical characteristics and prognostic factors in a series of 60 patients. Blood. 2002 ; 100(5) : 1648-54.(3iiiDiii)
3) Thieblemont C, et al. Treatment of splenic marginal zone B-cell lymphoma : an analysis of 81 patients. Clin Lymphoma. 2002 ; 3(1) : 41-7.(3iiiDiii)
4) Troussard X, et al. Splenic lymphoma with villous lymphocytes : clinical presentation, biology and prognostic factors in a series of 100 patients. Groupe Francais d’Hematologie Cellulaire(GFHC). Br J Haematol. 1996 ; 93(3) : 731-6.(3iiiDiii)
5) Hermine O, et al. Regression of splenic lymphoma with villous lymphocytes after treatment of hepatitis C virus infection. N Engl J Med. 2002 ; 347(2) : 89-94.(3iiiDiv)
| CQ10 | HCV 陰性脾B 細胞辺縁帯リンパ腫の治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 症状を有する脾腫や血球減少などの症状を呈するHCV 陰性脾B 細胞辺縁帯リンパ腫は,脾摘またはリツキシマブ単剤による治療が推奨される。
【解 説】
脾腫や血球減少などのない無症状の脾B 細胞辺縁帯リンパ腫では経過観察が行われる。治療を行わなくとも,経過には影響しない1)~4)。脾腫による圧迫症状や血球減少を認める場合には,治療を考慮する。治療は,脾摘またはリツキシマブ(R)単剤による治療を考慮する。脾摘は,治癒を目指すものではないが,症状と血球減少が軽快する。R は脾B 細胞辺縁帯リンパ腫に有効であり,小規模の第Ⅱ相試験であるが,高い奏効割合が報告されている5)。しかしながら,化学療法やR 併用化学療法と比較した試験はない。
【参考文献】
1) Berger F, et al. Non-MALT marginal zone B-cell lymphomas : a description of clinical presentation and outcome in 124 patients. Blood. 2000 ; 95(6) : 1950-6.(3iiiDiii)
2) Chacón JI, et al. Splenic marginal zone lymphoma : clinical characteristics and prognostic factors in a series of 60 patients. Blood. 2002 ; 100(5) : 1648-54.(3iiiDiii)
3) Thieblemont C, et al. Treatment of splenic marginal zone B-cell lymphoma : an analysis of 81 patients. Clin Lymphoma. 2002 ; 3(1) : 41-7.(3iiiDiii)
4) Troussard X, et al. Splenic lymphoma with villous lymphocytes : clinical presentation, biology and prognostic factors in a series of 100 patients. Groupe Francais d’Hematologie Cellulaire(GFHC). Br J Haematol. 1996 ; 93(3) : 731-6.(3iiiDiii)
5) Kalpadakis C, et al. Rituximab monotherapy is highly effective in splenic marginal zone lymphoma. Hematol Oncol. 2007 ; 25(3) : 127-31.(3iiiDiii)
3
リンパ形質細胞性リンパ腫/ ワルデンストレームマクログロブリン血症
(lymphoplasmacytic lymphoma:LPL/
Waldenström's macroglobulinemia:WM)
(lymphoplasmacytic lymphoma:LPL/
Waldenström's macroglobulinemia:WM)
◆総論1)2)
リンパ形質細胞性リンパ腫(lymphoplasmacytic lymphoma:LPL)は,WHO 分類(2008)によれば,小型B 細胞リンパ球,形質細胞への分化傾向にあるリンパ球,形質細胞が混在したリンパ系腫瘍と定義され,IgM 型M 蛋白の有無は問わない。一方,IgM 型M 蛋白血症を呈するワルデンストレームマクログロブリン血症(Waldenström’s macroglobulinemia:WM)は,骨髄浸潤とIgM 型M 蛋白血症を伴うLPL のサブセットとして定義されている。IgM 型M 蛋白血症を伴うB 細胞リンパ腫はLPL 以外にも認められるため,診断上,注意が必要である。
臨床像としては,IgM 蛋白血症が3g/dL 以上になると,高頻度(10~30%の症例)に過粘稠症候群をきたす。この場合,赤血球凝集に伴って,視力障害(眼底網膜静脈ソーセージ様変化)や脳血管障害を起こし得る。自己免疫疾患の合併や,クリオグロブリン血症,ミエリンに対する抗体活性によるミエリン融解による末梢神経障害,アミロイドーシス,M 蛋白が凝固因子,フィブリン,血小板と結合することによる凝固障害・出血症状を合併することがある。多発性骨髄腫とは異なり,正常免疫グロブリンの抑制は軽度である。
IgM が3 g/dL 未満,骨髄中の腫瘍細胞の割合が10%未満で,かつ,症状のない場合,形質細胞腫瘍に準じて,IgM monoclonal gammopathy of undetermined significance(MGUS)と呼ぶが,形質細胞腫瘍のMGUS に比べて進展が速く,年に1~5%がLPL/WM に進展する。
LPL/WM は,リンパ節,脾臓,肝臓,末梢血へ高頻度に浸潤・出現する。
臨床経過は一般に緩徐であり,生存期間中央値は5 年以上である。死因としては,原病の悪化,悪性度の高いリンパ腫への進展,感染,抗腫瘍療法に起因する二次性白血病などが挙げられる。
予後予測の指標として,international prognostic scoring system for WM(IPSSWM)が報告されている2)3)。「年齢65 歳超」,「ヘモグロビン値11.5 g/dL 以下」,「血小板数10 万/μL 以下」,「β2 ミクログロブリン3μg/mL 以上」,「血清IgM 7,000 mg/dL 以上」が予後不良因子として抽出され,5 年生存割合は,スコア0, 1 が87%,2 で68%,3~5 で36%であった。その他の予後不良因子として,汎血球減少,低アルブミン血症,末梢神経障害などが挙げられている。
治療の効果判定については,International Workshop(2006)の判定規準が用いられている4)5)。
【参考文献】
1) Vijay A, et al. Waldenstrom macroglobulinemia. Blood. 2007 ; 109(12) : 5096-103.(レビュー)
2) Dimopoulos MA, et al. Update on treatment recommendations from the Fourth International Workshop on Waldenstrom’s Macroglobulinemia. J Clin Oncol. 2009 ; 27(1) : 120-6.(レビュー)
3) Morel P, et al. International prognostic scoring system for Waldenstrom macroglobulinemia. Blood. 2009 ; 113(18) : 4163-70.(3iiiA)
4) Kimby E, et al. Update on recommendations for assessing response from the Third International Workshop on Waldenstrom’s Macroglobulinemia. Clin Lymphoma Myeloma. 2006 ; 6(5) : 380-3.(レビュー)
5) Treon SP, et al. Update on treatment recommendations from the Third International Workshop on Waldenstrom’s macroglobulinemia. Blood. 2006 ; 107(9) : 3442-6.(レビュー)
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
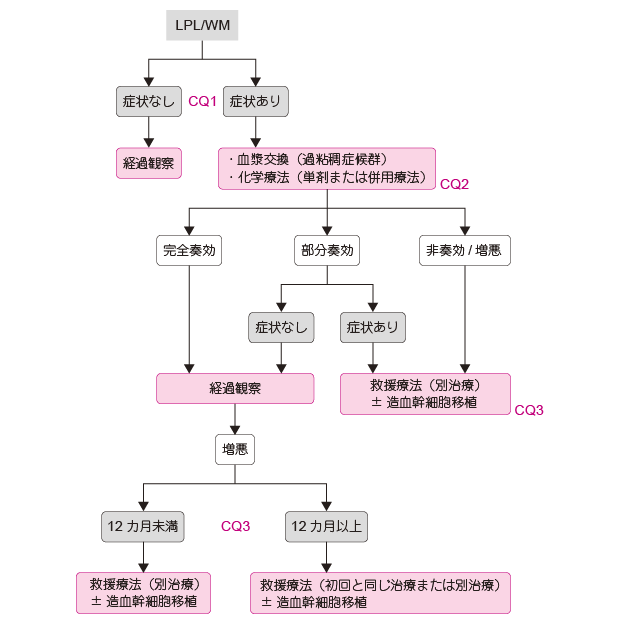
通常の化学療法では治癒は望めない1)~3)。症状のない場合には,未治療で経過観察を行い,症状がある場合には,治療開始を考慮する(CQ1)1)~3)。初回,および,再燃・再発時の化学療法としては,①アルキル化剤を中心とした化学療法,②プリンアナログを中心とした化学療法,③抗体療法(リツキシマブ),④多剤併用化学療法(リツキシマブ併用も含む),⑤ボルテゾミブ(国内未承認),⑥サリドマイド・レナリドミド(国内未承認)が挙げられる(CQ2, CQ3)1)~3)。大量化学療法/造血幹細胞移植は,若年のハイリスク患者や再発・再燃時の治療選択の一つとなり得るが,適応,実施時期,方法については未確立である(CQ3)1)2)。
参考文献
1) Vijay A, et al. Waldenstrom macroglobulinemia. Blood. 2007 ; 109(12) : 5096-103.(レビュー)
2) Dimopoulos MA, et al. Update on treatment recommendations from the Fourth International Workshop on Waldenstrom’s Macroglobulinemia. J Clin Oncol. 2009 ; 27(1) : 120-6.(レビュー)
3) Treon SP. How I treat Waldenstrom macroglobulinemia. Blood. 2009 ; 114(12) : 2375-85.(レビュー)
| CQ1 | 原発性マクログロブリン血症の治療はどの時点で開始するのが適切か |
|---|
-
推奨グレードカテゴリー2A
- 疾患関連の症状,合併症が出現した時点で治療を開始することが推奨される。
【解 説】
原発性マクログロブリン血症の治療は,疾患に関連した症状が認められた時に開始を考慮する1)。具体的な症状としては,持続する発熱,盗汗,体重減少,貧血による倦怠感であり,リンパ節腫大や脾腫の出現やヘモグロビン値<10 g/dL や血小板<10 万/μL も開始を考慮する規準となる。また,過粘稠症候群,末梢神経障害,アミロイドーシス,腎障害,クリオグロブリン血症などの合併症が出現した場合である。また,治療開始はIgM 値のみに基づいて決定されるものではない1)。IgM 値と臨床症状とは関連しない場合があるからである。逆にIgM 値が臨床所見・症状と関連するようであれば参考になり得る。
【参考文献】
1) Kyle RA, et al. Prognostic markers and criteria to initiate therapy in Waldenstrom’s macroglobulinemia : consensus panel recommendations from the Second International Workshop on Waldenstrom’s Macroglobulinemia. Semin Oncol. 2003 ; 30(2) : 116-20.(レビュー)
| CQ2 | 原発性マクログロブリン血症の初回治療として何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 原発性マクログロブリン血症の初回治療としては,過粘稠症候群を認める場合には血漿交換を実施し,化学療法としては,アルキル化薬,プリンアナログ,抗体薬(リツキシマブ)の単剤,または併用での実施が推奨される。
【解 説】
過粘稠症候群を認める場合には,まずは,血漿交換の実施を考慮する。
原発性マクログロブリン血症に対する大規模な比較試験は乏しいが,欧米のエキスパートパネルは以下の薬剤の単剤または併用での使用を推奨している1)。
アルキル化剤: chlorambucil(国内未承認),シクロホスファミド(CPA),メルファラン(MEL)
プリンアナログ:クラドリビン(2-CdA),フルダラビン(FLU)
抗体薬:リツキシマブ(R)
薬剤の併用方法は,プリンアナログ+アルキル化剤,R+プリンアナログ,R+プリンアナログ+アルキル化剤,または,R-CHOP 療法(R, CPA, DXR, VCR, PSL)などが報告されている。併用での有効性は少なくとも単剤と同等の効果が期待できるが,各治療法の優劣を比較した臨床試験や大規模な比較試験はない。
R の使用に際して,過粘稠症候群が悪化することがあるため,過粘稠症候群を認める場合やIgM≧5,000 mg/dL の場合には,治療前に血漿交換が推奨されている2)。
将来的に自家造血幹細胞移植併用大量化学療法が考慮される場合には,造血幹細胞への毒性により自家末梢血幹細胞採取効率への悪影響が懸念されるプリンアナログやchlorambucil の使用は避ける。
ボルテゾミブ(BOR),サリドマイド(THAL),レナリドミド(LEN),ベンダムスチンも有効性が報告され,海外では使用可能だが,本邦ではベンダムスチン以外は保険適用外である。
【参考文献】
1) Dimopoulos MA, et al. Update on treatment recommendations from the Fourth International Workshop on Waldenstrom’s Macroglobulinemia. J Clin Oncol. 2009 ; 27(1) : 120-6.(レビュー)
2) Treon SP, et al. Paradoxical increases in serum IgM and viscosity levels following rituximab in Waldenstrom’s macroglobulinemia. Ann Oncol. 2004 ; 15(10) : 1481-3.(3iiiC)
| CQ3 | 原発性マクログロブリン血症の再燃・再発時の救援治療として何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 初回治療後に再燃・再発した場合の救援療法として,アルキル化薬,プリンアナログ,抗体薬の単剤,または併用,あるいは新規薬剤や大量化学療法/ 造血幹細胞移植の実施が推奨される。
【解 説】
初回治療後に再燃・再発した場合の救援療法は,初回治療に対する反応の程度と奏効期間,忍容性,年齢や合併症など患者の身体状況,大量化学療法/造血幹細胞移植への適応,等を考慮して決定される1)。
初回治療が奏効し,無治療期間が比較的長く続いた場合(12 カ月以上)には,初回治療の再実施を考慮する。奏効期間が短い場合や抵抗性の場合は,初回治療とは異なるカテゴリーの単剤または併用治療が推奨される1)。
単剤による救援療法としては,アルキル化剤[chlorambucil(国内未承認)2)],プリンアナログ[クラドリビン(2-CdA)3),フルダラビン(FLU)4)],抗体薬[リツキシマブ(R)5),alemtuzumab(国内未承認)1)]が報告されており,併用療法として,プリンアナログ+アルキル化剤6),R+プリンアナログ,R +プリンアナログ+アルキル化剤,または,R-CHOP 療法(R, CPA, DXR, VCR,PSL)などが報告されている1)。近年では,ボルテゾミブ(BOR)7)8),サリドマイド(THAL),レナリドミド(LEN),ベンダムスチンの有効性が報告されているが1),本邦ではベンダムスチン以外は保険適用外である。各治療法の優劣を比較した臨床試験や大規模な比較試験はない。
若年者に対して,自家造血幹細胞移植併用大量化学療法や同種造血幹細胞移植の有効性を示す報告もあるが9)10),適応や有効性に関するエビデンスに乏しく,適応,実施時期,方法については未確立である。したがって,臨床試験として実施するのが望ましい。自家末梢血幹細胞移植併用大量化学療法が考慮される場合には,プリンアナログやchlorambucil の使用は避ける1)。
【参考文献】
1) Dimopoulos MA, et al. Update on treatment recommendations from the Fourth International Workshop on Waldenstrom’s Macroglobulinemia. J Clin Oncol. 2009 ; 27(1) : 120-6.(レビュー)
2) Kyle RA, et al. Waldenstrom’s macroglobulinaemia : a prospective study comparing daily with intermittent oral chlorambucil. Br J Haematol. 2000 ; 108(4) : 737-42.(1iiDiv)
3) Weber DM, et al. 2-Chlorodeoxyadenosine alone and in combination for previously untreated Waldenstrom’s macroglobulinemia. Semin Oncol. 2003 ; 30(2) : 243-7.(3iiiDiv)
4) Dhodapkar MV, et al. Prognostic factors and response to fludarabine therapy in Waldenstrom’s macroglobulinemia an update of a US intergroup trial (SWOG S9003). Semin Oncol. 2003 ; 30 (2) : 220-5.(3iiA)
5) Gertz MA, et al. Multicenter phase 2 trial of rituximab for Waldenstrom macroglobulinemia (WM) : an Eastern Cooperative Oncology Group Study (E3A98). Leuk Lymphoma. 2004 ; 45 (10) : 2047-55.(3iiiDiv)
6) Leblond V, et al. Multicenter, randomized comparative trial of fludarabine and the combination of cyclophosphamide-doxorubicin-prednisone in 92 patients with Waldenstrom macroglobulinemia in first relapse or with primary refractory disease. Blood. 2001 ; 98(9) : 2640-4.(1iiDiv)
7) Chen CI, et al. Bortezomib is active in patients with untreated or relapsed Waldenstrom’s macroglobulinemia : a phase Ⅱ study of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 2007 ; 25(12) : 1570-5.(3iiDiv)
8) Treon SP, et al. Multicenter clinical trial of bortezomib in relapsed/refractory Waldenstrom’s macroglobulinemia : results of WMCTG Trial 03-248. Clin Cancer Res. 2007 ; 13(11) : 3320-5.(3iiDiv)
9) Kyriakou C, et al. High-dose therapy and autologous stem-cell transplantation in Waldenstrom macroglobulinemia : the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol. 2010 ; 28(13) : 2227-32.(3iiiA)
10) Kyriakou C, et al. Allogeneic stem-cell transplantation in patients with Waldenstrom macroglobulinemia : report from the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol. 2010 ; 28(33) : 4926-34.(3iiiA)
4
マントル細胞リンパ腫
(Mantle cell lymphoma:MCL)
(Mantle cell lymphoma:MCL)
◆総論
リンパ節濾胞のマントル層(暗殻)を構成するB 細胞と同じ細胞表面形質を有する腫瘍である。免疫組織学的には CD5 と cyclin D1 が陽性で,分子遺伝学的には染色体転座t (11;14)(q13;q32) に伴うBCL-1 遺伝子再構成を有する独立した疾患単位である1)。わが国での発症頻度は,全悪性リンパ腫の3%程度である2)。発症年齢中央値は60 歳代半ばで男性に多い1)。約9 割の症例が初発時に病期Ⅲ,Ⅳの進行期で,表在リンパ節腫大以外に70%程度の症例は節外病変を有し,骨髄浸潤は半数以上,脾腫は30%以上,消化管浸潤は20~30%に認められる。免疫組織化学染色ではcyclin D1 陰性例が15%程度存在し,これらはcyclin D1 陽性例に比し予後良好と報告されている3)。
MCL の病期分類には,他の非ホジキンリンパ腫と同様にAnn Arbor 分類が用いられる。予後予測モデルとして,国際予後指標(International Prognostic Index:IPI)とは別に,年齢,Performance status,血清LDH,末梢血白血球数の4 因子について配点を規定し,総点数により予後をlow,intermediate,high の3 群に層別するMCL International Prognostic Index(MIPI)が提唱され,IPI より予後予測能が高いことが示されている4)。さらに,Ki-67 染色陽性率はMIPI とは独立した予後因子であることも示され,Ki-67 陽性率を加えた新たな層別因子も提唱されている4)5)。これらは現時点では一般臨床にはあまり用いられていないが,今後普及する可能性がある。
【参考文献】
1) Swerdlow SH, et al. Mantle cell lymphoma. Swerdlow SH, et al. eds. WHO Classification of Tumors of Hematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008 : pp229-32.
2) Lymphoma Study Group of Japanese Pathologist. The World Health Organization classification of malignant lymphomas in Japan : Incidence of recently recognized entities. Pathol Int. 2000 ; 50(9) : 696-702.
3) Yatabe Y, et al. Significance of cyclin D1 overexpression for the diagnosis of mantle cell lymphoma : a clinicopathologic comparison of cyclin D1-positive MCL and cyclin D1-negative MCL-like B-cell lymphoma. Blood. 2000 ; 95(7) : 2253-61.(3iiiA)
4) Hoster E, et al. A new prognostic index(MIPI) for patients with advanced-stage mantle cell lymphoma. Blood. 2008 ; 111(2) : 558-65.
5) Gressin R, et al. Evaluation of the(R) VAD+C regimen for the treatment of newly diagnosed mantle cell lymphoma. Combined results of two prospective phase Ⅱ trials from the French GOELAMS group. Haematologica 2010 ; 95(8) : 1350-57.(3iiiDiv)
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
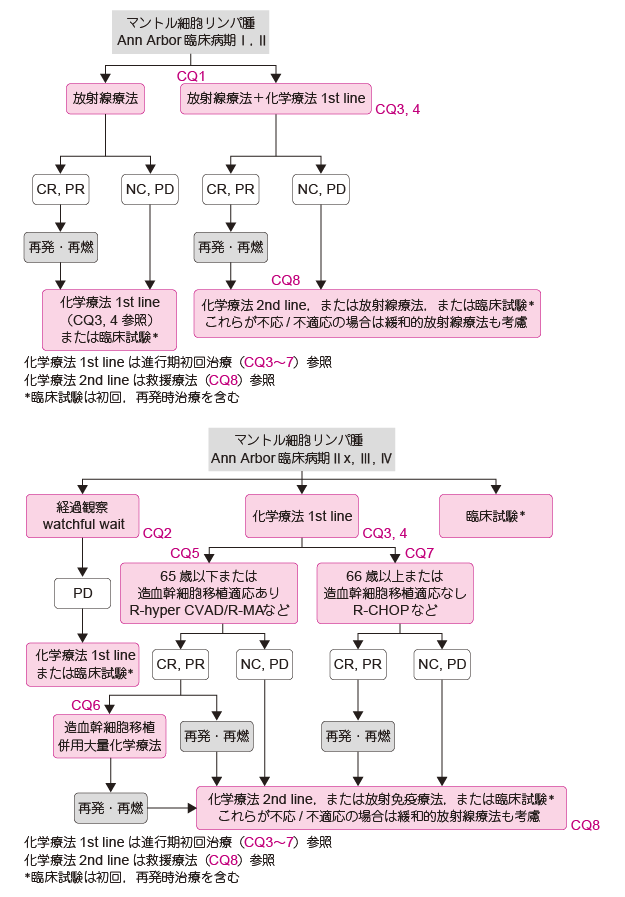
MCL は標準治療が確立しておらず,現在も精力的に臨床試験が進められている。本項では日常診療として実施可能な治療を基にアルゴリズムを作成した。
限局期ではinvolved-field radiotherapy(IFRT*)±化学療法群と,化学療法単独または経過観察群との治療成績の比較から,IFRT 単独もしくはIFRT と化学療法との併用が推奨される(CQ1)。進行期の治療の原則は多剤併用化学療法と抗CD20 キメラ抗体[リツキシマブ(R)]との併用療法である。限られた症例ではあるが,極めてindolent な臨床経過を示す群がある。これらはindolent MCL として,濾胞性リンパ腫などの低悪性度B 細胞リンパ腫と同様に無治療で経過観察することが可能であるが,診断時にこのような症例を見出す方法は確立していない(CQ2)。進行期MCL に対しアグレッシブ リンパ腫の標準的化学療法であるCHOP 療法(CPA, DXR, VCR,PSL)またはその類似療法単独の長期治療成績は不良である。これらにR を併用することで完全奏効(CR)割合は改善し良好な分子生物学的奏効も得られるが,長期無増悪生存割合の改善は十分ではない(CQ3,CQ4)。このため,65 歳以下の症例にはR と高用量シタラビンなどを組み込んだ強化型化学療法を実施し,奏効例には可能であれば引き続き地固め療法として自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation : HDC/AHSCT)を行うことが推奨される(CQ5,CQ6)。一方,66 歳以上あるいは強化型化学療法の実施が困難な場合は,R とCHOP 療法などとの併用が推奨される(CQ7)。初回治療には臨床病態,病理組織学所見などを詳細に検討し,患者個々に最も有用性が高いと考えられる治療法を選択する必要がある。再発/初回治療抵抗例には新規抗腫瘍薬の導入により良好な治療成績も報告され(CQ8),これら新規治療薬を用いた臨床試験も展開されている。標準治療が確立していないMCL では,臨床試験への登録が望ましい。これら救援療法が不応/不適応の場合は,緩和的なIFRT の適用も考慮される(CQ8)。
*リンパ腫病変が確認されたリンパ節の所属リンパ節領域および,リンパ腫病変が確認された節外病変に一定のマージンを設定した部位に対して行われる放射線療法。
| CQ1 | 限局期MCL の初回治療として推奨される治療法は何か |
|---|
-
推奨グレードカテゴリー2A
- 化学療法単独での治療効果は不良で,一方,放射線療法の感受性が高いことから,限局期の初回治療としてIFRT 単独(30~36 Gy),またはIFRT と化学療法との併用が推奨される。
【解 説】
巨大腫瘤のない初発ⅠA, ⅡA 期のMCL において,IFRT±化学療法(アルキル化剤単独またはCHOP 療法など)群と,化学療法単独または経過観察群を比較検討した比較的少数例の後方視的解析の結果,無増悪生存割合(PFS)には年齢とIFRT 実施の有無が有意な予後因子であった。5 年PFS は,60 歳以上に比べ60 歳未満は有意に優れていた。同様にIFRT 実施群のPFS はIFRT 未実施群に比べ有意に優れる結果であり,照射野内での再発は認めていない。一方,5 年全生存割合(OS)には,IFRT 実施群と非実施群との間に有意差はなかった1)。また初発限局期例および再発・治療抵抗例の後方視的解析でも,IFRT は15~20 Gy の比較的低線量で完全奏効(CR)割合64%を含む100%の局所奏効割合と,無増悪生存期間中央値10 カ月の良好な局所コントロールが報告されている2)。MCL は化学療法単独での治療成績が不良であることから,初発限局期の治療としてIFRT 単独(30~36 Gy),またはIFRT と多剤併用化学療法との併用が推奨される。
【参考文献】
1) Leitch HA, et al. Limited-stage mantle-cell lymphoma. Ann Oncol. 2003 ; 14(10) : 1555-61.(3iiiDiii)
2) Rosenbluth BD, Yahalom J. Highly effective local control and palliation of mantle cell lymphoma with involved-field radiation therapy(IFRT). Int J Radiat Oncol Biol Phys. 2006 ; 65(4) : 1185-91.(3iiDiv)
| CQ2 | MCL の初回治療として無治療経過観察は適切か |
|---|
-
推奨グレードカテゴリー2B
- MCL の一部はindolent な臨床経過を呈する。このような症例を診断時に同定するのは困難であるが,特に高齢でindolent な臨床経過を呈する症例には,無治療経過観察も考慮すべき治療として推奨される。
【解 説】
MCL の一部はindolent な臨床経過を呈することが知られている。臨床情報が明らかな97 例の後方視的解析では,31 例は無治療経過観察が可能であった。その期間は6 カ月以上が71%,1 年以上が14%,5 年以上は10%で,この群の全生存期間は診断早期よりCHOP 療法を開始した群より良好であった1)。この研究ではindolent な経過を呈する群を診断時に抽出する有意なマーカーは検出されていないが,免疫グロブリン重鎖可変領域遺伝子の再構成頻度の解析から,通常のMCL とは異なるsubtype であるとの報告がある2)。病理組織学的にはマントル層型,免疫染色Ki-67 の陽性率(MIB1 index)低値の例は予後良好である。臨床的には限局期のほか,節外病変主体・脾腫・白血化など脾辺縁帯リンパ腫類似病態を呈する例は一般にindolent な経過を呈し,比較的長期間の無治療経過観察が可能である3)。またindolent MCL はSOX11 の発現強度が低く4),染色体異常も極めて単純2)との報告がある。特に高齢でindolent な臨床経過を呈する症例は無治療経過観察の適応と考えられるが,indolent MCL を診断時に正しく鑑別する方法は確立しておらず,適用には慎重な配慮が必要である5)。
【参考文献】
1) Martin P, et al. Outcome of differed initial therapy in mantle-cell lymphoma. J Clin Oncol. 2009 ; 27(8) : 1209-13.(3iiiA)
2) Navarro A. et al. Molecular pathogenesis of mantle cell lymphoma : new perspectives and challenges with clinical implications. Semin Hematol. 2011 ; 48(3) : 155-65.(レビュー)
3) Kimura Y, et al. Small cell variant of mantle cell lymphoma is an indolent lymphoma characterized by bone marrow involvement, splenomegaly, and a low Ki-67 index. Cancer Sci. 2011 ; 102(9) : 1734-41.(3iiiA)
4) Wang X, et al. The subcellular Sox11 distribution pattern identifies subsets of mantle cell lymphoma : correlation to overall survival. Br J haematol. 2008 ; 143(2) : 248-53.(3iiiA)
5) Martin P, et al. Is there a role of“ watch and wait” in patients with mantle cell lymphoma. Semin Hematol. 2011 ; 48(3) : 189-93.(レビュー)
| CQ3 | 初発進行期MCL の治療としてリツキシマブ単独療法は有用か |
|---|
-
推奨グレードカテゴリー3
- 少なくとも初回治療としてリツキシマブ単独療法は適切ではなく,化学療法の実施が困難と考えられる例を除けば推奨されない。
【解 説】
欧州の低悪性度B 細胞リンパ腫に対するリツキシマブ(R)(375 mg/m2,週1 回4 週連続投与)単独療法の第Ⅱ相試験では,初発MCL の完全奏効(CR)割合は14%,部分奏効(PR)割合は37%であり,一方,既治療MCL のCR 割合は16%,PR 割合は38%で,R 単独療法はアルキル化剤単独療法に比べCR 割合,全奏効割合とも改善していない1)。治療成功生存期間(FFS)中央値は1.2 年で,未治療例と既治療例,CR 例とPR 例との間に有意な差を認めていない1)。また,R を標準的(週1 回4 週連続)に投与後,8 週間隔で3 回(各4 週連続)追加しても,全奏効割合,FFS,無イベント生存期間(EFS)のいずれにも改善は得られていない2)。初発例と既治療例との間でFFS 期間に差がないことは,R は化学療法とは異なる作用機序で効果を発現していると考えられるが,R 単独療法では十分な治療効果は期待できず,初発例の治療として適切ではない。多剤併用化学療法が困難な症例を除けば推奨されない。
【参考文献】
1) Foran JM, et al. European phase Ⅱ study of Rituximab (chimeric anti-CD20 monoclonal antibody) for patients with newly diagnosed mantle-cell lymphoma and previously treated mantle-cell lymphoma, immunocytoma, and small B-cell lymphocytic lymphoma. J Clin Oncol 2000 ; 18(2) : 317-24.(3iiiDiv)
2) Ghielmini, M, et al. Effect of single-agent rituximab given at the standard schedule or prolonged treatment in patients with mantle cell lymphoma : A study of the Swiss Group for Clinical Cancer Research(SAKK). J Clin Oncol. 2005 ; 23(4) : 705-11.(3iiDi)
| CQ4 | 初発進行期MCL の化学療法にはリツキシマブを併用すべきか |
|---|
-
推奨グレードカテゴリー1
- 初発進行期MCL の治療として,化学療法とリツキシマブとの併用は治療効果を増強するので,リツキシマブを併用することが推奨される。
【解 説】
初発,Ⅱ~Ⅳ期(80%は骨髄浸潤あり)を対象としたR-CHOP 療法(R, CPA, DXR, VCR, PSL)の第Ⅱ相試験1)では,完全奏効(CR,CRu)割合は48%,全奏効割合は96%で,48%には分子生物学的奏効が得られた。しかし,分子生物学的奏効例の無増悪生存期間(PFS)中央値は16.6 カ月で改善が得られていない。R 併用化学療法は末梢血や骨髄の腫瘍細胞を消失させ,良好な分子生物学的効果が得られるが一過性にとどまる。また,R-CHOP 療法とCHOP 療法の第Ⅲ相試験においても,全奏効割合,CR 割合,治療成功生存期間(FFS)は前者が有意に優れたが,全生存割合(OS)には有意な差は得られていない2)。一方,メタアナリシスではR は化学療法との併用で奏効割合,OS を改善することが示されている3)4)。高齢者(66 歳以上)を対象としたメタアナリシスでも,生存期間と2 年生存割合に関わる多変量解析の結果,R と化学療法との併用が最も強い予後良好因子であった5)。初発MCL では化学療法とR との併用は初期治療効果を有意に改善することから,両者の併用は強く推奨される。
【参考文献】
1) Howard OM, et al. Rituximab and CHOP induction therapy for newly diagnosed mantle-cell lymphoma : Molecular complete responses are not predictive of progression-free survival. J Clin Oncol. 2002 ; 20(5) : 1288-94.(3iiiDiv)
2) Lenz G, et al. Immunochemotherapy with rituximab and cyclophosphamide, doxorubicin, vincristine, and prednisone significantly improves response and time to treatment failure, but not long-term outcome in patients with previously untreated mantle cell lymphoma : results of a prospective randomized trial of the German Low Grade Lymphoma Study Group(GLSG). J Clin Oncol. 2005 ; 23(9) : 1984-92.(1iiDiv)
3) Tam CS, et al. Mature results of the M.D. Anderson Cancer Center risk-adapted transplantation strategy in mantle-cell lymphoma. Blood. 2009 ; 113(18) : 4144-52.(3iiiA)
4) Schulz H, et al. Immunochemotherapy with rituximab and overall survival in patients with indolent or mantle cell lymphoma : a systematic review and meta-analysis. J Natl Cancer Inst. 2007 ; 99(9) : 706-14.(1iiA)
5) Griffi ths R, et al. Addition of rituximab to chemotherapy alone as first-line therapy improves over-all survival in elderly patients with mantle cell lymphoma. Blood. 2011 ; 118(18) : 4808-16.(3iA)
| CQ5 | 65 歳以下の初発進行期MCL に推奨される化学療法は何か |
|---|
-
推奨グレードカテゴリー2A
- 初発進行期MCL に対するR-CHOP 療法は,奏効割合を改善したが奏効期間は短く,長期の治療成績は改善していない。一方,治療強度(dose intensity)を高めた強化型化学療法では長期治療成績の改善が得られており,これらの実施が可能な65 歳以下の比較的若年者には強化型化学療法が推奨される。
【解 説】
初発進行期MCL のCHOP 療法(CPA, DXR, VCR, PSL)の成績は完全奏効(CR)割合30%未満,10 年生存割合は8%1)で,R-CHOP 療法でも長期治療成績は必ずしも改善していない2)3)。MD アンダーソンがんセンターでは,治療強度を高めたhyper-CVAD/MA 療法(CPA, VCR,DXR, DEX/高用量MTX,高用量AraC)の奏効例に同種骨髄移植を追加することで優れた治療成績を得たが,適応は限られていた4)。その後リツキシマブ(R)を併用したR-hyper-CVAD/MA 療法では,造血幹細胞移植なしで3 年無増悪生存割合(PFS)64%と良好な成績を得ているが,無増悪生存曲線は平坦化しておらず,66 歳以上では有害事象の頻度が高いことが報告された5)。また,Nordic Lymphoma Group の65 歳以下を対象としたR と高用量シタラビン(AraC)導入前後の自家造血幹細胞移植併用大量化学療法に関する第Ⅱ相試験(Nordic regimen:R,治療強度増強CHOP/R,高用量AraC)では,R 導入後は6 年生存割合,無イベント生存割合(EFS),PFS,分子生物学的奏効生存期間が有意に改善した6)。強化型化学療法はR-CHOP 療法より良好な治療成績が得られ,65 歳以下の初発進行期症例には可能であればR と高用量シタラビンを併用した強化型化学療法が推奨される。なお,これらは引き続き自家造血幹細胞移植併用大量化学療法を実施することを前提としていることに留意する必要がある(CQ6)。
【参考文献】
1) Fisher, RI et al. A clinical analysis of two indolent lymphoma entities : mantle cell lymphoma and marginal zone lymphoma(including the mucosa-associated lymphoid tissue and monocytoid B-cell lymphoma) : a Southwest Oncology Group study. Blood. 1995 ; 85(4) : 1075-82.(3iiiA)
2) Howard, OM. et al. Rituximab and CHOP induction therapy for newly diagnosed mantle-cell lymphoma : Molecular complete responses are not predictive of progression-free survival. J Clin Oncol. 2002 ; 20(5) : 1288-94.(3iiiDiv)
3) Lenz G, et al. Immunochemotherapy with rituximab and cyclophosphamide, doxorubicin, vincristine, and prednisone significantly improves response and time to treatment failure, but not long-term outcome in patients with previously untreated mantle cell lymphoma : results of a prospective randomized trial of the German Low Grade Lymphoma Study Group(GLSG). J Clin Oncol. 2005 ; 23(9) : 1984-92.(1iiDiv)
4) Khouri IF, et al. Hyper-CVAD and high dose methotrexate/cytarabine followed by stem-cell transplantation : an active regimen for aggressive mantle-cell lymphoma. J Clin Oncol. 1998 ; 16(12) : 3803-09.(3iiiDi)
5) Romaguera JE, et al. High rate of durable remissions after treatment of newly diagnosed aggressive mantle-cell lymphoma with rituximab plus hyper-CVAD alternating with rituximab pulse high-dose methotrexate and cytarabine. J Clin Oncol. 2005 ; 23(28) : 7013-23.(3iiDiv)
6) Geisler CH, et al. Long-term progression-free survival of mantle-cell lymphoma after intensive front-line immunochemotherapy with in vivo-purged stem cell rescue : a nonrandomized phase 2 multicenter study by Nordic Lymphoma Group. Blood 2008 ; 112(7) : 2687-93.(3iiiDi)
| CQ6 | 初回治療が奏効した比較的若年者のMCL には地固め 療法として自家造血幹細胞移植併用大量化学療法を実 施すべきか |
|---|
-
推奨グレードカテゴリー2A
- 初回治療奏効後の自家造血幹細胞移植併用大量化学療法は無増悪生存期間を延長するので,地固め療法として実施することが推奨される。
【解 説】
リツキシマブ(R)導入以前のMDACC での第Ⅱ相試験[hyper-CVAD/MA 療法(CPA, VCR,DXR, DEX,高用量MTX,高用量AraC)奏効例に対し55 歳以下は同種造血幹細胞移植,56~65 歳は自家造血幹細胞移植を実施]では,hyper-CVAD 療法はCHOP 療法(CPA, DXR, VCR,PSL)に比べ無イベント生存割合(EFS),全生存割合(OS)が有意に優れていた1)。また,European MCL Network での治療奏効後の造血幹細胞移植とインターフェロンα維持療法との第Ⅲ相試験では,無増悪生存期間中央値は造血幹細胞移植群で有意に延長した(3 年生存割合は有意差なし)2)。MDACC のR-hyper-CVAD/MA 療法では無増悪生存曲線は平坦化しないが3),Nordic Lymphoma Group の自家造血幹細胞移植を用いた2 つの第Ⅱ相試験の比較では,R 導入後は6 年OS,EFS,無増悪生存割合(PFS),分子生物学的奏効生存期間が有意に優れていた4)。MCL は高率に骨髄,末梢血に浸潤を認めるが,R と高用量シタラビン(AraC)との併用で高いpurging 効果が得られ5),腫瘍細胞の混入が少ない造血幹細胞の採取が可能である。MDACC の解析では,high-dose chemotherapy with autologous hematopoietic stem cell transplantation(HDC/ AHSCT)によりPFS が改善し,無増悪生存曲線が平坦化するのは第一奏効期での実施に限られており6),65 歳以下の初発進行期で治療奏効が得られた例にはHDC/AHSCT を実施することが推奨される。
【参考文献】
1) Khouri, IF et al. Hyper-CVAD and high dose methotrexate/cytarabine followed by stem-cell transplantation : an active regimen for aggressive mantle-cell lymphoma. J Clin Oncol. 1998 ; 16(12) : 3803-09.(3iiiDi)
2) Dreylihg M, et al. Early consolidation by myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission significantly prolongs progression-free survival in mantle-cell lymphoma : results of a prospective randomized trial of the European MCL Network. Blood. 2005 ; 105(7) : 2677-84.(1iDiii)
3) Romaguera JE, et al. High rate of durable remissions after treatment of newly diagnosed aggressive mantle-cell lymphoma with rituximab plus hyper-CVAD alternating with rituximab pulse high-dose methotrexate and cytarabine. J Clin Oncol. 2005 ; 23(28) : 7013-23.(3iiDiv)
4) Geisler CH, et al. Long-term progression-free survival of mantle-cell lymphoma after intensive front-line immunochemotherapy with in vivo-purged stem cell rescue : a nonrandomized phase 2 multicenter study by Nordic Lymphoma Group. Blood 2008 ; 112(7) : 2687-93.(3iiiDi)
5) Magni M, et al. Successful in vivo purging of CD34-containing peripheral blood harvests in mantle cell and indolent lymphoma ; evidence for a role of both chemotherapy and rituximab infusion. Blood. 2000 ; 96(3) : 864-69.(3iiiDiv)
6) Tam CS, et al. Mature results of the M.D. Anderson Cancer Center risk-adapted transplantation strategy in mantle-cell lymphoma. Blood. 2009 ; 113(18) : 4144-52.(3iiiA)
| CQ7 | 66 歳以上あるいは65 歳以下でも強力な化学療法の 適応とならない初発進行期MCL に対する標準治療は 何か |
|---|
-
推奨グレードカテゴリー2A
- 自家造血幹細胞移植併用大量化学療法を含む強力な化学療法の適応がない場合は,R-CHOP 療法またはその類似療法が推奨される。
【解 説】
初発進行期MCL のCHOP 療法(CPA, DXR, VCR, PSL)の成績は不良である1)。CHOP 療法とCOP 療法(CPA, VCR, PSL)との比較試験では,完全奏効(complete response:CR)割合,全奏効割合,生存期間中央値,無再発生存期間中央値には有意差はない2)3)が,ドキソルビシン(DXR)を含む治療は有意にCR 割合が高く,IPI のLow およびLow-Intermediate risk 群に限れば全生存割合(OS),無病生存割合(DFS)は有意に優れるとの報告4)もあり,DXR は予後良好群には有用と考えられる。CHOP 療法およびその類似療法はリツキシマブ(R)併用により分子生物学的奏効割合,全奏効割合は改善する5)6)が,長期の無増悪生存割合(PFS)やOS の改善は十分ではない。しかし,66 歳以上に対するR-hyper-CVAD/MA 療法(R, CPA, VCR, DXR, DEX)は有害事象が高頻度で奏効期間も短く,推奨されないと結論されている7)。R-CHOP 療法(R,CPA, DXR, VCR, PSL)は初期治療効果に優れ,高齢者(66 歳以上)初発例でのR-FC 療法(R,FLU, CPA)との第Ⅲ相試験でもOS が有意に優れた8)ことから,治療強度を高めた化学療法の適応がない場合はR-CHOP 療法またはその類似療法が推奨される。
【参考文献】
1) Fisher, RI et al. A clinical analysis of two indolent lymphoma entities : mantle cell lymphoma and marginal zone lymphoma(including the mucosa-associated lymphoid tissue and monocytoid B-cell lymphoma) : a Southwest Oncology Group study. Blood. 1995 ; 85(4) : 1075-82.(3iiiA)
2) Meusers P, et al. Multicenter randomized therapeutic trial for advanced centrocytic lymphoma : Anthracycline dose not improve the prognosis. Hematol Oncol. 1989 ; 7(5) : 365-80.(3iiiDiv)
3) Weisenburger DD, et al. Mantle cell lymphoma. A clinicopathologic study of 68 cases from Nebraska Lymphoma Study Group. Am J Hematol. 2000 ; 64(3) : 190-6.(3iiiA)
4) Zucca E, et al. Patterns of survival in mantle cell lymphoma. Ann Oncol. 1995 ; 6(3) : 257-62.(3iiiA)
5) Howard, OM. et al. Rituximab and CHOP induction therapy for newly diagnosed mantle-cell lymphoma : Molecular complete responses are not predictive of progression-free survival. J Clin Oncol. 2002 ; 20(5) : 1288-94.(3iiiDiv)
6) Lenz G, et al. Immunochemotherapy with rituximab and cyclophosphamide, doxorubicin, vincristine, and prednisone significantly improves response and time to treatment failure, but not long-term outcome in patients with previously untreated mantle cell lymphoma : results of a prospective randomized trial of the German Low Grade Lymphoma Study Group(GLSG). J Clin Oncol. 2005 ; 23(9) : 1984-92.(1iiDiv)
7) Romaguera JE, et al. High rate of durable remissions after treatment of newly diagnosed aggressive mantle-cell lymphoma with rituximab plus hyper-CVAD alternating with rituximab pulse high-dose methotrexate and cytarabine. J Clin Oncol. 2005 ; 23(28) : 7013-23.(3iiDiv)
8) Kluin-Nelemans HC, et al. Treatment of older patients with mantle-cell lymphoma. N Engl J Med. 2012 ; 367(6) : 520-31.(1iiDiv)
| CQ8 | 再発・治療抵抗MCL に推奨される治療は何か |
|---|
-
推奨グレードカテゴリー2B
- 再発・治療抵抗性MCL に対し下記の治療法は高い奏効割合が報告されており,いずれも救援療法として推奨される。
- フルダラビン,クラドリビン,ベンダムスチンの各単剤療法
- 上記薬剤とリツキシマブまたは他の抗腫瘍薬との併用療
- 放射免疫療法薬(90Y イブリツモマブチウキセタン)単剤療法
【解 説】
再発・治療抵抗低悪性度B 細胞リンパ腫に対するR-FCM 療法(R, FLU, CPA, MIT)とFCM 療法とのランダム化比較試験では,50%生存期間はR-FCM 療法が有意に優れたが,全奏効割合と50%無増悪生存期間(PFS)には有意差がない1)。両療法の奏効例を対象としたリツキシマブ(R)維持療法(4 週連続投与を3 カ月後,9 カ月後に実施)は,治療奏効持続期間を有意に延長した2)。同様にクラドリビン(2-CdA)3),ベンダムスチン4)5)も特にR との併用で高い奏効割合と比較的良好なPFS が得られている。90Y イブリツモマブチウキセタンも奏効割合を改善する。PFS は比較的短いが6)7),救援療法奏効例では地固め療法としてPFS の延長が期待される7)8)。これらの治療はいずれも再発・初回治療抵抗例の治療として推奨される。これらの救援療法が不応あるいは非適応の場合,IFRT の後方視的解析では比較的低線量で良好な局所コントロールが得られるとの報告があり9),IFRT の適用も考慮される。
【参考文献】
1) Forstpointner R, et al. The addition of rituximab to a combination of frudarabine, cyclophosphamide, mitoxantrone(FCM) significantly increases the response rate and prolongs survival as compared with FCM alone in patients with relapsed and refractory follicular and mantle cell lymphomas : results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood. 2004 ; 104(10) : 3064-71.(1iiDiv/1iiA)
2) Forstpointner R, et al. Maintenance therapy with rituximab leads to a significant prolongation of response duration after salvage therapy with a combination of rituximab, fludarabine, cyclophosphamide, and mitoxantrone(R-FCM) in patients with recurring and refractory follicular lymphoma and mantle cell lymphoma : Results of a prospective randomized study of the German Low Grade Lymphoma Study Group(GLSG). Blood. 2006 ; 108(13) : 4003-8.(1iiDiii)
3) Inwards DJ, et al. Long-term results of the treatment of patients with mantle cell lymphoma with cladribine(2-CDA) alone(95-80-53) or 2-CDA and rituximab(N0189) in the North Central Cancer Treatment Group. Cancer 2008 ; 113(1) : 108-16.(3iiiDiv)
4) Rummel MJ, et al. Bendamustine plus rituximab is effective and has a favorable toxicity profile in the treatment of mantle cell and low-grade non-Hodgkin’s lymphoma. J Clin Oncol. 2005 ; 23(15) : 3383-89.(3iiiDiii)
5) Robinson KS, et al. Phase II multicenter study of bendamusutine plus rituximab in patients with relapsed indolent B-cell and mantle cell non-Hodgkin’s lymphoma. J Clin Oncol. 2008 ; 26(27) : 4473-39.(3iiiDiv)
6) Wang M, et al. Phase-II study of Yttrium 90(90Y) ibritumomab tiuxetan in patients with relapsed or refractory mantle cell lymphoma. J Clin Oncol. 2009 ; 27(31) : 5213-18.(3iiiDiv)
7) Weigert O, et al. Efficacy of radioimmunotherapy with(90Y) ibritumomab tiuxetan is superior as consolidation in relapsed or refractory mantle cell lymphoma : Results of two phase Ⅱ trial of European MCL Network and PLRG. J Clin Oncol. 2006 ; 24 : 7533a.(3iiiDiv)
8) Jurczak W, et al. 90Y-ZevalinR(90Y ibritumomab tiuxetan) radioimmunotherapy(RIT) consolidation for FCM induction chemotherapy in mantle cell lymphoma(MCL) patient : Result from the PLRG upon completed enrollment. Blood. 2006 ; 108 : 2747a.(3iiiDiv)
9) Rosenbluth BD, Yahalom J. Highly effective local control and palliation of mantle cell lymphoma with involved-field radiation therapy(IFRT). Int J Radiation Oncology Biol Phys. 2008 ; 65(4) : 1185-91.(3iiDiv)
5
びまん性大細胞型B 細胞リンパ腫
(diffuse large B-cell lymphoma, not otherwise specified:DLBCL,NOS)
(diffuse large B-cell lymphoma, not otherwise specified:DLBCL,NOS)
◆総論
WHO 分類(2008)1)におけるびまん性大細胞型B 細胞リンパ腫(Diffuse large B-cell lymphoma,not otherwise specified:DLBCL,NOS)は,本邦の全NHL のうち3 割強を占める2),もっとも発生頻度の高い病型である。DLBCL としての初発例の他に,他の低悪性度B 細胞リンパ腫から組織学的進展する例もあり,さまざまな病態を示す不均一な疾患群である。形態学的,分子学的,免疫組織学的に種々のバリアントもしくはサブグループに分類されるが,現在のところそれらによる治療の層別化は,一般的に行われていない。
本項では,DLBCL,NOS に加え,DLBCL の亜型(subtype)のうちT 細胞/組織球豊富型大細胞型B 細胞リンパ腫(T-cell/histiocyte-rich large B-cell lymphoma),皮膚原発びまん性大細胞型B 細胞リンパ腫-下肢型(Primary cutaneous DLBCL, leg type),および加齢性EBV 陽性びまん性大細胞型B 細胞リンパ腫(EBV positive DLBCL of the elderly),さらに類縁の病型である原発性縦隔大細胞型B 細胞リンパ腫(Primary mediastinal large-B cell lymphoma),血管内大細胞型B 細胞リンパ腫(Intravascular large B-cell lymphoma),慢性炎症に伴うびまん性大細胞型B細胞リンパ腫(DLBCL associated with chronic inflammation),リンパ腫様肉芽腫症(Lymphomatoid granulomatosis),ALK 陽性大細胞型B 細胞リンパ腫(ALK positive LBCL)をまとめてDLBCL として取り扱う。
病期分類にはAnn Arbor 分類3)が,予後予測モデルとしては国際予後指標4)が広く用いられている。治療の効果判定には「NHL の効果判定規準の標準化国際ワークショップレポート」5)が用いられていきたが,近年のFDG-PET の普及度と有用性を受けて,効果判定へFDG-PET を導入した「改訂版NHL の効果判定規準の標準化国際ワークショップレポート」6)が,広く用いられている。
【参考文献】
1) Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008.
2) The world health organization classification of malignant lymphomas in japan : incidence of recently recognized entities. Lymphoma Study Group of Japanese Pathologists. Pathol Int. 2000 ; 50(9) : 696-702.
3) Carbone PP, et al. Report of the committee on Hodgkin’s disease staging classification. Cancer Res. 1971 ; 31(11) : 1860-1.
4) A predictive model for aggressive non-Hodgkin’s lymphoma. The International Non-Hodgkin’s Lymphoma Prognostic Factors Project. N Engl J Med. 1993 ; 329(14) : 987-94.(3iA)
5) Cheson BD, et al. Report of an International Workshop to standardize response criteria for non-Hodgkin’s lymphomas. J Clin Oncol. 1999 ; 17(4) : 1244.
6) Cheson BD, et al. Revised response criteria for malignant lymphoma. J Clin Oncol. 2007 ; 25(5) : 579-86.
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
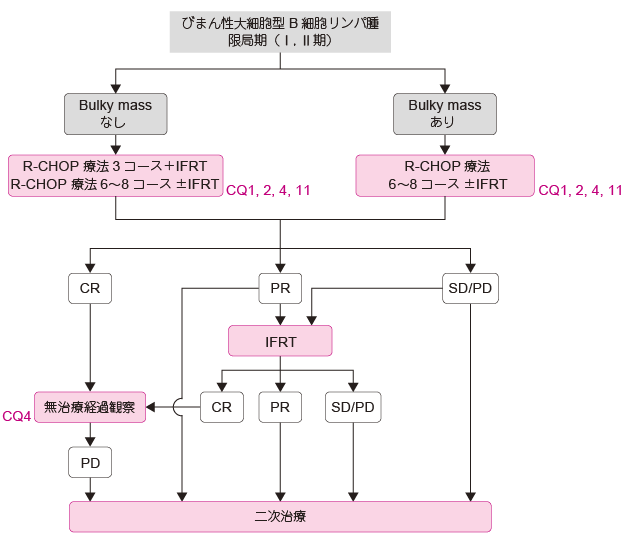
放射線療法の適応を考慮する場合,Ⅱ期では病変が連続性に存在して1 照射野として治療可能であることが必要である。よってここでの限局期は,Ann Arbor 分類での臨床病期Ⅰおよび連続性Ⅱ期を指す。
大規模なランダム化比較試験の結果により,限局期DLBCL に対する標準治療はCHOP 療法(CPA, DXR, VCR, PSL)3 コースに引き続いてinvolved-field radiotherapy(IFRT)を行うcombined modality treatment(CMT)であった1)。なお,bulky mass を有する例はCHOP 療法3 コースとIFRT とのCMT は推奨されない。リツキシマブ(R)導入後は,bulky mass(最大腫瘍径が10 cm を超える,または縦隔病変の最大横径が最大胸郭内径の1/3 以上)を有しない限局期DLBCL に対してはR-CHOP 療法3 コースとIFRT のCMT,あるいはR-CHOP 療法6~8 コースが,bulky mass を有する場合はR-CHOP 療法6~8 コースが推奨される2)3)。R-CHOP 療法3 コースとIFRT のCMT と,R-CHOP 療法6~8 コースを使い分ける明確な指標はなく,6~8 コースの化学療法の適否可能性を考慮して治療を選択する(CQ2)。化学療法の適応が困難な場合は,IFRT を行う。
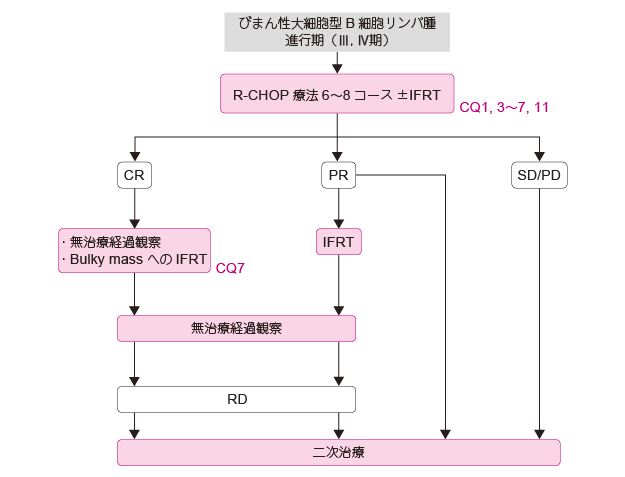
化学療法後の地固め療法としての放射線照射については,8 コースのCHOP 療法後に30 Gy のIFRT を行っても生存が改善しないという比較試験が報告されている4)。しかし, 大規模な後方視的解析では,限局期のみでなく進行期でも放射線照射が行われた例では生存が改善しており5),治療前に病変が存在していた部位,特にbulky mass の場合には,化学療法後にIFRT(従来の領域またはそれ以下)を考慮してもよいと考えられる。
治療後に完全奏効(complete response : CR)へ至った例では無治療で経過観察する。部分奏効(partial response : PR)までの効果しか得られなかった場合,IFRT の後に照射部位に病変が残存し,総照射線量が40 Gy 未満の場合は,計50 Gy 程度までの追加のIFRT を行う。R-CHOP 療法6~8 コース後PR で残存病変が1 照射野に限局している場合,IFRT を行う。SD,PD で救援化学療法の実施が困難な場合はIFRT を行い,それ以外では救援化学療法を行う。
CD20 陽性の進行期DLBCL に対する化学療法は,大規模な比較試験の結果により6~8 コースのR-CHOP 療法が標準治療である6)7)(CQ1, CQ3, CQ4)。6 コースと8 コースを使い分けるエビデンスや規準はなく,化学療法の適否可能性を考慮してコース数を決定する(CQ4)。化学療法後に放射線照射を追加することで全生存が改善する可能性があるため5),治療前に病変が存在していた部位,特にbulky mass が存在していた部位へは,化学療法後にIFRT を考慮してもよい。
R-CHOP 療法後にCR となった場合,R 維持療法による生存割合改善のデータは存在しないため,無治療経過観察とする8)。若年者でIPI のHigh-Intermediate, High risk 群では自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation : HDC/AHSCT)による地固め療法により予後が改善する可能性があるが9),一般診療として推奨できるだけのエビデンスは不十分であり,実施する場合は適切に計画された臨床試験のもとで行う必要がある。その場合は,臨床試験の計画書で定められた治療レジメンを行う(CQ7)。
PR までの効果しか得られず,残存病変が1 照射野に限局しており救援療法の実施が困難な場合は,IFRT を行う。
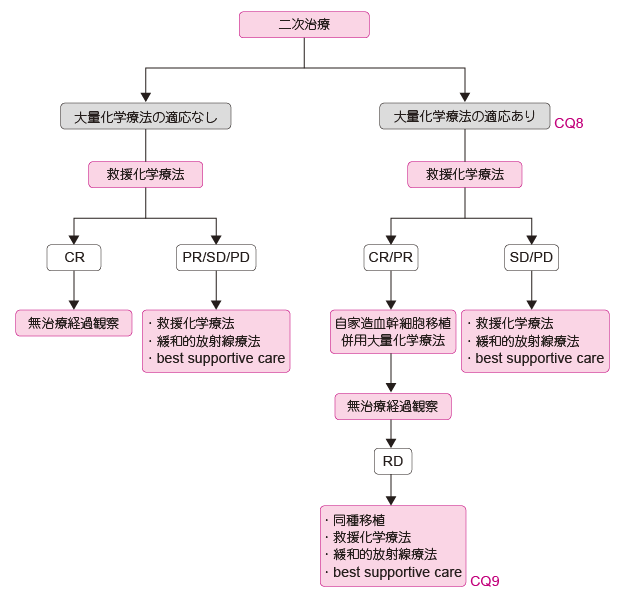
再発・再燃DLBCL に対しては,若年者(65 歳以下)で救援療法により奏効(CR,PR)が得られる場合には,HDC/AHSCT を実施することが推奨される(CQ8)。
初回治療不応/ 再発のDLBCL に対してはHDC/AHSCT 以外のエビデンスが存在しないため,各救援化学療法の優劣は明らかではなく,レジメンは以下のいずれかが選択される。
HDC/AHSCT 後の再発・再燃例に対して同種造血幹細胞移植は考え得る治療選択の一つであるが,治療関連死亡が多く,有用性を示すエビデンスが乏しいため,臨床試験での実施が推奨される(CQ9)。
救援化学療法
DHAP 療法(DEX, CDDP, AraC)(+R)10)11)
(R-)ESHAP 療法(mPSL, ETP, AraC, CDDP)12)
(R-)ICE 療法(IFM, CBDCA, ETP)13)
CHASE(R)療法(CPA, AraC, DEX, ETP)14)
Dose adjusted(DA)-EPOCH(-R)療法(ETP, PSL, VCR, CPA, DER)15)
MINE 療法(MIT, IFM, メスナ,ETP)16)
GDP 療法(Gem, DEX, CDDP)17)
参考文献
1) Miller TP, et al. Chemotherapy alone compared with chemotherapy plus radiotherapy for localized intermediate-and high-grade non-Hodgkin’s lymphoma. N Engl J Med 1998 ; 339(1) : 21-6.(1iiA)
2) Persky DO, et al. Phase Ⅱ study of rituximab plus three cycles of CHOP and involved-field radiotherapy for patients with limited-stage aggressive B-cell lymphoma : Southwest Oncology Group study 0014. J Clin Oncol. 2008 ; 26(14) : 2258-63.(3iiiA)
3) Pfreundschuh M, et al. CHOP-like chemotherapy plus rituximab versus CHOP-like chemotherapy alone in young patients with good-prognosis diffuse large-B-cell lymphoma : a randomised controlled trial by the MabThera International Trial(MInT) Group. Lancet Oncol. 2006 ; 7(5) : 379-91.(1iiDi/1iiA)
4) Horning SJ, et al. Chemotherapy with or without radiotherapy in limited-stage diffuse aggressive non-Hodgkin’s lymphoma : Eastern Cooperative Oncology Group study 1484. J Clin Oncol. 2004 ; 22 (15) : 3032-8.(1iiDii)
5) Phan J, et al. Benefit of consolidative radiation therapy in patients with diffuse large B-cell lymphoma treated with R-CHOP chemotherapy. J Clin Oncol. 2010 ; 28(27) : 4170-6.(3iiiA)
6) Fisher RI, et al. Comparison of a standard regimen(CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma. N Engl J Med. 1993 ; 328(14) : 1002-6.(1iiA)
7) Coiffier B, et al. CHOP chemotherapy plus rituximab compared with CHOP alone in elderly patients with diffuse large-B-cell lymphoma. N Engl J Med. 2002 ; 346(4) : 235-42.(1iiDi/1iiA)
8) Habermann TM, et al. Rituximab-CHOP versus CHOP alone or with maintenance rituximab in older patients with diffuse large B-cell lymphoma. J Clin Oncol.2006 ; 24(19) : 3121-7.(1iiDi)
9) Shipp MA, et al. International Consensus Conference on High-Dose Therapy with Hematopoietic Stem Cell Transplantation in Aggressive Non-Hodgkin’s Lymphomas : report of the jury. J Clin Oncol. 1999 ; 17(1) : 423-9.
10) Gisselbrecht C, et al. Salvage regimens with autologous transplantation for relapsed large B-cell lymphoma in the rituximab era. J Clin Oncol. 2010 ; 28(27) : 4184-90.(1iiDiv/1iiA)
11) Mey UJ, et al. Dexamethasone, high-dose cytarabine, and cisplatin in combination with rituximab as salvage treatment for patients with relapsed or refractory aggressive non-Hodgkin’s lymphoma. Cancer Invest. 2006 ; 24(6) : 593-600.(3iiiA)
12) Martín A, et al. R-ESHAP as salvage therapy for patients with relapsed or refractory diffuse large B-cell lymphoma : the influence of prior exposure to rituximab on outcome. A GEL/TAMO study. Haematologica. 2008 ; 93(12) : 1829-36.(3iiiDiv)
13) Kewalramani T, et al. Rituximab and ICE as second-line therapy before autologous stem cell transplantation for relapsed or primary refractory diffuse large B-cell lymphoma. Blood. 2004 ; 103 (10) : 3684-8.(3iiiDiv)
14) Oki Y, et al. Phase Ⅱ study of a salvage regimen using cyclophosphamide, high-dose cytarabine, dexamethasone, etoposide, and rituximab in patients with relapsed or refractory B-cell non-Hodgkin’s lymphoma. Cancer Sci. 2008 ; 99(1) : 179-84.(3iiiDiv)
15) Jermann M, et al. Rituximab-EPOCH, an effective salvage therapy for relapsed, refractory or transformed B-cell lymphomas : results of a phase Ⅱ study. Ann Oncol. 2004 ; 15(3) : 511-6.(3iiiDi)
16) Rodriguez MA, et al. A phase Ⅱ trial of mesna/ifosfamide, mitoxantrone and etoposide for refractory lymphomas. Ann Oncol. 1995 ; 6(6) : 609-11.(3iiiA)
17) Crump M, et al. Gemcitabine, dexamethasone, and cisplatin in patients with recurrent or refractory aggressive histology B-cell non-Hodgkin lymphoma : a Phase Ⅱ study by the National Cancer Institute of Canada Clinical Trials Group(NCIC-CTG). Cancer. 2004 ; 101(8) : 1835-42.(3iiiDiv)
| CQ1 | DLBCL に対する化学療法にリツキシマブの併用は必要か |
|---|
-
推奨グレードカテゴリー1
- DLBCL に対して化学療法を行う場合,リツキシマブの併用が推奨される。進行期DLBCL に対する化学療法としては,R-CHOP 療法が推奨される。
【解 説】
抗CD20 抗体製剤のリツキシマブ(R)が臨床に導入されて以来,ほとんどの例でCD20 抗原を発現しているDLBCL に対して,R 併用化学療法の開発が進んだ。フランスのGroupe d’Etude des Lymphomes de l’Adulte(GELA)は,初発の60 歳以上の患者を対象としたCHOP 療法とRCHOP 療法の第Ⅲ相比較試験を行い,無イベント生存期間(EFS),全生存期間(OS),完全奏効割合で有意にR-CHOP 療法が上回っていたという結果を報告した1)。ドイツを中心とした研究グループからは若年者,IPI の予後因子数が0 または1,bulky mass を有するⅠ期またはⅡ~Ⅳ期の初発の患者を対象とした,CHOP(またはCHOP 類似)療法と,R-CHOP(またはR-CHOP 類似)療法との比較試験が報告された。ここでも,EFS とOS がR-CHOP 療法で有意に上回っていたという結果であった2)。ドイツのGerman High-Grade Non-Hodgkin Lymphoma Study Group は,初発の高齢者DLBCL 患者を対象にCHOP 療法の治療間隔を短縮したCHOP-14 療法 6 コースまたは8 コース,それにR の併用の有無を比較した試験を行い,EFS とOS がR を併用したレジメンで有意に改善したと報告した3)。これらの結果より,DLBCL に対して化学療法を行う場合はR を併用することが推奨される。
R 導入前にさまざまな多剤併用化学療法がアグレッシブ リンパ腫に対して開発された。しかしアメリカで初発の進行期アグレッシブ リンパ腫を対象としたCHOP 療法とm-BACOD 療法(MTX, BLM, DXR, CPA, VCR, DEX),ProMACE-CytaBOM 療法(PSL, DXR, CPA, ETP, AraC,BLM, VCR, MTX),MACOP-B 療法(MTX, DXR, CPA, VCR, PSL, BLM,)の大規模な比較試験が行われ,無病生存期間(DFS)とOS は4 群の間で差はみられず,致死的な毒性はCHOP 療法で有意に少なかったことが報告された4)。他にも初発のアグレッシブ リンパ腫を対象としたCHOP 療法とm-BACOD 療法,MACOP-B 療法を比較した試験が報告されているが,いずれも生存期間でCHOP 療法を上回るものではなかった5)6)。これらの試験の結果より,初発の進行期アグレッシブ リンパ腫に対する標準的な化学療法レジメンはCHOP 療法であると結論づけられており,R と併用される化学療法としてはCHOP 療法が標準的である。なお,R-CHOP 療法が奏効した後のR 維持療法は,行っても生存が延長しないため不要である7)。
【参考文献】
1) Coiffier B, et al. CHOP chemotherapy plus rituximab compared with CHOP alone in elderly patients with diffuse large-B-cell lymphoma. N Engl. J Med. 2002 ; 346(4) : 235-42.(1iiDi/1iiA)
2) Pfreundschuh M, et al. CHOP-like chemotherapy plus rituximab versus CHOP-like chemotherapy alone in young patients with good-prognosis diffuse large-B-cell lymphoma : a randomised controlled trial by the MabThera International Trial(MInT) Group. Lancet Oncol. 2006 ; 7(5) : 379-91.(1iiDi/1iiA)
3) Pfreundschuh M, et al. Six versus eight cycles of bi-weekly CHOP-14 with or without rituximab in elderly patients with aggressive CD20+B-cell lymphomas : a randomised controlled trial(RICOVER-60). Lancet Oncol. 2008 ; 9(2) : 105-16.(1iiDi/1iiA)
4) Fisher RI, et al. Comparison of a standard regimen(CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma. N Engl J Med. 1993 ; 328(14) : 1002-6.(1iiA)
5) Gordon LI, et al. Comparison of a second-generation combination chemotherapeutic regimen(m-BACOD)with a standard regimen (CHOP) for advanced diffuse non-Hodgkin’s lymphoma. N Engl J Med.1992 ; 327(19) : 1342-9.(1iiA)
6) Cooper IA, et al. Randomized comparison of MACOP-B with CHOP in patients with intermediate-grade non-Hodgkin’s lymphoma. The Australian and New Zealand Lymphoma Group. J Clin Oncol 1994 ; 12(4): 769-78.(1iiDiv)
7) Habermann TM, et al. Rituximab-CHOP versus CHOP alone or with maintenance rituximab in older patients with diffuse large B-cell lymphoma. J Clin Oncol. 2006 ; 24(19) : 3121-7.(1iiDi)
| CQ2 | 初発限局期DLBCL に対する標準治療は何が推奨されるか |
|---|
-
推奨グレードカテゴリー2A
- R-CHOP 療法を3 コース行った後にIFRT を追加するcombined modality treatment が推奨される。
-
推奨グレードカテゴリー1
- R-CHOP 療法6~8 コースが推奨される。
【解 説】
限局期はAnn Arbor 分類での臨床病期Ⅰおよび連続性Ⅱ期に該当する。放射線療法の適応を考慮する場合,Ⅱ期では病変が連続性に存在して1 照射野として治療可能であること,すなわちcontiguous stage Ⅱであることが必要である。
リツキシマブ(R)導入以前にいくつかの大規模ランダム化比較試験が行われた。Southwest Oncology Group(SWOG)で行われたS8736 試験ではCHOP 療法 8 コースと,CHOP 療法3 コースに引き続いてIFRT を行うCMT が比較され,無増悪生存期間(PFS)および全生存期間(OS)でCHOP 療法3 コース+IFRT の成績が有意に良好であった1)。一方GELA では高齢者限局期アグレッシブ リンパ腫を対象としたCHOP 療法4 コース+ IFRT とCHOP 療法4 コースのランダム化第Ⅲ相試験が行われたが,無イベント生存期間(EFS)およびOS において両群に有意差を認めなかった2)。GELA では若年限局期アグレッシブ リンパ腫を対象にして,CHOP 療法3 コース+IF-RT と治療強度を高めた併用化学療法であるACVBP 療法(DXR, CPA, VDS, BLM, PSL)とのランダム化第Ⅲ相試験が行われ,ACVBP 療法が勝ることが報告された3)。しかし,ACBVP 療法は治療強度が高く高毒性である。
R 導入後に行われた限局期DLBCL に対する大規模試験の報告は乏しい。SWOG はstage-modified IPI で1 つ以上の予後因子を有する限局期DLBCL を対象にして,R-CHOP 療法3 コースと放射線治療併用療法の第Ⅱ相試験を施行して良好な治療成績を報告した4)。MabThera International Trial (MInT)は若年低リスクDLBCL を対象に施行された,R 併用化学療法6 コースとR 非併用化学療法のランダム化比較試験である。この試験では臨床病期Ⅰ/Ⅱ期の限局期症例が72%含まれていたが,R 併用化学療法がR 非併用化学療法にEFS,OS で優った5)。なお本試験ではbulky mass や節外病変部位に対して放射線療法が施行された。
以上から限局期DLBCL に対してはR-CHOP 療法3 コース+IFRT のCMT, あるいはR-CHOP 療法6~8 コースが推奨される治療法である。
【参考文献】
1) Miller TP, et al. Chemotherapy alone compared with chemotherapy plus radiotherapy for localized intermediate-and high-grade non-Hodgkin’s lymphoma. N Engl J Med. 1998 ; 339(1) : 21-6.(1iiA)
2) Bonnet C, et al. CHOP Alone Compared With CHOP Plus Radiotherapy for Localized Aggressive Lymphoma in Elderly Patients : A Study by the Groupe d’Etude des Lymphomes de l’Adulte. J Clin Oncol. 2007 ; 25(7) : 787-92.(1iiDi/1iiA)
3) Reyes F, et al. ACVBP versus CHOP plus radiotherapy for localized aggressive lymphoma. N Engl J Med. 2005 ; 352(12) : 1197-205.(1iiDi/1iiA)
4) Persky DO, et al. Phase Ⅱ study of rituximab plus three cycles of CHOP and involved-field radiotherapy for patients with limited-stage aggressive B-cell lymphoma : Southwest Oncology Group study 0014. J Clin Oncol. 2008 ; 26(14) : 2258-63.(3iiiA)
5) Pfreundschuh M, et al. CHOP-like chemotherapy plus rituximab versus CHOP-like chemotherapy alone in young patients with good-prognosis diffuse large-B-cell lymphoma : a randomised controlled trial by the MabThera International Trial(MInT) Group. Lancet Oncol. 2006 ; 7(5) : 379-91.(1iiDi/1iiA)
| CQ3 | 進行期DLBCL に対してdose intensifi ed therapy は推奨されるか |
|---|
-
推奨グレードカテゴリー4
- R-CHOP 療法の強度を高めても予後は改善しないため,dose intensified therapy は推奨されない。
【解 説】
CHOP 療法は,ドキソルビシン(DXR)やシクロホスファミド(CPA)の用量が予後と相関することが知られている1)。そこで,それらの薬剤の用量を増やしたり治療間隔を短縮したdose intensified therapy の有用性が検討されてきたが,初発のアグレッシブ リンパ腫を対象とした複数の比較試験で同様の結果が示されておらず,CHOP 療法の強度を高めたdose intensified therapy の有用性は明確にはされていない2)~4)。DLBCL に対してリツキシマブ(R)併用化学療法が標準治療となってからのdose intensified therapy に関する検討は,イギリスとフランスより報告されているR-CHOP-21 療法とR-CHOP-14 療法の比較試験がある。前者は初発の若年者,高齢者とも対象とした試験であるが,全生存期間で両群に差はみられなかった5)。後者は60 歳以上の初発の高齢者を対象とした試験で,中間解析ではあるが,そこでも無イベント生存期間(EFS)と全生存期間(OS)で両群に差はみられなかった6)。これらのことより,R-CHOP 療法の強度を高める治療は推奨されない。
【参考文献】
1) Kwak LW, et al. Prognostic significance of actual dose intensity in diffuse large-cell lymphoma : results of a tree-structured survival analysis. J Clin Oncol. 1990 ; 8(6) : 963-77.(3iiiA)
2) Pfreundschuh M, et al. Two-weekly or 3-weekly CHOP chemotherapy with or without etoposide for the treatment of young patients with good-prognosis(normal LDH) aggressive lymphomas : results of the NHL-B1 trial of the DSHNHL. Blood. 2004 ; 104(3) : 626-33.(1iiDi/1iiA)
3) Pfreundschuh M, et al. Two-weekly or 3-weekly CHOP chemotherapy with or without etoposide for the treatment of elderly patients with aggressive lymphomas : results of the NHL-B2 trial of the DSHNHL. Blood. 2004 ; 104(3). 634-41.(1iiDi/1iiA)
4) Ohmachi K, et al. Phase Ⅲ trial of CHOP-21 versus CHOP-14 for aggressive non-Hodgkin’s lymphoma : final results of the Japan Clinical Oncology Group Study, JCOG 9809. Ann Oncol. 2011 ; 22 (6) : 1382-91.(1iiDiii)
5) Cunningham D, et al. Rituximab plus cyclophosphamide, doxorubicin, vincristine, and prednisolone in patients with newly diagnosed diffuse large B-cell non-Hodgkin lymphoma : a phase 3 comparison of dose intensification with 14-day versus 21-day cycles. Lancet. 2013 ; 381(9880) : 1817-26.(1iiA)
6) Delarue R, et al. Dose-dense rituximab-CHOP compared with standard rituximab-CHOP in elderly patients with diffuse large B-cell lymphoma (the LNH03-6B study) : a randomised phase 3 trial. Lancet Oncol. 2013 ; 14(6) 525-33.(1iiDi/1iiA)
| CQ4 | 進行期DLBCL に対するR-CHOP 療法におけるCHOP 療法の至適コース数は何コースか |
|---|
-
推奨グレードカテゴリー2A
- 標準的なR-CHOP 療法のコース数は6~8 コースであるが,6 コースと 8 コースの差は不明である。
【解 説】
CHOP 療法(CPA, DXR, VCR, PSL)は1960 年代に開発された併用化学療法レジメンであるが,原法はCHOP 療法を完全奏効まで行い,奏効となった後にCOP 療法(CPA, VCR, PSL)またはOAP 療法(VCR, AraC, PSL)による維持療法を3~4 週毎に18 カ月間行うというものであった1)。当初は心毒性を考慮しドキソルビシン(DXR)の総投与量によりコース数が規定されていたが1)2),その後, 病変が消失してから2 コース追加・最大6 コースまで,または8 コースのセットの治療として行われるようになった3)4)。CHOP 療法(R-CHOP 療法)が標準治療であると決定づけた比較試験では,CHOP 療法(R-CHOP 療法)は8 コースで行われているが,明確な根拠はない。DLBCL に対する標準治療のR-CHOP-21 療法では,6 コースと8 コースを比較したエビデンスは存在しないため,至適コース数は未確定である。
【参考文献】
1) McKelvey EM, et al. Hydroxyldaunomycin (Adriamycin) combination chemotherapy in malignant lymphoma. Cancer. 1976 ; 38(4) : 1484-93.(1iiA)
2) Elias L, et al. Combination chemotherapy of diffuse histiocytic lymphoma with cyclophosphamide, adriamycin, vincristine and prednisone(CHOP). Cancer. 1978 ; 42(4) : 1705-10.(3iiiDiv)
3) Jones SE. Chemoimmunotherapy versus chemotherapy for remission induction in patients with non-Hodgkin’s lymphoma. progress report of a Southwest Oncology Group study. Recent Results Cancer Res. 1978 ; 65 : 164-9.(1iiA)
4) Armitage JO, et al. Advanced diffuse histiocytic lymphoma treated with cyclophosphamide, doxorubicin, vincristine, and prednisone (CHOP) without maintenance therapy. Cancer Treat Rep. 1980 ; 64(4-5) : 649-54.(3iiiDiv)
| CQ5 | DLBCL では中枢神経系再発予防のための髄注は必要か |
|---|
-
推奨グレードカテゴリー2A
- 精巣原発のDLBCL では,中枢神経系再発予防のためR-CHOP 療法に予防的髄注を併用することが推奨される。
-
推奨グレードカテゴリー2B
- 進行期,骨髄浸潤陽性,節外病変を多数有するIPI 高リスク例,副鼻腔原発のDLBCL 例では,髄注を併用することで中枢神経系再発の頻度が下がる可能性があるが,有用性が確立しているわけではない。
【解 説】
精巣原発のDLBCL に関しては,International Extranodal Lymphoma Study Group により大規模な後方視的解析が報告され,373 例のうち52%が再発し,10 年までの累積の中枢神経系再発は15%であった1)。同グループは,病期Ⅰ~Ⅱ期の初発の精巣原発DLBCL 患者に対して,R-CHOP 療法6~8 コースに4 回のメトトレキサートの髄注,対側精巣への放射線照射(Ⅱ期の例では,リンパ節病変の領域にも照射)を併用するという前方視的第Ⅱ相試験を行い,5 年の累積中枢神経系再発割合が6%という結果を報告した2)。これらの結果より,精巣原発のDLBCL に対しては予防的髄注と放射線照射の併用が推奨される。
DLBCL では,2~10%に中枢神経系再発が起こるとされている3)~6)。骨髄,副鼻腔,眼窩,骨/椎体,末梢血に病変を有する例は予防的に髄注を行うと中枢神経系再発の頻度が下がる可能性はあるが,定まった見解はない7)8)。
【参考文献】
1) Zucca E, et al. Patterns of outcome and prognostic factors in primary large-cell lymphoma of the testis in a survey by the International Extranodal Lymphoma Study Group. J Clin Oncol. 2003 ; 21 (1) : 20-7.(3iiA)
2) Vitolo U, et al. First-line treatment for primary testicular diffuse large B-cell lymphoma with rituximab-CHOP, CNS prophylaxis, and contralateral testis irradiation : final results of an international phase Ⅱ trial. J Clin Oncol. 2011 ; 29(20) : 2766-72.(3iiiDiii)
3) Hollender A, et al. Central nervous system involvement following diagnosis of non-Hodgkin’s lymphoma : a risk model. Ann Oncol. 2002 ; 13(7) : 1099-107.(3iD)
4) Shimazu Y, et al. Diffuse large B-cell lymphoma with central nervous system relapse : prognosis and risk factors according to retrospective analysis from a single-center experience. Int J Hematol. 2009 ; 89(5) : 577-83.(3iD)
5) Villa D, et al. Incidence and risk factors for central nervous system relapse in patients with diffuse large B-cell lymphoma : the impact of the addition of rituximab to CHOP chemotherapy. Ann Oncol. 2010 ; 21(5) : 1046-52.(3iD)
6) Bernstein SH, et al. Natural history of CNS relapse in patients with aggressive non-Hodgkin’s lymphoma : a 20-year follow-up analysis of SWOG 8516--the Southwest Oncology Group. J Clin Oncol. 2009 ; 27(1): 114-9.(3iiiD)
7) Arkenau HT, et al. The role of intrathecal chemotherapy prophylaxis in patients with diffuse large B-cell lymphoma. Ann Oncol. 2007 ; 18(3) : 541-5.(3iiiD)
8) Laskin JJ, et al. Primary paranasal sinus lymphoma : natural history and improved outcome with central nervous system chemoprophylaxis. Leuk Lymphoma. 2005 ; 46(12) : 1721-7.(3iiiD)
| CQ6 | 心機能の低下が予想される初発DLBCL に対して適 切な化学療法は何が推奨されるか |
|---|
-
推奨グレードカテゴリー2A
- ドキソルビシンの投与量低減あるいは中止,ボーラス投与から持続投与への変更を考慮する。
【解 説】
ドキソルビシン(DXR)の代表的な毒性に心筋障害がある。心筋障害による心不全発症のリスクはDXR の累積投与量と相関しており,総投与量が400 mg/m2 未満では発症割合は0.14%程度であるが,550 mg/m2 になると7%,700 mg/m2 を超えると18%まで上昇するとされている1)。DLBCL に対する化学療法ではDXR のactual relative dose intensity が予後と相関するとされているが2),Dutch-Belgian Hemato-Oncology Cooperative Group(HOVON)で行われた,初発の高齢者アグレッシブ リンパ腫を対象とした試験では,G-CSF の予防投与によりrelative dose intensity は有意に改善したが,生存に差はなかった3)。DXR を含んだ化学療法を受けたDLBCL 患者の大規模な後方視的研究では,化学療法のコース数が6 コース未満であった場合は心不全のリスクは増加せず4),アイオワ大学でCHOP 療法(CPA, DXR, VCR, PSL)を受けた中悪性度NHL 患者の後方視的解析では,毒性などで治療が6 コース未満で早期中止となった場合,74 歳未満では生存期間が低下するが,75 歳以上では6 コース以上の治療を完遂した例と比べて生存期間は低下しなかった5)。これらのことより,心機能の低下が予想される高齢者に対しては,DXR による心筋障害の危険性軽減のための薬剤の減量や中止は,考慮すべき方法のひとつである。
アントラサイクリンを含んだレジメンのメタアナリシスでは,心筋障害のリスクはミトキサントロン(MIT)よりもアントラサイクリンで,アントラサイクリンの持続投与よりもボーラス投与で有意に高かったが6),CHOP 療法のDXR をMIT へ変更したCNOP 療法とCHOP 療法の未治療例に対する比較試験の報告では,心毒性の頻度は同等であったが,生存に関しては有意にCHOP 療法が上回っていた7)8)。これらのことから,心筋障害のリスク軽減を目的にDXR をMIT へ変更することは予後が劣る可能性があるため,推奨されない。わが国で開発されたDXR のアナログにピラルビシン(THP-DXR)がある。この薬剤は,動物モデルでは心筋障害はDXR よりも軽度であることが示されている9)。CHOP-14 療法と,CHOP-14 療法のDXR を同量のTHP-DXR へ置き換えたTHP-COP-14 療法のアグレッシブ リンパ腫を対象としたランダム化第Ⅱ相試験では,奏効割合,全生存期間(OS)は両群で同等で,重篤な心筋障害はTHP-COP-14 療法群で1 例も起こらなかったとされており10),小規模な報告ではあるが,THP-COP 療法がCHOP 療法の代替となる可能性が示唆されている。DXR の持続投与法を検討した臨床試験としては,初発のDLBCL に対するdose-adjusted(DA)-EPOCH 療法(ETP, PSL, VCR, CPA, DXR)の第Ⅱ相試験がある。血液毒性による用量調整で,DXR はほとんどの例で増量されていたにもかかわらず1 例も心毒性はみられず,良好な成績が報告されていた11)。DXR の投与法をボーラス投与から持続投与へ変更することで,心毒性は軽減され,CHOP 療法と同等の効果が得られる可能性が示唆されている。
【参考文献】
1) Von Hoff DD, et al. Risk factors for doxorubicin-induced congestive heart failure. Ann Intern Med. 1979 ; 91(5) : 710-7.(3iiiD)
2) Kwak LW, et al. Prognostic significance of actual dose intensity in diffuse large-cell lymphoma : results of a tree-structured survival analysis. J Clin Oncol. 1990 ; 8(6) : 963-77.(3iiiA)
3) Doorduijn JK, et al. CHOP compared with CHOP plus granulocyte colony-stimulating factor in elderly patients with aggressive non-Hodgkin’s lymphoma. J Clin Oncol. 2003 ; 21(16) : 3041-50.(1iiDiv)
4) Hershman DL, et al. Doxorubicin, cardiac risk factors, and cardiac toxicity in elderly patients with diffuse B-cell non-Hodgkin’s lymphoma. J Clin Oncol. 2008 ; 26(19) : 3159-65.(3iiiD)
5) Chrischilles EA, et al. Factors associated with early termination of CHOP therapy and the impact on survival among patients with chemosensitive intermediate-grade non-Hodgkin’s lymphoma. Cancer Control. 2003 ; 10(5) : 396-403.(3iiiA)
6) Smith LA, et al. Cardiotoxicity of anthracycline agents for the treatment of cancer : systematic review and meta-analysis of randomised controlled trials. BMC Cancer. 2010 ; 10 : 337.(1iiD)
7) Sonneveld P, et al. Comparison of doxorubicin and mitoxantrone in the treatment of elderly patients with advanced diffuse non-Hodgkin’s lymphoma using CHOP versus CNOP chemotherapy. J Clin Oncol. 1995 ; 13(10) : 2530-9.(1iiA)
8) Osby E, et al. CHOP is superior to CNOP in elderly patients with aggressive lymphoma while outcome is unaffected by filgrastim treatment : results of a Nordic Lymphoma Group randomized trial. Blood. 2003 ; 101(10) : 3840-8.(1iiDi)
9) Dantchev D, et al. Low heart and skin toxicity of a tetrahydropyranyl derivative of adriamycin (THPADM)as observed by electron and light microscopy. J Antibiot(Tokyo). 1979 ; 32(10) : 1085-6.
10) Tsurumi H, et al. Biweekly CHOP or THP-COP regimens in the treatment of newly diagnosed aggressive non-Hodgkin’s lymphoma. A comparison of doxorubicin and pirarubicin : a randomized phase Ⅱ study. J Cancer Res Clin Oncol. 2004 ; 130(2) : 107-13.(3iiiDiv)
11) Wilson WH, et al. Dose-adjusted EPOCH chemotherapy for untreated large B-cell lymphomas : a pharmacodynamic approach with high efficacy. Blood. 2002 ; 99(8) : 2685-93.(3iiiDiv)
| CQ7 | 初回化学療法で奏効を得たDLBCL に対して引き続き自家造血幹細胞移植併用大量化学療法による地固め療法を行うことは勧められるか |
|---|
-
推奨グレードカテゴリー4
- 若年者高リスク群(IPI : High/Intermediate, High)においても一般診療として推奨できるだけのエビデンスは不十分であり,臨床試験での実施が推奨される。
-
推奨グレードカテゴリー4
- 高齢者や若年者低リスク群(IPI : Low, Low/Intermediate)には推奨されない。
【解 説】
自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)が実施可能な対象は若年者(65 歳以下)であり,高齢者には推奨されない。国際予後指標(International Prognostic Index:IPI)低リスク群(Low,Low/Intermediate)では,標準的化学療法R-CHOP 療法の4 年全生存割合(OS)は80%以上と良好であり1),初回治療奏効後に組み込んだ(up front)HDC/AHSCT は推奨されない。一方,初回治療の地固めとしてHDC/AHSCT を検討する場合には,若年者IPI 高リスク群(High/Intermediate,High)が妥当であることが報告された2)。リツキシマブ(R)導入以前の比較試験においては,HDC/AHSCT の有効性が示された試験3)4)と有効性が示されなかった試験5)6)があり,有効性に関しての一定した結論は得られていなかった。
R 導入後には,中間解析も含めると4 試験の結果が発表されている7)~10)。2 つの試験では2 年無増悪生存割合(PFS)でup front HDC/AHSCT の成績が優れているとの結果であったが9)10),2つの試験においては優位性が示されなかった7)8)。いずれの試験においてもOS での有用性は示されていない。しかし探索的な解析で,IPI-high リスク群は2 年PFS,OS が優れているとの結果が示されており9),HDC/AHSCT により成績の向上が期待できる患者群の存在が示唆されている。
以上より,若年者高リスク群に対してもup front HDC/AHSCT は未だ標準治療とは言えず,臨床試験での実施が推奨される。
【参考文献】
1) Sehn LH, et al. The revised International Prognostic Index(R-IPI) is a better predictor of outcome than the standard IPI for patients with diffuse large B-cell lymphoma treated with R-CHOP. Blood. 2007 ; 109(5) : 1857-61.(3iA/3iDiii)
2) Shipp MA, et al. International Consensus Conference on High-Dose Therapy with Hematopoietic Stem Cell Transplantation in Aggressive Non-Hodgkin’s Lymphomas : report of the jury. J Clin Oncol. 1999 ; 17(1) : 423-9.
3) Haioun C, et al. Survival benefit of high-dose therapy in poor-risk aggressive non-Hodgkin’s lymphoma : final analysis of the prospective LNH87-2 protocol--a groupe d’Etude des lymphomes de l’Adulte study. J Clin Oncol. 2000 ; 18(16) : 3025-30.(1iiDiii/1iiA)
4) Milpied N, et al. Initial treatment of aggressive lymphoma with high-dose chemotherapy and autologous stem-cell support. N Engl J Med. 2004 ; 350(13) : 1287-95.(1iiDi/1iiA)
5) Gisselbrecht C, et al. Shortened first-line high-dose chemotherapy for patients with poor-prognosis aggressive lymphoma. J Clin Oncol. 2002 ; 20(10) : 2472-9.(1iiDi/1iiA)
6) Verdonck LF, et al. Comparison of CHOP chemotherapy with autologous bone marrow transplantation for slowly responding patients with aggressive non-Hodgkin’s lymphoma. N Engl J Med. 1995 ; 332(16) : 1045-51.(1iiA)
7) Le Gouill S, et al. First-line rituximab (R) high-dose therapy (R-HDT) versus R-CHOP14 for young adults with diffuse large B-cell lymphoma : Preliminary results of the GOELAMS 075 prospective multicenter randomized trial. J Clin Oncol(ASCO Meeting Abstracts). 2011 ; 29 : 8003.(1iiDi/1iiA)
8) Schmitz N, et al. Conventional chemoimmunotherapy (R-CHOEP-14) or high-dose therapy (R-Mega-CHOEP) for young, high-risk patients with aggressive B-cell lymphoma : Final results of the randomized Mega-CHOEP trial of the German High-Grade Non-Hodgkin Lymphona Study Group(DSHNHL). J Clin Oncol(ASCO Meeting Abstracts). 2011 ; 29 : 8002.(1iiDi/1iiA)
9) Stiff PJ, et al. Randomized phase Ⅲ U.S./Canadian intergroup trial(SWOG S9704) comparing CHOP{ +/ -} R for eight cycles to CHOP {+/-} R for six cycles followed by autotransplant for patients with high-intermediate (H-Int) or high IPI grade diffuse aggressive non-Hodgkin lymphoma (NHL). J Clin Oncol(ASCO Meeting Abstracts). 2011 ; 29 : 8001.(1iiDiii/1iiA)
10) Vitolo U, et al. A Randomized Multicenter Phase Ⅲ Study for First Line Treatment of Young Patients with High Risk (AAIPI 2-3) Diffuse Large B-Cell Lymphoma (DLBCL) : Rituximab (R) Plus Dose-Dense Chemotherapy CHOP14/MEGACHOP14 with or without Intencified High-Dose Chemotherapy(HDC) and Autologous Stem Cell Transplantation (ASCT). Results of DLCL04 Trial of Italian Lymphoma foundation(FIL). Ann Oncol. 2011 ; 22 : 072.(1iiDiii/1iiA)
| CQ8 | 再発・再燃DLBCL に対して自家造血幹細胞移植併用大量化学療法は勧められるか |
|---|
-
推奨グレードカテゴリー1
- 若年者(65 歳以下)で救援療法に奏効(完全奏効+部分奏効)が認められる場合には,自家造血幹細胞移植併用大量化学療法を実施することが推奨される。
【解 説】
再発・再燃DLBCL に対して通常の救援療法単独での長期予後は満足すべきものではなく,救援療法に引き続く地固め療法としての自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)による長期予後成績の改善が試みられてきた1)。
DLBCL を主体とする再発・再燃中高悪性度リンパ腫に対して,HDC/AHSCT の優位性を示した比較試験はPARMA 試験である2)。DHAP 療法2 コース後に奏効を認めた患者を,さらに4コースのDHAP と放射線治療を実施する群とHDC/AHSCT と放射線療法を実施する群に割り付けを行い比較した。5 年全生存割合,無イベント生存割合ともにHDC/AHSCT 群が優れていた。
リツキシマブ(R)導入後のHDC/AHSCT の有無に関する比較試験は実施されていないが,診断後12 カ月以降の再発症例に関しては,初回治療のR 使用の有無は無イベント生存期間に影響を及ぼさず,R 導入後においても再発・再燃DLBCL に対してのHDC/AHSCT の実施は推奨される3)。
以上より,HDC/AHSCT の対象となる65 歳以下の再発・再燃DLBCL に対しては,救援療法に奏効(完全奏効+部分奏効)が認められる場合には,HDC/AHSCT を実施することが推奨される。
【参考文献】
1) Philip T, et al. High-dose therapy and autologous bone marrow transplantation after failure of conventional chemotherapy in adults with intermediate-grade or high-grade non-Hodgkin’s lymphoma. N Engl J Med. 1987 ; 316(24) : 1493-8.(3iiDii)
2) Philip T, et al. Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin’s lymphoma. N Engl J Med. 1995 ; 333(23) : 1540-5.(1iiDi/1iiA)
3) Gisselbrecht C, et al. Salvage regimens with autologous transplantation for relapsed large B-cell lymphoma in the rituximab era. J Clin Oncol. 2010 ; 28(27) : 4184-90.(1iiDiv/2A)
| CQ9 | 再発・再燃DLBCL に対して同種造血幹細胞移植の適応はあるか |
|---|
-
推奨グレードカテゴリー2B
- 自家造血幹細胞移植併用大量化学療法後の再発・再燃症例に対して同種造血幹細胞移植は考慮されるべき治療選択の一つだが,臨床試験での実施が推奨される。
【解 説】
再発・再燃DLBCL に対しては,同種造血幹細胞移植(以下,同種移植)ではなく,まずは自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)の適応が考慮される。HDC/AHSCT 後の再発・再燃は絶対的予後不良であり,何らかの臨床試験による治療法が推奨されるが,その選択肢の一つに同種移植が挙げられる。また,自家末梢血幹細胞採取が不良な患者においても,同種移植が治療選択の一つとして考慮されるが,この場合にも臨床試験としての実施が推奨される。
DLBCL に対する同種移植に関する大規模な前方視的試験のデータは乏しく,多くは後方視的解析である。従来の骨髄破壊的同種移植は,再発は少ないものの,非再発治療関連死亡が50%と多いため,HDC/AHSCT に対する優位性は示されていない1)2)。治療関連死亡を減らすため,HDC/ AHSCT 後の再発例に対して骨髄非破壊的同種移植を実施した症例の多施設および登録データによる後方視的解析では,非再発治療関連死亡が約30%,生存割合が約50%と報告されている3)4)。これらの結果からは,骨髄非破壊的同種移植により長期生存が得られる患者群が存在することが示唆される。
以上より,HDC/AHSCT 後の再発症例に対して同種移植は考慮されるべき治療選択の一つであるが,臨床試験での実施が推奨される。
【参考文献】
1) Aksentijevich I, et al. Clinical outcome following autologous and allogeneic blood and marrow transplantation for relapsed diffuse large-cell non-Hodgkin’s lymphoma. Biol Blood Marrow Transplant. 2006 ; 12(9): 965-72.(3iiiA)
2) Peniket AJ, et al. An EBMT registry matched study of allogeneic stem cell transplants for lymphoma : allogeneic transplantation is associated with a lower relapse rate but a higher procedure-related mortality rate than autologous transplantation. Bone Marrow Transplant. 2003 ; 31(8) : 667-78.(3iiA)
3) Thomson KJ, et al. Favorable long-term survival after reduced-intensity allogeneic transplantation for multiple-relapse aggressive non-Hodgkin’s lymphoma. J Clin Oncol. 2009 ; 27(3) : 426-32.(3iiiD/3iiiA)
4) van Kampen RJ, et al. Allogeneic stem-cell transplantation as salvage therapy for patients with diffuse large B-cell non-Hodgkin’s lymphoma relapsing after an autologous stem-cell transplantation : an analysis of the European Group for Blood and Marrow Transplantation Registry. J Clin Oncol. 2011 ; 29(10) : 1342-8.(3iiA)
| CQ10 | 節外性リンパ腫など治療上の特別な配慮が必要なDLBCL の病態・病型には何があるか |
|---|
-
推奨グレードカテゴリー2A
- 中枢神経系原発DLBCL に対してはメトトレキサート大量療法を基盤とする化学療法を先行し,引き続き全脳照射を行う治療が推奨される。ただし高齢者では全脳照射による遅発性中枢神経障害のリスクに注意を要する。精巣原発DLBCL に対しては中枢神経系および精巣の再発予防法を併用することが推奨される(CQ6)。
【解 説】
DLBCL にはいくつかの亜型や類縁病型がある。また,WHO 分類(2008)では規定されない節外性DLBCL の中には特徴的な病態を示すものがある。これらのうち一部については治療上の特別な配慮が必要である。中枢神経原発DLBCL では中枢神経系への薬剤移行などを考慮して,メトトレキサート(MTX)大量療法を基盤とする化学療法を先行し,引き続き全脳照射を行う治療が推奨される。ただし高齢者では全脳照射による遅発性中枢神経障害のリスクに注意を要する。(現在,日本脳腫瘍学会がPCNSL を含む脳腫瘍診療ガイドラインを作成中であり,PCNSL については日本血液学会として作成に協力している。本CQ におけるPCNSL の記載は脳腫瘍診療ガイドラインにおけるPCNSL 案を踏まえたものである。これは近日中に日本癌治療学会および日本脳腫瘍学会のホームページで公表予定であり,その参照を推奨する)。精巣原発DLBCL では中枢神経系および対側精巣での再発を予防するために,R-CHOP に加えて予防的な抗がん剤の髄腔内投与と健側を含む精巣への放射線照射が推奨される(CQ5)。胃原発DLBCL についてはCQ11 で解説する。
これら以外の節外性DLBCL,および総論でDLBCL として取り扱うと記載したものについてはDLBCL ガイドラインに従うことを推奨する。
| CQ11 | 胃原発DLBCL の治療方針は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 胃DLBCL についてはLugano 分類に基づく病期分類を行い,限局期と進行期に区分して取り扱う。治療としてはDLBCL で推奨される治療法が推奨される。
【解 説】
消化管悪性リンパ腫の臨床病期分類としては,Ann Arbor 分類に加えてLugano 分類が用いられる1)。胃原発DLBCL についてはLugano 分類でのⅠ期,およびⅡ1 期を限局期として取り扱う。
リツキシマブ(R)導入前に施行された,限局期胃DLBCL に対して外科手術,外科手術と放射線治療,外科手術と化学療法,および化学療法を比較するランダム化比較試験では,化学療法が全生存期間で優れ,かつ外科手術を含む治療法よりも治療関連死亡(TRM)が少ないことが報告された2)。また外科手術は行わずにCHOP 療法に引き続いてinvolved field rediotherapy(IFRT)を行う治療について,良好な生存期間と胃穿孔や消化管出血など重篤な有害事象の頻度が低いことが報告された3)4)。このため現在では胃切除術を行わずに化学療法,ないしは化学療法に引き続いて放射線療法を行う胃温存療法が標準治療と考えられる。R 導入後では後方視的な検討によってR-CHOP 療法やR-CHOP 療法に引き続いてIFRT を行う治療法によって良好な生存期間が報告されている5)6)。限局期DLBCL に対するR-CHOP 療法とCHOP 療法の比較試験はないが,限局期DLBCL と同様に,限局期胃DLBCL に対してもR-CHOP 療法3 コースに引き続いてIFRT を行うCMT,あるいはR-CHOP 療法6~8 コースが推奨される。
Lugano 分類でのⅡ2 期以上が該当する進行期胃DLBCL に対しては,進行期DLBCL と同様にR-CHOP 療法6~8 コースが推奨される。
ただし,胃病変局所からの出血や深い潰瘍性病変を認める場合は,R-CHOP 療法などの化学療法開始後に大量出血や胃穿孔を併発するリスクが高くなるため,この点への注意が必要なことと緊急外科手術を要する状況が起こり得ることを患者・家族に十分に説明しておく必要がある。
【参考文献】
1) Rohatiner A, et al. Report on a workshop convened to discuss the pathological and staging classifications of gastrointestinal tract lymphoma. Ann Oncol. 1994 ; 5(5) : 397-400.
2) Aviles A, et al. The role of surgery in primary gastric lymphoma : results of a controlled clinical trial. Ann Surg. 2004 ; 240(1) : 44-50.(1A)
3) Ishikura S, et al. Japanese multicenter phase Ⅱ study of CHOP followed by radiotherapy in stage Ⅰ-Ⅱ, diffuse large B-cell lymphoma of the stomach. Cancer Sci. 2005 ; 96(6) : 349-52.(2A)
4) Koch P, et al. Treatment results in localized primary gastric lymphoma : data of patients registered within the German multicenter study(GIT NHL 02/96). J Clin Oncol. 2005 ; 23(28) : 7050-9.(2A)
5) Wohrer S, et al. Rituximab, cyclophosphamide, doxorubicin, vincristine and prednisone (R-CHOP) for treatment of early-stage gastric diffuse large B-cell lymphoma. Ann Oncol. 2004 ; 15(7) : 1086-90.(3iiiA)
6) Tanaka T, et al. Retrospective analysis of primary gastric diffuse large B cell lymphoma in the rituximab era : a multicenter study of 95 patients in Japan. Ann Hematol. 2012 ; 91(3) : 383-90.(3iiiA)
6
バーキットリンパ腫
(Burkitt lymphoma:BL)
(Burkitt lymphoma:BL)
◆総論
バーキットリンパ腫(Burkitt lymphoma:BL)は腫瘤形成性の高悪性度(highly aggressive)B 細胞リンパ腫である。WHO 分類(2008)では“Burkitt lymphoma”と,“Burkitt leukemia variant”が掲載された1)。BL には赤道アフリカやパプアニューギニアなどに多く見られるendemic BL,欧米や日本などで認められるsporadic BL およびhuman immunodeficiency virus(HIV)感染に関連して発症するimmunodeficiency associated BL の3 つの臨床病型が知られている。発生頻度は成人では悪性リンパ腫全体の1~2%程度であるが,小児においては,endemic 地域では全小児悪性腫瘍の過半数を,non-endemic 地域では25~40%を占め,男女比は2~3:1 で男性に多い。回盲部腫瘤などの腹部腫瘤で発症することが多く,腹腔内リンパ節,卵巣,腎,乳房,骨髄,中枢神経などへの浸潤も珍しくない。臨床的には極めて進行が速いが,適切な治療を行うことで高率に治癒が期待できる病型でもある。
典型的なBL では,小型から中型までの腫瘍細胞がびまん性かつ融合性増殖を示し,核片を貪食するマクロファージが淡く抜けてstarry sky appearance(星空像)を呈し,95%超の細胞でKi-67 が陽性で,MYC 転座が認められる2)。またgene expression profiling(GEP)では,特徴的なmolecular signature を有するがMYC 転座を認めない例,BL とDLBCL との中間型のmolecular signature を示す一群も同定された3)4)。これらの結果を受けWHO 分類(2008)では,MYC 転座の有無にかかわらず,形態および形質でBL,びまん性大細胞型B 細胞リンパ腫(diffuse large B cell lymphoma:DLBCL)を診断し,BL としてもDLBCL としても非定型的である場合は,暫定的な疾患群であるB-cell lymphoma, unclassifiable, with features intermediate between DLBCL and BL(Intermediate DLBCL/BL)と診断するとした5)。
BL は小児や若年成人の発症が多いため,Ann Arbor 分類ではなく,St. Jude/Murphy の病期分類がしばしば使用される6)。節性病変を主体とするホジキンリンパ腫に対する分類からスタートしたAnn Arbor 分類よりも,節外病変主体のBL にはSt. Jude/Murphy の病期分類の方がリスク予測と合致すると言われる。しかし成人,とくに高齢成人では,Ann Arbor 分類が使用されることが多い。
予後不良因子としては,年齢(40 歳以上),LDH 上昇,中枢神経系浸潤,骨髄浸潤,10 cm 超の巨大腫瘤,+7q, de(l 13)の染色体異常が知られている7)。
BL ではFDG-PET 検査が感度,特異度ともに高いため8),治療効果判定にはPET を組み込んだ改訂国際ワークショップ規準9)が望ましい。ただし,急激な病勢の進行のため,治療開始前のFDG-PET 検査は実施困難な場合がある。
【参考文献】
1) Leoncini L, et al. Burkitt lymphoma. WHO Classification of Tumours of Hematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008 : pp262-4.
2) Pelicci PG, et al. Chromosomal breakpoints and structural alterations of the c-myc locus differ in endemic and sporadic forms of Burkitt lymphoma. Proc Natl Acad Sci U S A. 1986 ; 83(9) : 2984-8.
3) Hummel M, et al. A biologic definition of Burkitt’s lymphoma from transcriptional and genomic profiling. N Engl J Med. 2006 ; 354(23) : 2419-30.
4) Dave SS, et al. Molecular diagnosis of Burkitt’s lymphoma. N Engl J Med. 2006 ; 354(23) : 2431-42.
5) Kluin PM, et al. B-cell lymphoma, unclassifiable, with features intermediate between diffuse large B-cell lymphoma and Burkitt lymphoma. WHO Classification of Tumours of Hematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008 : pp265-6.
6) Murphy SB. Classification, staging and end results of treatment of childhood non-Hodgkin’s lymphomas : dissimilarities from lymphomas in adults. Semin Oncol. 1980 ; 7(3) : 332-9.(3iiiD)
7) Poirel HA, et al. Specific cytogenetic abnormalities are associated with a significantly inferior outcome in children and adolescents with mature B-cell non-Hodgkin’s lymphoma : results of the FAB/LMA 96 international study. Luekemia. 2009 ; 23(2) : 323-31.(2Di)
8) Karantanis D, et al. 18F-FDG PET and PET/CT in Burkitt’s lymphoma. Eur J Radiol. 2010 ; 75(1) : e68-73.(3iiiD)
9) Cheson BD, et al. Revised response criteria for malignant lymphoma. J Clin Oncol. 2007 ; 25(5) : 579-86.
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
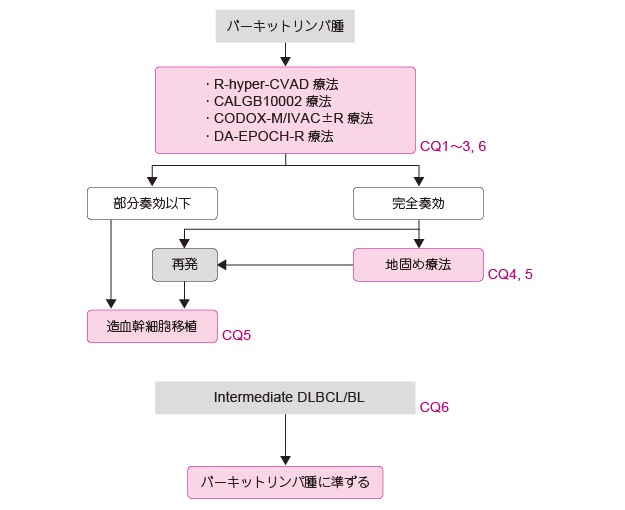
BL と診断された場合は上記のアルゴリズムに従うことが推奨される。BL に対して複数の標準治療レジメンが報告されているが,それぞれの優劣は明らかでなく,リツキシマブ(R)併用の意義もレジメンにより異なる可能性がある(CQ1, CQ2)。腫瘍崩壊症候群の発症頻度が高く,特に初回化学療法施行時にその予防は必須である(CQ3)。地固め療法としての放射線照射や造血幹細胞移植の意義は不明であり,また予防的全脳照射は避けるべきである(CQ4, CQ5)。初回治療抵抗患者や再発患者に対する造血幹細胞移植の有用性は確立されていないが,救援療法感受性例に対しては,自家造血幹細胞移植併用大量化学療法の効果が期待できる(CQ5)。
Intermediate DLBCL/BL は暫定的な疾患群であり,標準治療アプローチは現時点で明確でないが,BL に準じた治療選択が妥当と考えられる。(CQ6)。
| CQ1 | BL に対する初回治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー2A
- 複数の治療レジメンが報告されており,それぞれの優劣は不明である。Modified CODOX-M/IVAC 療法± R, あるいはR-Hyper-CVAD 療法などが推奨される。
【解 説】
BL に対してCHOP 療法などを行った際の治療成績は,長期生存が10%未満と極めて不良であった。米国National Cancer Institute のMagrath らによって,CODOX-M(CPA, VCR, DXR,MTX)/IVAC(IFM, ETP, AraC)療法の有効性と安全性が報告された1)。欧州で成人BL に対するCODOX-M/IVAC 療法の追試(LY06)が行われ,その有用性が確認された2)。減量レジメンとして,一部の薬剤を減量したmodified CODOX-M/IVAC 療法が報告され,比較的高齢の患者でも有効性が示された3)。さらに,欧州を中心としたグループから同様の減量レジメン(LY10)が報告された4)。日本でも成人患者に対するmodified CODOX-M/IVAC 療法の安全性と有効性が報告された5)。その他にはR-hyper-CVAD 療法(R, CPA, DXR, VCR, DEX)6),CALGB9251 療法7)およびR とG-CSF を併用したCALGB10002 療法8),dose-adjusted(DA)-EPOCH-R 療法(ETP,PSL, VCR, CPA, DXR, R)9)などが報告されている。これらのレジメンに関する比較試験は存在しないため,それぞれの優劣は不明である。実地診療においては,modified CODOX-M/IVAC±R 療法あるいはR-hyper-CVAD 療法などが推奨される。ただし,高齢者や合併症などでこれらの治療強度が高いレジメンの施行が困難な場合は,DA-EPOCH-R 療法が考慮される。
【参考文献】
1) Magrath I, et al. Adult and children with small non-cleaved-cell lymphoma have a similar excellent outcome when treated with the same chemotherapy regimen. J Clin Oncol. 1996 ; 14(3) : 925-34.(3iiiD)
2) Mead GM, et al. An international evaluation of CODOX-M and CODOX-M alternating with IVAC in adult Burkitt’s lymphoma : results of United Kingdom Lymphoma Group LY06 study. Ann Oncol. 2002 ; 13(8) : 1264-74.(3iiiDi)
3) LaCasce A, et al. Modified Magrath regimens for adults with Burkitt and Burkitt-like lymphomas : preserved efficacy with decreased toxicity. Leuk Lymphoma. 2004 ; 45(4) : 761-7.(3iiiD)
4) Mead GM, et al. A prospective clinicopathologic study of dose-modified CODOX-M/IVAC in patients with sporadic Burkitt lymphoma defined using cytogenetic and immunophenotypic criteria(MRC/NCRI LY10 trial). Blood. 2008 ; 112(6) : 2248-60.(3iiDiii)
5) Maruyama D, et al. Modified cyclophosphamide, vincristine, doxorubicin, and methotrexate(CODOX-M)/ifosfamide, etoposide, and cytarabine (IVAC) therapy with or without rituximab in Japanese adult patients with Burkitt lymphoma (BL) and B-cell lymphoma, unclassifiable, with features intermediate between diffuse large B-cell lymphoma and BL. Int J Hematol. 2010 ; 92(5) : 732-43.(3iiiD)
6) Thomas DA, et al. Chemoimmunotherapy with hyper-CVAD plus rituximab for the treatment of adult Burkitt and Burkitt-type lymphoma or acute lymphoblastic leukemia. Cancer. 2006 ; 106 (7) : 1569-80.(3iiiD)
7) Lee EJ, et al. Brief-duration high-intensity chemotherapy for patients with small noncleaved-cell lymphoma or FAB L3 acute lymphocytic leukemia : results of Cancer and Leukemia Group B Study 9251. J Clin Oncol. 2001 ; 19(20) : 4014-22.(3iiiDiv)
8) Rizzieri DA, et al. Efficacy and toxicity of rituximab and brief duration, high intensity chemotherapy with filgrastim support for Burkitt or Burkitt-like leukemia/lymphoma : Cancer and Leukemia Group B(CALGB)Study 10002. Blood. 2010 ; 116 : Abstract 858.(3iiiDiv)
9) Dunleavy K, et al. A prospective study of Dose-Adjusted(DA) EPOCH with rituximab in adult patients with newly diagnosed Burkitt lymphoma : A regimen with high efficacy and low toxicity. 10th International Conference on Malignant Lymphomas Abstracts. Ann Oncol 2008 ; 19(suppl 4) : iv83-4(Abstract 009).(3iiiD)
| CQ2 | BL の初回治療にリツキシマブの併用は有効か |
|---|
-
推奨グレードカテゴリー2B
- 施行するレジメンによりリツキシマブ併用の意義が異なる可能性があるが,特に強力な抗がん剤治療が施行困難な高齢患者の治療成績を改善すると考えられる。
【解 説】
BL に対するリツキシマブ(R)併用の有用性については,hyper-CVAD 療法(CPA, VCR,DXR, DEX)にR を併用した群が,hyper-CVAD 療法単独のhistorical control 群と比較して優れていたことが報告された1)。また,初発BL 患者に対するR を併用したDA-EPOCH-R 療法(ETP,DXR, CPA, VCR, PSL, R)の予備的な検討結果でも,有効性が報告されている2)。CALGB9251 レジメンにG-CSF およびR を併用したCALGB10002 試験において,CALBG9251 のhistorical control と比べて,全生存割合(OS)で優れていたことが報告された3)。また,特に高齢者においてメトトレキサート(MTX)やシタラビン(AraC)の投与量を減量してもR を併用することにより良好な治療成績が得られたと報告された4)。一方,CODOX-M(CPA, VCR, DXR, MTX)/ IVAC(IFM, ETP, AraC)療法にR を併用した報告は5)~7),いずれも後方視的かつ少数例での検討ではあるが,今のところR 併用による明らかな上乗せ効果は示されていない。逆に,R 併用による好中球回復遅延,遅発性好中球減少あるいは感染症が増加する可能性がある5)~7)。BL に対するR 併用の意義は,施行するレジメンの治療強度などにより異なる可能性がある。特に,強力な化学療法による毒性増強が懸念され,かつ,抗がん剤の減量を要する高齢患者に対しては,R を併用することにより治療成績の向上に寄与すると考えられる。
【参考文献】
1) Thomas DA, et al. Chemoimmunotherapy with hyper-CVAD plus rituximab for the treatment of adult Burkitt and Burkitt-type lymphoma or acute lymphoblastic leukemia. Cancer. 2006 ; 106 (7) : 1569-80.(3iiiD)
2) Dunleavy K, et al. A prospective study of Dose-Adjusted(DA) EPOCH with rituximab in adult patients with newly diagnosed Burkitt lymphoma : A regimen with high efficacy and low toxicity. 10th International Conference on Malignant Lymphomas Abstracts. Ann Oncol 2008 ; 19(suppl 4) : iv83-4(Abstract 009).(3iiiD)
3) Rizzieri DA, et al. Efficacy and toxicity of rituximab and brief duration, high intensity chemotherapy with filgrastim support for Burkitt or Burkitt-like leukemia/lymphoma : Cancer and Leukemia Group B(CALGB)Study 10002. Blood. 2010 ; 116 : Abstract 858.(3iiiDiv)
4) Hoelzer D, et al. High survival rate in adult Burkitt’s lymphoma/leukemia and diffuse large B-cell lymphoma with mediastinal involvement. Blood. 2007 ; 110 : Abstract 518.(3iiiD)
5) Maruyama D, et al. Modified cyclophosphamide, vincristine, doxorubicin, and methotrexate(CODOX-M)/ifosfamide, etoposide, and cytarabine (IVAC) therapy with or without rituximab in Japanese adult patients with Burkitt lymphoma (BL) and B-cell lymphoma, unclassifiable, with features intermediate between diffuse large B-cell lymphoma and BL. Int J Hematol. 2010 ; 92(5) : 732-43.(3iiiD)
6) Mohamedbhai SG, et al. Rituximab in combination with CODOX-M/IVAC : a retrospective analysis of 23 cases of non-HIV related B-cell non-Hodgkin lymphoma with proliferation index > 95%. Br J Haematol. 2011 ; 152(2) : 175-81.(3iiiD)
7) Barnes JA, et al. Evaluation of the addition of rituximab to CODOX-M/IVAC for Burkitt’s lymphoma : a retrospective analysis. Ann Oncol. 2011 ; 22(8) : 1859-64.(3iiiD)
| CQ3 | BL において腫瘍崩壊症候群の予防は必須か |
|---|
-
推奨グレードカテゴリー2A
- BL は悪性腫瘍の中で腫瘍崩壊症候群のリスクが最も高い疾患の一つであり,特に,初回化学療法施行時にはラスブリカーゼと輸液による予防が推奨される。
【解 説】
ドイツのBerlin-Frankfurt-Munster グループが行った2 つの多施設共同臨床試験に登録された小児非ホジキンリンパ腫患者1,791 人の解析では,大量補液,アロプリノールあるいはラスブリカーゼなどの予防のもと,患者全体では腫瘍崩壊症候群の発症割合は4.4%であったのに対し,BL 患者では8.4%と高率であった。さらにBL が白血化した状態[FAB 分類におけるL3,WHO 分類(2008)におけるBurkitt leukemia variant]では26.4%と最もリスクの高い病型であった。特に,LDH が500 U/L 以上の患者では発症リスクが増加した1)。これらの結果を受けて,BL は腫瘍崩壊症候群のハイリスク疾患として挙げられており,腫瘍崩壊症候群予防として大量補液とラスブリカーゼの投与が推奨されている2)。
【参考文献】
1) Wossmann W, et al. Incidence of tumor lysis syndrome in children with advanced stage Burkitt’s lymphoma/ leukemia before and after introduction of prophylactic use of urate oxidase. Ann Hematol. 2003 ; 82(3) : 160-5.(3iiiD)
2) Coiffier B, et al. Guidelines for the management of pediatric and adult tumor lysis syndrome : an evidence-based review. J Clin Oncol. 2008 ; 26(16) : 2767-78.
| CQ4 | BL に対して放射線治療は勧められるか |
|---|
-
推奨グレードカテゴリー4
- BL に対する追加的放射線治療の有用性は示されていない。また,中枢神経系浸潤予防を目的とした全脳照射は避けるべきである。
【解 説】
1986 年に,Stanford 大学のグループが18 人の成人BL を対象として,大量メトトレキサート(MTX)を含むCHOMP 療法(CPA, DXR, VCR, PSL,大量MTX)を行い,10 cm 以上のbulky mass を有する患者に対して追加照射を行った。3 人が腹部bulky mass に対して放射線照射を受けたが,うち2 人に照射野内再発を認めた1)。以降のBL に対する治療研究においては,放射線療法を含まず,化学療法の治療強度を強める方向で開発されており,現在においてもBL に対する放射線療法の有用性は示されていない。
また,CALGB9251 試験2)およびその長期追跡調査結果3)では,中枢神経系浸潤の予防として髄注と全脳照射との併用による重篤な神経毒性が問題となった。次いでリツキシマブ(R)とG-CSF を併用したCALGB10002 試験では予防的全脳照射は行われず,髄注のみが施行されたが中枢神経系再発の頻度はCALGB9251 試験と同程度(3~4%)であった。以上より,中枢神経系浸潤の予防には髄注および代謝拮抗剤(MTX やAraC)の大量投与で十分であり,予防的全脳照射は不要であると結論された4)。
【参考文献】
1) Bernstein JI, et al. Combined modality therapy for adults with small noncleaved cell lymphoma(Burkitt’s and non-Burkitt’s types). J Clin Oncol. 1986 ; 4(6) : 847-58.(3iiiD)
2) Lee EJ, et al. Brief-duration high-intensity chemotherapy for patients with small noncleaved-cell lymphoma or FAB L3 acute lymphocytic leukemia : results of Cancer and Leukemia Group B Study 9251. J Clin Oncol. 2001 ; 19(20) : 4014-22.(3iiiDiv)
3) Rizzieri DA, et al. Intensive chemotherapy with and without cranial radiation for Burkitt leukemia and lymphoma : final results of Cancer and Leukemia Group B Study 9251. Cancer. 2004 ; 100 (7) : 1438-48.(3iiiDiv)
4) Rizzieri DA, et al. Efficacy and toxicity of rituximab and brief duration, high intensity chemotherapy with filgrastim support for Burkitt or Burkitt-like leukemia/lymphoma : Cancer and Leukemia Group B(CALGB)Study 10002. Blood. 2010 ; 116 : Abstract 858.(3iiiDiv)
| CQ5 | BL に対して造血幹細胞移植は勧められるか |
|---|
-
推奨グレードカテゴリー4
- 第一寛解期における自家造血幹細胞移植併用大量化学療法(自家移植)は推奨されない。
-
推奨グレードカテゴリー2B
- 再発患者のうち救援療法に感受性を示す患者では引き続く自家移植の効果が期待できる。
-
推奨グレードカテゴリー3
- 同種造血幹細胞移植(同種移植)の有効性を示唆する十分なデータは存在しない。
【解 説】
第一寛解期における自家移植の有用性は確立されていない1)2)。European Group for Blood and Marrow Transplantation(EBMT)からの報告では,第一寛解期で自家移植を施行したBL 患者の3 年全生存割合(OS)は72%であった2)が,この成績はCQ1 に示したようなBL タイプの強力な化学療法単独による治療成績と大差がない。一方,再発患者のうち救援療法に感受性を示した患者では3 年OS が37%であったが,治療抵抗性患者では7%に過ぎなかった2)。以上より,第一寛解期での自家移植の有効性を示唆する根拠は乏しく,再発後に救援療法に感受性を示す患者では自家移植の効果が期待できる2)。また,再発後の救援療法については,初回治療に用いられるレジメン(CQ3),DHAP 療法(DEX, AraC, CDDP)2),R-ICE 療法(R, IFM, CBDCA, ETP)3),ドキソルビシン(DXR)とトポテカンの併用療法4)などが報告されているが,標準治療は存在しない。BL に対する同種移植はさらに報告が少ない。EBMT からの報告では,移植時に63%の患者が完全奏効(CR)の状態で同種移植を行っても,無増悪生存期間(PFS)および全生存期間中央値は各2.5 カ月および4.7 カ月と,効果は極めて限定的であった5)。
【参考文献】
1) Jost LM, et al. Short-term weekly chemotherapy followed by high-dose therapy with autologous bone marrow transplantation for lymphoblastic and Burkitt’s lymphomas in adult patients. Ann Oncol. 1995 ; 6(5) : 445-51.(3iiiD)
2) Sweetenham JW, et al. Adult Burkitt’s and Burkitt-like non-Hodgkin’s lymphoma--outcome for patients treated with high-dose therapy and autologous stem-cell transplantation in first remission or at relapse : results from the European Group for Blood and Marrow Transplantation. J Clin Oncol. 1996 ; 14(9) : 2465-72.(3iiA)
3) Griffin TC, et al. A study of rituximab and ifosfamide, carboplatin, and etoposide chemotherapy in children with recurrent/refractory B-cell (CD20+) non-Hodgkin lymphoma and mature B-cell acute lymphoblastic leukemia : a report from the Children’s Oncology Group. Pediatr Blood Cancer. 2009 ; 52(2) : 177-81.(3iiiDiv)
4) Smith SM, et al. Sequential doxorubicin and topotecan in relapsed/refractory aggressive non-Hodgkin’s lymphoma : Results of CALGB 59906. Leukemia Lymphoma 2006 ; 47(8) : 1511-7.(3iiiD)
5) Peniket AJ, et al. An EBMT registry matched study of allogeneic stem cell transplants for lymphoma : allogeneic transplantation is associated with a lower relapse rate but a higher procedure-related mortality rate than autologous transplantation. Bone Marrow Transplant. 2003 ; 31(8) : 667-78.(3iiA)
| CQ6 | Intermediate DLBCL/BL に対する治療は何が勧められるか |
|---|
-
推奨グレードカテゴリー3
- 現時点では,DLBCL,BL いずれかの治療を用いるかは推奨できないが,BL に準じた治療選択が妥当と考えられる。
【解 説】
Intermediate DLBCL/BL はWHO 分類(2008)に記載された,多様な集団を含む暫定的な疾患群であり,従来Burkitt-like lymphoma(BLL)と診断されていた集団の多くが含まれる。本疾患群に対する標準治療を一概に論ずることは困難であるが,BLL はhighly aggressive な経過をとり,CHOP 療法(CPA, DXR, VCR, PSL)などのDLBCL タイプの化学療法による予後は不良で,BL タイプの化学療法が有効であったとの報告がある1)2)。また,BL タイプの化学療法に関するいくつかの報告3)~6)では, 対象患者にBL だけでなくBLL が含まれている。したがって,Intermediate DLBCL/BL に対して,現時点ではBL に準じた治療選択が妥当であろう。ただ,Intermediate DLBCL/BL の中に,MYC 転座およびBCL2 転座をともに有する場合があり,BL タイプの化学療法を行ったとしても生存期間中央値は2.4~18 カ月と極めて予後不良であることが報告されている7)。
【参考文献】
1) Smeland S, et al. Treatment of Burkitt’s/Burkitt-like lymphoma in adolescents and adults : a 20-year experience from the Norwegian Radium Hospital with the use of three successive regimens. Ann Oncol. 2004 ; 15(7) : 1072-8.(3iiiDiii)
2) Nomura Y, et al. High-grade mature B-cell lymphoma with Burkitt-like morphology : results of a clinicopathological study of 72 Japanese patients. Cancer Sci. 2008 ; 99(2) : 246-52.(3iiiD)
3) Magrath I, et al. Adult and children with small non-cleaved-cell lymphoma have a similar excellent outcome when treated with the same chemotherapy regimen. J Clin Oncol. 1996 ; 14(3) : 925-34.(3iiiD)
4) Thomas DA, et al. Chemoimmunotherapy with hyper-CVAD plus rituximab for the treatment of adult Burkitt and Burkitt-type lymphoma or acute lymphoblastic leukemia. Cancer. 2006 ; 106 (7) : 1569-80.(3iiiD)
5) Maruyama D, et al. Modified cyclophosphamide, vincristine, doxorubicin, and methotrexate(CODOX-M)/ifosfamide, etoposide, and cytarabine (IVAC) therapy with or without rituximab in Japanese adult patients with Burkitt lymphoma (BL) and B-cell lymphoma, unclassifiable, with features intermediate between diffuse large B-cell lymphoma and BL. Int J Hematol. 2010 ; 92(5) : 732-43.(3iiiD)
6) Lee EJ, et al. Brief-duration high-intensity chemotherapy for patients with small noncleaved-cell lymphoma or FAB L3 acute lymphocytic leukemia : results of Cancer and Leukemia Group B Study 9251. J Clin Oncol. 2001 ; 19(20) : 4014-22.(3iiiDiv)
7) Johnson NA, et al. Lymphomas with concurrent BCL2 and MYC translocations : the critical factors associated with survival. Blood. 2009 ; 114(11) : 2273-9.(3iiiD)
7
末梢性T リンパ腫
(peripheral T-cell lymphoma:PTCL)
(peripheral T-cell lymphoma:PTCL)
◆総論
WHO 分類(2008)では約20 のPTCL およびNK 細胞腫瘍の疾患単位が掲載されている1)。成熟T/NK 細胞腫瘍では,世界の各地域間で病型相対頻度が異なることが知られている。International T-Cell Lymphoma Project として約1,300 例を対象として行われた多国間共同後方視的研究によると,欧米で頻度の高いPTCL 病型は頻度が高いものから順に,PTCL,非特定型(PTCL, not otherwise specified:PTCL-NOS),血管免疫芽球性T 細胞リンパ腫(angioimmunoblastic Tcell lymphoma:AITL),未分化大細胞リンパ腫(anaplastic large cell lymphoma:ALCL),ALK陽性とALCL, ALK 陰性となる2)。本項では上述の4 病型について取り扱い,わが国で頻度の高い成人T 細胞白血病・リンパ腫(adult T-cell leukemia-lymphoma:ATL)と節外性NK/T 細胞リンパ腫,鼻型(extranodal NK/T-cell lymphoma, nasal type:ENKL)については別項で取り扱う。皮膚T 細胞リンパ腫(CTCL)に関しては,皮膚悪性腫瘍診療ガイドラインⅡ:皮膚リンパ腫 第1 版3)が作成されている。
PTCL における病期分類は,ほかの非ホジキンリンパ腫と同様にAnn Arbor 分類が用いられる。予後予測モデルとしては国際予後指標(International Prognostic Index:IPI)が有用であり2),PTCL-NOS に関してはイタリアの研究グループから提唱された病型特異的予後予測モデルであるPIT(Prognostic Index for PTCL-U)がある。PIT では,年齢>60 歳,Performance Status(PS)>1,血清LDH 値>施設基準値上限,骨髄浸潤陽性の4 つが予後不良因子として規定されている4)。
PTCL に対する効果判定規準としては,主に国際ワークショップ規準5)が用いられている。改訂国際ワークショップ規準6)では効果判定にpositron emission tomography(PET)実施が組み込まれており,PTCL でも日常診療での導入が進みつつある。
補足:International T-Cell Lymphoma Project において全T/NK 細胞腫瘍に占める頻度が5%未満と報告された稀なPTCL 病型として, 腸管症関連T 細胞リンパ腫(enteropathy-associated T-cell lymphoma : EATL),肝脾T 細胞リンパ腫(hepatosplenic T-cell lymphoma : HSTL),原発性皮膚ALCL,皮下脂肪織炎様T 細胞リンパ腫が挙げられる2)。EATL はCeliac 病の頻度の高い欧州では全悪性リンパ腫の9.1%を占め,北米でも5.8%を占めるもののアジアでは1.9%と頻度が低い7)。
HSTL は細胞傷害性T 細胞,通常はγδ型T 細胞に由来する腫瘍で,若年男性に多く,著明な肝脾腫を特徴とする1)。EATL, HSTL ともにCHOP(類似)療法による予後は不良であり,病型特異的治療は未確立である。その他の2 病型は皮膚/皮下組織を主な病変部位とするリンパ腫である。
【参考文献】
1) Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008.
2) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study : pathology findings and clinical outcomes. J Clin Oncol. 2008 ; 26(25) : 4124-30.(3iiA)
3) 科学的根拠に基づく皮膚悪性腫瘍診療ガイドラインⅡ:皮膚リンパ腫第1 版.日本皮膚科学会/日本皮膚悪性腫瘍学会編,金原出版,東京,2010.(ガイドライン)
4) Gallamini A, et al. Peripheral T-cell lymphoma unspecified (PTCL-U) : a new prognostic model from a retrospective multicentric clinical study. Blood. 2004 ; 103(7) : 2474-9.(3iiA)
5) Cheson BD, et al. Report of an International Workshop to standardize response criteria for non-Hodgkin’s lymphomas. J Clin Oncol. 1999 ; 17(4) : 1244-53.
6) Cheson BD, et al. Revised response criteria for malignant lymphoma. J Clin Oncol. 2007 ; 25(5) : 579-86.
7) Delabie J, et al. Enteropathy-associated T-cell lymphoma : clinical and histological findings from the International Peripheral T-Cell Lymphoma Project. Blood. 2011 ; 118(1) : 148-55.
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
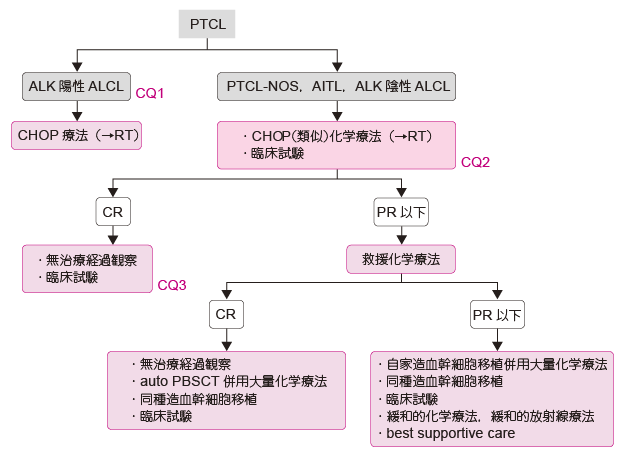
PTCL(本項では総論で指定した4 病型について取り扱う)は無治療で月単位の病勢進行を示すアグレッシブ リンパ腫(中悪性度リンパ腫)に分類され,リツキシマブ(R)導入以前は,アグレッシブ リンパ腫の約80%を占めるびまん性大細胞型B 細胞リンパ腫(diffuse large B-cell lymphoma:DLBCL)とともに病態研究と治療開発がなされ,PTCL の標準治療は他のアグレッシブ リンパ腫と同様とみなされてきた。
R 導入以前にREAL 分類の臨床的有用性の評価を試みた国際共同後方視的研究において, ALCL を除く全PTCL の予後がDLBCL より不良であることが指摘された1)。また,主にCHOP(類似)療法が実施された患者集団におけるPTCL 病型間の予後比較において,PTCL-NOS とAITL の予後はほぼ同様であり,ALCL のうちALK 陽性例の予後が特に良好であることが判明した2)。以上の背景から現在では,ALK 陽性ALCL とそれ以外のPTCL との2 群に分けて治療方針が決定されている。
ALK 陽性ALCL では,DLBCL に匹敵する治療成績が得られているCHOP 療法[限局期ではinvolved-field radiotherapy(IFRT)を追加]が推奨される(CQ1)。PTCL-NOS, AITL, ALK 陰性ALCL においても,治療実績が最も多く報告されているCHOP 療法などの多剤併用化学療法が推奨される(CQ2)。ただしその治療効果は不十分であり,標準治療レジメンは確定しておらず,臨床試験への参加が推奨される(CQ2)。初発進行期PTCL の初回完全奏効(CR)例における自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)追加の意義は不明であり,一般診療として行うことは推奨されず,臨床試験として実施することが望ましい(CQ3)。初回治療後部分奏効(PR)以下の場合の治療選択に関するエビデンスは乏しく,現在新規化学療法レジメン,新規薬剤,HDC/AHSCT,同種造血幹細胞移植(allogeneic hematopoietic stem cell transplantation : allo-HSCT)の臨床試験が進行中である。
【第1.1 版追記コメント】
新規治療薬のうち抗CD30 antibody-drug conjugateであるブレンツキシマブベドチンに関しては,米国および国内での臨床試験3,4)の結果に基づいて,再発または難治性のCD30 陽性ALCL に対する国内承認が2014 年1 月に取得された。また抗CCR4 抗体 モガムリズマブについては,国内第Ⅱ相試験5)の結果に基づいて,世界に先駆けて2014 年3 月に、再発または難治性のCCR4 陽性のPTCL および皮膚T細胞リンパ腫に対する効能追加承認がなされた。
参考文献
1) A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin’s lymphoma. The Non-Hodgkin’s Lymphoma Classification Project. Blood. 1997 ; 89(11) : 3909-18.(3iiA)
2) Savage KJ, et al. ALK- anaplastic large-cell lymphoma is clinically and immunophenotypically different from both ALK+ALCL and peripheral T-cell lymphoma, not otherwise specified : report from the International Peripheral T-Cell Lymphoma Project. Blood. 2008 ; 111(12) : 5496-504.(3iiA)
【第1.1版追記】
3) Pro B, et al. Brentuximab vedotin (SGN-35) in patients with relapsed or refractory systemic anaplastic large-cell lymphoma: results of a phase II study. J Clin Oncol. 2012;30(18):2190-6.(3iiiDiv)
4) Ogura M, et al. Phase I / II study of brentuximab vedotin in Japanese patients with relapsed or refractory CD30-positive Hodgkin's lymphoma or systemic anaplastic large-cell lymphoma. Cancer Sci. 2014;105(7):840-6.(3iiiDiv)
5) Ogura M, et al. Multicenter phase II study of mogamulizumab (KW-0761), a defucosylated anti-cc chemokine receptor 4 antibody, in patients with relapsed peripheral T-cell lymphoma and cutaneous T-cell lymphoma. J Clin Oncol. 2014;32(11):1157-63.(3iiiDiv)
| CQ1 | 初発ALK 陽性ALCL に対する最適の治療は何か |
|---|
-
推奨グレードカテゴリー2A
- 初発ALK 陽性ALCL ではCHOP 療法(限局期ではIFRT を追加)が推奨される。
【解 説】
ALK 陽性ALCL は,ALK 陰性ALCL より若年者に多く,節外病変数2 以上の患者割合が高い1)。1999 年に報告された北米2 施設共同の後方視的研究により,ALK 陽性ALCL では従来のアグレッシブ リンパ腫に対する標準治療であるCHOP 療法(CPA, DXR, VCR, PSL)あるいはその類似療法[限局期ではinvolved-field radiotherapy(IFRT)を追加]による良好な治療成績が報告されている1)。全PTCL の中でCHOP 療法あるいはその類似療法(限局期ではIFRT 追加)により最良の治療効果が得られることがその後の複数の後方視的解析の結果から示されており2)3),初回治療として推奨される。
【参考文献】
1) Gascoyne RD, et al. Prognostic significance of anaplastic lymphoma kinase (ALK) protein expression in adults with anaplastic large cell lymphoma. Blood. 1999 ; 93(11) : 3913-21.(3iiA)
2) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study : pathology findings and clinical outcomes. J Clin Oncol. 2008 ; 26(25) : 4124-30.(3iiA)
3) Savage KJ, et al. ALK- anaplastic large-cell lymphoma is clinically and immunophenotypically different from both ALK+ALCL and peripheral T-cell lymphoma, not otherwise specified : report from the International Peripheral T-Cell Lymphoma Project. Blood. 2008 ; 111(12) : 5496-504.(3iiA)
| CQ2 | 初発PTCL-NOS, AITL, ALK 陰性ALCL に対する最適の初回治療は何か |
|---|
-
推奨グレードカテゴリー2A
- CHOP 療法などの多剤併用化学療法による治療実績が最も多く,推奨される。ただし,標準治療レジメンは確定しておらず,臨床試験参加が推奨される。
【解 説】
PTCL はアグレッシブ リンパ腫の10~15%を占める。米国での大規模ランダム化比較試験1)においてCHOP 療法(CPA, DXR, VCR, PSL)がアグレッシブ リンパ腫に対する標準治療に位置づけられたことを受けて,PTCL の標準治療もCHOP 療法であるとみなされ,国内外の日常診療で広く行われてきた。
その後,国内外での複数の後方視的研究により,PTCL はDLBCL を代表とするアグレッシブB 細胞リンパ腫と比較して,CHOP またはその類似療法による治療成績が有意に不良であることが明らかにされた2)~4)。さらに,PTCL の中でもALK 陽性ALCL はCHOP(類似)療法で良好な治療成績が得られることが明らかにされた(CQ1)。
PTCL は稀な疾患の集合体であり,各病型の初発例を対象とした前方視的臨床試験は極めて少ない。このため,初発PTCL-NOS, AITL, ALK 陰性ALCL における標準治療は未確立であり,CHOP 療法などの多剤併用化学療法がこれまでの治療実績から推奨される。他のアグレッシブ リンパ腫に準じて化学療法後にIFRT を追加することがあるが,その適応に関する明確なエビデンスはない。既存薬剤の新しい組み合わせによる新規併用化学療法,および種々の新規薬剤を含む化学療法の臨床試験が国内外で進行中であり,標準治療が未確立であることから,臨床試験への参加が推奨される。
【参考文献】
1) Fisher RI, et al. Comparison of a standard regimen(CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma. N Engl J Med. 1993 ; 328(14) : 1002-6.(1iiA)
2) A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin’s lymphoma. The Non-Hodgkin’s Lymphoma Classification Project. Blood. 1997 ; 89(11) : 3909-18.(3iiA)
3) Gisselbrecht C, et al. Prognostic significance of T-cell phenotype in aggressive non-Hodgkin’s lymphomas. Groupe d’Etudes des Lymphomes de l’Adulte(GELA). Blood. 1998 ; 92(1) : 76-82.(3iiA)
4) Watanabe T, et al. Pretreatment serum total protein is a significant prognostic factor to predict outcome of peripheral T/NK-cell lymphoma patients. Leuk Lymphoma. 2010 ; 51(5) : 813-21.(3iiA)
| CQ3 | 初発進行期PTCL-NOS, AITL, ALK 陰性ALCL の化学療法後CR 例において地固め療法としての自家造血幹細胞移植併用大量化学療法は必要か |
|---|
-
推奨グレードカテゴリー2A
- 初発進行期PTCL-NOS, AITL, ALK 陰性ALCL の初回完全奏効例における自家造血幹細胞移植併用大量化学療法は,一般診療として行うことは勧められない。臨床試験として実施することが望ましい。
【解 説】
初発進行期PTCL-NOS, AITL, ALK 陰性ALCL の予後は不良であり,5 年全生存割合(OS)はいずれも50%未満である1)。初回完全奏効(complete response : CR)での自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)が検討されており,良好な治療成績を報告している後方視的研究が複数存在する。これを受けて,欧米でいくつかの第Ⅱ相試験が行われた。スペインから3 年OS 73% 2)と良好な治療効果が報告された一方で,他の試験での3~5 年OS は50%程度であり3)4),化学療法単独と比較して著明な改善が示されたとは結論されていない。ランダム化比較試験の結果報告はないため,現時点での評価は困難である。以上より初発進行期PTCL の初回CR 例でのHDC/AHSCT は,一般診療として行うことは推奨されず,臨床試験として実施することが望ましい。
【参考文献】
1) Vose J, et al. International peripheral T-cell and natural killer/T-cell lymphoma study : pathology findings and clinical outcomes. J Clin Oncol. 2008 ; 26(25) : 4124-30.(3iiA)
2) Rodriguez J, et al. Frontline autologous stem cell transplantation in high-risk peripheral T-cell lymphoma : a prospective study from The Gel-Tamo Study Group. Eur J Haematol. 2007 ; 79(1) : 32-8.(3iiiA)
3) Reimer P, et al. Autologous stem-cell transplantation as first-line therapy in peripheral T-cell lymphomas : results of a prospective multicenter study. J Clin Oncol. 2009 ; 27(1) : 106-13.(3iiiA)
4) d’Amore F, et al. Up-front autologous stem-cell transplantation in peripheral T-cell lymphoma : NLGT-01. J Clin Oncol. 2012 ; 30(25) : 3093-9.(3iiiA)
8
成人T 細胞白血病・リンパ腫
(adult T-cell leukemia-lymphoma:ATL)
(adult T-cell leukemia-lymphoma:ATL)
◆総論
成人T 細胞白血病・リンパ腫(adult T-cell leukemia-lymphoma:ATL)は,九州・沖縄地方を主とする西南日本に多発するT 細胞腫瘍として,1977 年内山,高月らによって提唱された疾患概念である1)。1980 年代のはじめには原因ウイルスとしてhuman T-lymphotropic virus type-I(HTLV-1)が発見された2)~5)。WHO 分類(2008)においてATL は,高度の核異型を伴ったリンパ球よりなる,HTLV-1 によって引き起こされる末梢性T 細胞腫瘍と定義されている6)。
Flower cell と呼ばれる異常リンパ球の増多を主体とした白血球増多,リンパ節腫脹,皮膚病変,ATL 細胞の浸潤による多臓器障害,高LDH 血症,高Ca 血症,日和見感染症などが出現する。日本以外では中央アフリカおよび中南米出身者に比較的高頻度に発生している。HTLV-1 キャリアは現在日本には西南日本沿岸部を主に110 万人程度存在し,キャリアからATL の発症率は年間1,000 人に0.6~0.7 人とされる7)8)。HTLV-1 の感染は感染細胞が正常リンパ球に直接接触して成立する。感染経路として輸血,性交,母乳が知られているが,ATL 発症につながる重要な感染経路は母乳である。いくつかの多発地域ではHTLV-1 母子感染予防対策が行われており,6 カ月以上の長期授乳による母子感染率は20.5%であるのに対して人工栄養による母子感染率は2.4%と報告されている9)。
ATL 発症は20 歳代までは極めて稀で,その後増加し,60 歳頃をピークにして以降徐々に減少する。1 人のHTLV-1 キャリアが,生涯でATL を発症する確率は約5%である。HTLV-1 キャリアにおけるATL 発症の危険因子としては,多変量解析で,母子感染,高齢者,末梢血中の高ウイルス量,ATL の家族歴あり,他の疾患の治療中に初めて抗HTLV-1 抗体検査を受け陽性が判明した症例10)が報告されている。近年,HTLV-1 キャリアとATL 患者の高齢化が進んでいる11)12)。
1991 年にJapan Clinical Oncology Group(JCOG)リンパ腫グループ(LSG)による813 例のATL 患者の全国実態調査をもとに, 多変量解析による予後因子として, 年齢, 全身状態(performance status:PS),総病変数,高Ca 血症,高LDH 血症が同定された13)~16)。そして予後因子解析と臨床病態の特徴から「急性型」,「リンパ腫型」,「慢性型」,「くすぶり型」の4 臨床病型分類が提唱されている17)(表1)。これらの割合は急性型57%,リンパ腫型24%,慢性型19%,くすぶり型6%であった。急性型,リンパ腫型,予後不良因子(LDH,アルブミン,BUN のいずれか1 つ以上が異常値)を持つ慢性型ATL は急速な経過をたどることがほとんどであり,それぞれの生存期間中央値(MST)は6 カ月,10 カ月,15 カ月であることから一括してアグレッシブATL と呼ばれる。一方くすぶり型および予後不良因子を有していない慢性型ATL は比較的緩徐な経過を辿り,それぞれの4 年生存割合は約63%と約70%である18)ことから,インドレントATL と呼ばれる。
JCOG-LSG がアグレッシブATL を対象とし,継続して臨床試験を行ってきたことから,化学療法における反応性の評価では,JCOG 治療効果判定規準が広く使用されてきた14)19)。近年では非ホジキンリンパ腫と慢性リンパ性白血病に対するもの20)21)をもとに改変した修正版ATL に対するJCOG 治療効果判定規準22)が用いられている(表2)。
| 評価項目 | くすぶり型 | 慢性型*1 | リンパ腫型*1 | 急性型*1 | |
|---|---|---|---|---|---|
| 抗HTLV-1 抗体*2 | + | + | + | + | |
| リンパ球数(×103/mm3)*3 | < 4 | ≧ 4 | < 4 | ||
| 異常リンパ球数*4 | ≧ 5%*7 | +*8 | ≦ 1% | +*8 | |
| Flower cell | *5 | *5 | no | + | |
| LDH | ≦1.5N | ≦2N | |||
| 補正Ca 値(mg/dL)*6 | <11.0 | <11.0 | |||
| 組織学的に腫瘍病変が確認されたリンパ節腫大 | No | + | |||
| 腫瘍病変 | 皮膚 | *7 | |||
| 肺 | *7 | ||||
| リンパ節 | no | yes | |||
| 肝腫大 | no | ||||
| 脾腫大 | no | ||||
| 中枢神経 | no | no | |||
| 骨 | no | no | |||
| 胸水 | no | no | |||
| 腹水 | no | no | |||
| 消化管 | no | no | |||
空欄は他の病型で規定される条件以外の制約はないことを示す。
N:正常値上限
*1 予後不良因子を有する慢性型:BUN>施設基準値上限,LDH>施設基準値上限,血清アルブミン<施設基準値下限の1 つでも満たす場合
*2 PA 法あるいはELISA 法やWestern blot 法のいずれかで陽性であること。
Immunofluorescence 法やWestern blot 法により,陽性反応が確認されていることが望ましい。測定可能な施設では,Southern blot 法により,HTLV-1 provirus のATL 細胞への組み込みを確認する。
*3 正常リンパ球と異常リンパ球を含むリンパ球様細胞の実数の和
*4 形態学的に明らかなATL 細胞
*5 ATL に特徴的なflower cell が認められてもよい。
*6 補正Ca 値は以下の式で求める。
血清アルブミン値≧4.0(g/dL)の場合:補正カルシウム値(mg/dL)=総カルシウム値(mg/dL)
血清アルブミン値<4.0(g/dL)の場合:補正カルシウム値(mg/dL)=総カルシウム値(mg/dL)-0.8[アルブミン(g/dL)-4]
*7 末梢血中の異常リンパ球が5%未満でくすぶり型と診断されるには,皮膚あるいは肺に組織学的に腫瘍病変が確認されることが必要である。
*8 末梢血中の異常リンパ球が5%未満で慢性型または急性型と診断されるには,組織学的に腫瘍病変が確認されることが必要である。
| 総合効果 | 評価項目 | |||||||
|---|---|---|---|---|---|---|---|---|
| 標的病変 | 非標的病変 | 骨髄浸潤 | 末梢血病変 (異常リンパ球) |
皮膚病変 | 新病変 | |||
| 節性 | 節外性 | 節性 | 節外性 | |||||
| CR | 正常 | 消失 | 正常 | 消失 | 陰性 | 正常 | 正常 | なし |
| PR | SPD の50%以上の縮小 | 正常 or 非増大 |
消失 or 非増大 |
問わない (未検可) |
正常 or 減少 |
正常 or 縮小 |
なし | |
| SD | CR,PR,PD のいずれにも判定されない | |||||||
| PD | 以下のいずれか1 項目でも満たした場合にPD と判定する | |||||||
| SPD の50%以上の増大 or 節性標的病変の再腫大 or 節外性標的病変の再出現 |
増大 or 再腫大 |
増大 or 再出現 |
陽性化 | 増加 | 増大 or 再出現 |
あり | ||
上記の項目のいずれかでも評価不能であれば総合評価は「評価不能not evaluable(NE)」とする。
| 総合効果 | 評価項目 | |||||
|---|---|---|---|---|---|---|
| 非標的病変 | 骨髄浸潤 | 末梢血病変 (異常リンパ球) |
皮膚病変 | 新病変 | ||
| CR | 正常 | 消失 | 陰性 | 正常 | 正常 | なし |
| PR* | 正常 or 非増大 |
消失 or 非増大 |
問わない (未検可) |
正常 or 減少 |
正常 or 縮小 |
なし |
| SD | CR,PR,PD のいずれにも判定されない | |||||
| PD | 以下のいずれか1 項目でも満たした場合にPD と判定する | |||||
| 増大 or 再腫大 |
増大 or 再出現 |
陽性化 | 増加 | 増大 or 再出現 |
あり | |
上記の項目のいずれかでも評価不能であれば総合評価は「評価不能not evaluable(NE)」とする。
*CR の規準を満たす場合,総合効果はCR とする。
【参考文献】
1) Uchiyama T, et al : Adult T-cell leukemia : clinical and hematologic features of 16 cases. Blood. 1977 ; 50(3): 481-92.
2) Poiesz BJ, et al. Detection and isolation of type C retrovirus particles from fresh and cultured lymphocytes of a patient with cutaneous T-cell lymphoma. Proc Natl Acad Sci USA. 1980 ; 77(12) : 7415-9.
3) Hinuma Y, et al : Adult T-cell leukemia : antigen in an ATL cell line and detection of antibodies to the antigen in human sera. Proc Natl Acad Sci USA. 1981 ; 78(10) : 6476-80.
4) Yoshida M, et al ; Monoclonal integration of human T-cell leukemia provirus in all primary tumors of adult T-cell leukemia suggests causative role of human T-cell leukemia virus in the disease. Proc Natl Acad Sci USA. 1984 ; 81(8) : 2534-7.
5) Miyoshi I, et al : Type C virus particles in a cord T-cell line derived by co-cultivating normal human cord leukocytes and human leukaemic T cells. Nature. 1981 ; 294(5843) : 770-1.
6) Oshima K, et al. Adult T-cell leukaemia/lymphoma. Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008 : pp281-4.
7) Tajima K : Epidemiology of HTLV-Ⅰ/Ⅱ in Japan and the world. Gann Monograph on Cancer Research 1992 ; 39 ; 129-49.
8) Blattner WA, et al : Epidemiology of HTLV-Ⅰ and HTLV-Ⅱ infection. In : Takatsuki K, ed. Adult T-cell Leukemia. New York, NY : Oxford University Press ; 1994 : 45-90.
9) 長崎県ATL ウイルス母子感染防止研究協力事業連絡協議会編:長崎県ATL ウイルス母子感染防止研究協力事業報告書.1998 年3 月
10) Iwanaga M, et al : Human T-cell leukemia virus typeⅠ(HTLV-1) proviral load and disease progression in asymptomatic HTLV-1 carriers : a nationwide prospective study in Japan. Blood. 2010 ; 116(8) : 1211-9.
11) Satake M, et al : Current prevalence of HTLV-1 in Japan as determined by screening of blood donors. J Med Virol. 2012 ; 84(2) : 327-35.
12) Yamada Y, et al : Nationwide survey of adult T-cell leukemia/lymphoma (ATL) in Japan. Rinsho Ketsueki. 2011 ; 52(11) : 1765-71.
13) Lymphoma Study Group : Major prognostic factors of patients with adult T-cell leukemia-lymphoma : a cooperative study. Leuk Res. 1991 ; 15(2-3) : 81-90.
14) Takatsuki K : Adult T-cell leukemia. New York, NY, Oxford University Press, 1994.
15) Tobinai K, et al : Adult T-cell leukemia-lymphoma, in Abeloff MD, et al, editors. Clinical Oncology(ed 3). Philadelphia, PA, Elsevier Churchill Livingstone, 2004, pp3109-30.
16) International Agency for Research on Cancer Working Group on the Evaluation of Carcinogenic Risks to Humans : Human immunodeficiency viruses and human T-cell lymphotropic viruses. International Agency for Research on Cancer Monographs on the Evaluation of Carcinogenic Risks to Humans. http://monographs.iarc.fr/ENG/Monographs/vol67/mono67.pdf
17) Shimoyama M and members of the Lymphoma Study Group(1984-1987) : Diagnostic criteria and classification clinical subtypes of adult T-cell leukemia-lymphoma. Br J Haematol. 1991 ; 79(3) : 428-37.
18) 山田恭暉ほか:第421 回日本臨床血液学会,シンポジウム5.悪性リンパ腫の治療戦略 高悪性度リンパ腫(成人T 細胞白血病).臨床血液.2001 ; 42(4) ; 293-8.(3iiiA)
19) Tsukasaki K, et al : VCAP-AMP-VECP compared with biweekly CHOP for adult T-cell leukemia-lymphoma : Japan Clinical Oncology Group Study JCOG9801. J Clin Oncol. 2007 ; 25(34) : 5458-64.(1iiA)
20) Cheson BD, et al. Report of an International Workshop to standardize response criteria for non-Hodgkin’s lymphomas. J Clin Oncol. 1999 ; 17(4) : 1244.
21) Cheson BD, et al : National Cancer Institute-sponsored Working Group guidelines for chronic lymphocytic leukemia : revised guideline for diagnosis and treatiment. Blood. 1996 ; 87(12) : 4990-7.(ガイドライン)
22) Tsukasaki K, et al : Definition, prognostic factors, treatment, and response criteria of adult T-cell leukemia-lymphoma : a proposal from an international consensus meeting. J Clin Oncol. 2009 ; 27(3) : 453-9.
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
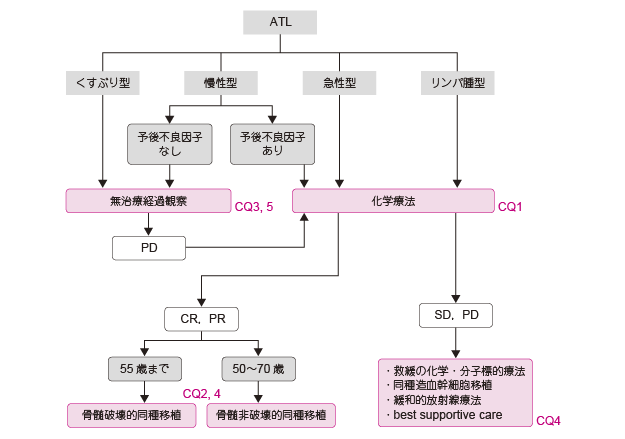
急性型,リンパ腫型,予後不良因子(LDH,アルブミン,BUN いずれか一つ以上が異常値)をもつ慢性型,すなわちアグレッシブATL に対しては多剤併用化学療法を施行する(CQ1)。そして治療反応性が得られ,年齢・全身状態・主要臓器機能に問題がなく,適切なドナーが見つかった場合は同種造血幹細胞移植(allogeneic hematopoietic stem cell transplantation : allo-HSCT,同種移植)を検討する(CQ2, CQ4)。
くすぶり型,予後不良因子を有していない慢性型,すなわちインドレントATL に対してはアグレッシブATL へ進展するまで無治療経過観察する(CQ3, CQ5)。増悪した後は初発のアグレッシブATL と同様に治療する。
| CQ1 | 初発アグレッシブATL に対して最も推奨される治療法は何か |
|---|
-
推奨グレードカテゴリー1
- VCAP-AMP-VECP 療法が最も推奨される。
【解 説】
1970 年代から1980 年代にかけて,JCOG-LSG による臨床試験ではATL に対し非ホジキンリンパ腫と同様の化学療法が行われ,そのMST は約8 ヵ月と極めて予後不良であった1)~3)。1991 年JCOG-LSG よりATL の臨床病型分類が提唱された後,アグレッシブATL を対象とした臨床試験が継続的に行われてきた。まず1991 年から,単剤で再発・再燃ATL に対して治療反応性がみられた4)ペントスタチンを組み入れた化学療法の第Ⅱ相試験が行われたが,従来の治療成績を上回らなかった5)。1994 年から行われた8 つの抗がん剤を用い,G-CSF を用いて治療強度を高め,メトトレキサート(MTX)とプレドニゾロン(PSL)の髄注を併用したLSG15 療法の第Ⅱ相試験では,それまでのATL の治療成績と比較して良好な成績が得られた6)。そして1998 年からVCAP(VCR, CPA, DXR, PSL)-AMP(DXR, MCNU, PSL)-VECP(VDS, ETP, CBDCA, PSL)(modified LSG15)療法と,非ホジキンリンパ腫の標準治療の一つと当時みなされていたCHOP-14 療法とを比較する第Ⅲ相試験(JCOG9801)が行われ,VCAP-AMP-VECP 療法は血液毒性は高いもののCHOP-14 療法よりも完全奏効割合と全生存割合に優れており,ATL に対する標準治療と考えられる7)。ただ,この臨床試験は70 歳未満を対象としたため,高齢者への適用の可能性に関しては不明である。
【参考文献】
1) Shimoyama M, et al. Chemotherapeutic results and prognostic factors of patients with advanced non-Hodgkin’s lymphoma treated with VEPA or VEPA-M. J Clin Oncol. 1988 ; 6(1) : 128-41.(2A)
2) Shimoyama M, et al. Major prognostic factors of adult patients with advanced T-cell lymphoma/leukemia. J Clin Oncol. 1988 ; 6(7) : 1088-97.(2A)
3) Tsukasaki K, et al. Lymphoma study group of JCOG. Jpn J Clin Oncol. 2012 ; 42(2) : 85-95.(2A)
4) Tobinai K, et al. Phase I study of YK-176 (2’-deoxycoformycin) in patients with adult T-cell leukemialymphoma : the DCF Study Group. Jpn J Clin Oncol. 1992 ; 22(3) : 164-71.(3iiiDiv)
5) Tsukasaki K, et al. Deoxycoformycin-containing combination chemotherapy for adult T-cell leukemialymphoma : Japan Clinical Oncology Group Study (JCOG9109). Int J Hematol. 2003 ; 77 (2) : 164-70.(3iiiDiv)
6) Yamada Y, et al. A new G-CSF-supported combination chemotherapy, LSG15, for adult T-cell leukemialymphoma : Japan Clinical Oncology Group Study 9303. Br J Haematol. 2001 ; 113(2) : 375-82.(3iiiDiv)
7) Tsukasaki K, et al. VCAP-AMP-VECP compared with biweekly CHOP for adult T-cell leukemia-lymphoma : Japan Clinical Oncology Group Study JCOG9801. J Clin Oncol. 2007 ; 25(34) : 5458-64.(1iiA)
| CQ2 | アグレッシブATL に対する同種造血幹細胞移植は有用か |
|---|
-
推奨グレードカテゴリー2A
- ATL に対する初回治療に反応性がみられた症例に対しては,HLA 一致血縁,非血縁ドナーが得られた場合,同種造血幹細胞移植は長期生存が期待できる治療法として推奨される。
【解 説】
ATL に対する同種造血幹細胞移植(allogeneic hematopoietic stem cell transplantation : allo-HSCT)は,自家造血幹細胞移植併用大量化学療法では再発が極めて高率であるのに対し,当初単施設からの少数例の報告で化学療法では得難い長期生存例が確認された。その後に多施設後方視的解析の結果から,1 年全生存割合(OS)50~52%,3 年OS が45%と有望な成績が報告された1)~4)。そして大規模な後方視的調査として日本のデータベースを基に,allo-HSCT が施行されたATL 386 例の3 年OS が33%と報告された5)。
これらはallo-HSCT を施行し得たという選択された一群に対してではあるが,化学療法単独と比較して有望な治療成績である。移植片対宿主病(graft-versus-host disease:GVHD)合併症例において再発率が低いこと,移植後再発例において免疫抑制剤の減量・中止により再寛解に到達した症例があることなどから,移植片対ATL(graft-versus-ATL : GvATL)効果が有望な治療成績の要因の一つと考えられる。ATL に対する初回治療後に治療反応性がみられた症例には,HLA 一致血縁ドナー,非血縁ドナーが得られた場合,allo-HSCT は長期生存,さらには治癒が期待できる治療法として推奨される。ただしいずれの報告でもGVHD,感染症などによる高い治療関連死亡(TRM)が示されており,化学療法後に長期奏効が得られる場合も稀にはあるため,患者へは十分な情報の提供が必要である。
allo-HSCT で骨髄破壊的前処置もしくは骨髄非破壊的前処置のいずれを選択するかについて明確なデータはないが,年齢で分けることが一般的である。骨髄破壊的前処置の対象年齢の上限は55 歳,そして骨髄非破壊的前処置は50~70 歳(非血縁の場合は65 歳まで)を対象とすることが実臨床と臨床試験では行われている6)~8)。近年,血縁HTLV-1 キャリアドナーからのallo-HSCT 施行後に,ドナーHTLV-1 感染細胞由来の再発例が報告された9)。その後,日本造血細胞移植学会から,血縁キャリアをドナーとする場合には末梢血を用いたHTLV-1 のサザンブロット解析でモノクローナル/オリゴクローナルでないこと,臨床的にATL くすぶり型でなくHTLV-1 キャリアに留まることを確認することが推奨されている10)。
ATL に対するallo-HSCT は,化学療法では得難い長期生存例が観察されており有効な治療法と言える。しかし,ドナーの選択,前処置法,高い移植関連死亡を減少させる感染症予防の方法などコンセンサスが得られていない課題も多い。現在日本で,アグレッシブATL に対するallo-HSCT の臨床試験が進行中である。
【参考文献】
1) Utsunomiya A, et al. Improved outcome of adult T-cell leukemia/lymphoma with allogeneic hematopoietic stem cell transplantation. Bone Marrow Transplant. 2001 ; 27(1) : 15-20.(3iiiA)
2) Kami M, et al. Allogeneic haematopoietic stem cell transplantation for the treatment of adult T-cell leukemia/ lymphoma. Br J Haematol. 2003 ; 120(2) : 304-9.(3iiiA)
3) Fukushima T, et al. Allogeneic hematopoietic stem cell transplantation provides sustained long-term survival for patients with adult T-cell leukemia/lymphoma. Leukemia 2005 ; 19(5) : 829-34.(3iiiA)
4) Kato K, et al. Allogeneic bone marrow transplantation from unrelated human T-cell leukemia virus-1-negative donors for adult T-cell leukemia/lymphoma : retrospective analysis of data from the Japan Donor Program. Biol Blood Marrow Transplant. 2007 ; 13(1) : 90-9.(3iiiA)
5) Hishizawa M, et al. Transplantation of allogeneic hematopoietic stem cells for adult T-cell leukemia : a nationwide retrospective study. Blood. 2010 ; 116(8) : 1369-76.(3iiiA)
6) Okamura J, et al. Allogeneic stem-cell transplantation with reduced conditioning intensity as a novel immunotherapy and antiviral therapy for adult T-cell leukemia/lymphoma. Blood. 2005 ; 105 (10) : 4143-5.(2A)
7) Tanosaki R, et al. Allogeneic hematopoietic stem cell transplantation using reduced-intensity conditioning for adult T-cell leukemia/lymphoma : impact of antithymocyte globulin on clinical outcome. Biol Blood Marrow Transplant. 2008 ; 14(6) : 702-8.(3iiiA)
8) Choi I, et al. Long-term outcome after hematopoietic SCT for adult T-cell leukemia/lymphoma : results of prospective trials. Bone Marrow Transplant. 2011 ; 46(1) : 116-8.(3iiiA)
9) Tamaki H, et al. Donor-derived T-cell leukemia after bone marrow transplantation. N Engl Med. 2006 ; 354(16) : 1758-9.
10) 血縁造血幹細胞(骨髄・末梢血) ドナー傷害保険加入適格基準(2011.3, Version 2.0),日本造血幹細胞移植学会 ドナー委員会
| CQ3 | インドレント(くすぶり型,予後不良因子を持たない慢性型)ATL の標準治療は無治療経過観察か |
|---|
-
推奨グレードカテゴリー2B
- インドレントATL に対する化学療法は生存期間の延長にはつながらず,無治療経過観察が推奨される。
【解 説】
九州および沖縄の40 施設におけるくすぶり型および慢性型ATL 337 例を対象とした後方視的解析では1),その生存期間中央値(MST)はそれぞれ5.2 年と3.6 年であった。そのサブグループ解析では,くすぶり型での無治療群と抗がん剤投与群との間で全生存期間(OS)に差はなかった。一方,慢性型では無治療群の方が抗がん剤投与群よりも有意に生存期間が長かった(MST 7.4 年vs 2.0 年)。また,1988~1997 年に九州の多施設でくすぶり型ATL と診断された26 例のMST は7.3 年(観察期間中央値6.5 年)であった2)。また,単施設での後方視的研究報告によると,1974~2003 年にくすぶり型(25 例),慢性型(予後不良因子を持つ慢性型37 例,予後不良因子を持たない慢性型26 例,不明2 例)と診断され,増悪するまで無治療経過観察が行われた計90 例では,観察期間中央値が4.1 年の時点で12 人が10 年以上生存していた。しかし,2 年,5 年,10 年,15 年生存割合はそれぞれ約60%,47%,23%,13%と長期予後は不良であった3)。MST と無増悪MST はそれぞれ4.1 年と3.3 年であり,くすぶり型と慢性型の生存曲線がいずれもプラトーに到達せず下降したことから,増悪後のMST は約1 年と推定され,MST は長く長期生存例が一定の割合で存在するものの,増悪後の予後は不良であることが示唆される。
以上のようにインドレントATL の長期予後は決して良好ではない。しかし,有効な治療法がまだ見出されていないため,急性転化まで無治療で経過観察することが,わが国では現在コンセンサスとして定着している。
くすぶり型で皮膚病変のみを持つ症例の局所治療は,皮膚悪性腫瘍診療ガイドライン4)の参照が推奨される。
【参考文献】
1) 山田恭暉ほか.第421 回日本臨床血液学会,シンポジウム5.悪性リンパ腫の治療戦略 高悪性度リンパ腫(成人T 細胞白血病).臨床血液.2001 ; 42(4) ; 293-8.(3iiiA)
2) Ishitsuka K, et al. Smoldering adult T-cell leukemia-lymphoma : a follow-up study in Kyushu. Br J Haematol. 2008 ; 143(3) : 442-4.(3iiiA)
3) Takasaki Y, et al. Long-term study of indolent adult T-cell leukemia-lymphoma. Blood 2010 ; 115(22) : 4337-43.(3iiiA)
4) 成人T 細胞白血病・リンパ腫(ATLL)(皮膚のみに病変を有する病型).科学的根拠に基づく皮膚悪性腫瘍診療ガイドラインⅡ(第1 版).皮膚リンパ腫.日本皮膚科学会/日本皮膚悪性腫瘍学会編集,金原出版 2010, pp84-93.(ガイドライン)
| CQ4 | 再発・難治アグレッシブATL に対する治療法は何が勧められるか |
|---|
-
推奨グレードカテゴリー2B
- 現時点で同種造血幹細胞移植が生存に寄与する唯一の救援療法である。モガムリズマブの有用性については現在評価中である。
【解 説】
アグレッシブATL に対してはこれまでさまざまな化学療法が試みられてきたが,一旦治療効果が得られてもその持続期間は短く,その後は急速な経過を辿ることが多い。そのため臨床試験の遂行は困難で,単施設での少数例の報告がほとんどである。わが国におけるmodified EPOCH 療法(ETP, DXR, CPA, VCR, PSL)1),ペントスタチン2),ソブゾキサン3),塩酸イリノテカンとシスプラチン併用4)などの小規模な第Ⅰ・Ⅱ相試験の結果が報告されている。いずれも奏効割合は30~40%であったが,効果持続期間は1~6 ヵ月であった。
ケモカイン受容体のCCR4 はATL の90%以上で発現しており,予後不良因子でもある。ヒト化抗CCR4 抗体(モガムリズマブ)の第Ⅰ相試験では再発難治のアグレッシブATL 13 名中4 名に治療反応がみられ5),さらには至適投与量の単剤での第Ⅱ相試験で13/26 名(50%,うち8 名はCR)に奏効したことが報告された6)。2012 年5 月よりモガムリズマブは再発・難治性ATL に対して承認された。現在,初発のアグレッシブATL を対象としたモガムリズマブとVCAP-AMPVECP 療法[VCAP(VCR, CPA, DXR, PSL),AMP(DXR, MCNU, PSL),VECP(VDS, ETP,CBDCA, PSL)]との併用療法のランダム化第Ⅱ相比較試験が進行中であり,今後の評価が必要である。
CQ2 にあるように,同種造血幹細胞移植(allogeneic hematopoietic stem cell transplantation : allo-HSCT)は化学療法後の再発・難治アグレッシブATL の一部に長期生存をもたらすことが複数の報告で示されている。
局所再発の場合,症状緩和を目的とした局所放射線療法を行ってもよい7)。
【参考文献】
1) 小鶴三男ほか.再発・難治悪性リンパ腫に対するmodified EPOCH 療法. 臨床と研究. 1998 ; 75(7) ; 1630-6.(3iiiA)
2) Tobinai K, et al. Phase I study of YK-176 (2’-deoxycoformycin) in patients with adult T-cell leukemialymphoma : the DCF Study Group. Jpn J Clin Oncol. 1992 ; 22(3) : 164-71.(3iiiDiv)
3) Ohno R, et al. Treatment of adult T-cell leukemia/lymphoma with MST-16, a new oral antitumor drug and a derivative of bis(2,6-dioxopiperazine). The MST-16 Study Group. Cancer. 1993 ; 71(7) : 2217-21.(3iiiDiv)
4) 福島卓也ほか.治療難反応性成人T 細胞白血病・リンパ腫(ATL)に対する塩酸イリノテカン+シスプラ チンによるsalvage 療法の成績. 第5 回日本臨床腫瘍学会学術集会(2007).プログラム・抄録集 p.172(3iiiDiv)
5) Yamamoto K, et al. Phase I study of KW-0761, a defucosylated humanized anti-CCR4 antibody, in relapsed patients with adult T-cell leukemia-lymphoma and peripheral T-cell lymphoma. J Clin Oncol. 2010 ; 28(9) : 1591-8.(3iiiDiv)
6) Ishida T, et al. Defucosylated anti-CCR4 monoclonal antibody(KW-0761) for relapsed adult T-cell leukemia-lymphoma : a multicenter phase II study. J Clin Oncol. 2012 ; 30(8) : 837-42.(3iiiDiv)
7) Simone II CB, et al. Radiation therapy for the management of patients with HTLV-1-associated adult Tcell leukemia/lymphoma. Blood 2012 ; 120(9) : 1816-9.(3iiiDiv)
| CQ5 | ATL に対するインターフェロンαとジドブジンの併用療法は有用か |
|---|
-
推奨グレードカテゴリー3
- ATL に対するインターフェロンα/ジドブジン療法は,一般診療としては推奨されない。
【解 説】
ATL はCHOP 療法などのリンパ腫に対する標準治療では難治であり,HTLV-1 が関与することから,欧米ではインターフェロンα(IFNα)とジドブジン(AZT)の併用療法が検討され,1995年には2 つの小規模な臨床試験でアグレッシブATL に対する有望な奏効割合が報じられた1)2)。しかし,初発例に限るとその奏効割合と生存期間中央値(MST)は当時のJCOG-LSG による化学療法より下回っていたこともあって,日本でこの治療法は本格的に検討されなかった1)~3)。2010 年に,欧州と北中南米での後方視的併合解析において,リンパ腫型よりも白血化している急性型,慢性型,くすぶり型で本治療法が有用であったと報告された4)。これを受けてNCCN ガイドラインでは,リンパ腫型以外のATL に対してIFNα/AZT 療法を推奨している(NCCN ガイドライン:カテゴリー2A)。またこの報告では,IFNα/AZT 療法群での治療成績は白血化しているこれらの3 病型で化学療法群を上回っていた一方,急性型ATL に対する化学療法の治療成績は,日本での化学療法の成績を下回っていた。一方,慢性型とくすぶり型では,症例数は少ないものの観察期間中央値5 年で全例が生存しており,皮膚病変の改善にも有用と報告された4)。本併用療法は,長期にわたる治療が必要であり,倦怠感などの全身症状,造血障害など多様な有害事象を認めるものの,化学療法や同種造血幹細胞移植(allogeneic hematopoietic stem cell transplantation : allo-HSCT)に比べて毒性は低いと報告されている。
以上よりIFNα/AZT 療法は,確かにATL に対して有望な治療法であるが,これまでの海外での小規模な臨床的検討と後方視的解析によるエビデンスが十分でないことから,一般診療では推奨されない。なお,IFNα,AZT ともにATL では国内適応外である。現在わが国で,インドレントATL に対するIFNα/AZT 療法と無治療経過観察との比較試験が計画されている。
【参考文献】
1) Gill PS, et al. Treatment of adult T-cell leukemia-lymphoma with a combination of interferon alfa and zidovudine. N Engl J Med. 1995 ; 332(26) : 1744-8.(3iiiDiv)
2) Hermine O, et al. Treatment of adult T-cell leukemia-lymphoma with zidovudine and interferon alfa. N Engl J Med. 1995 ; 332(26) : 1749-51.(3iiiDiv)
3) Tobinai K, et al. Interferon alfa and zidovudine in adult T-cell leukemia-lymphoma (correspondence). N Engl J Med. 1995 ; 333(19) : 1285-6.(3iiiDiv)
4) Bazarbachi A, et al. Meta-Analysis on the Use of Zidovudine and Interferon-Alfa in Adult T-Cell Leukemia/ Lymphoma Showing Improved Survival in the Leukemic Subtypes. J Clin Oncol. 2010 ; 28 (27) : 4177-83.(3iiiA)
9
節外性NK/T 細胞リンパ腫,鼻型
(extranodal NK/T-cell lymphoma, nasal type:ENKL)
(extranodal NK/T-cell lymphoma, nasal type:ENKL)
◆総論
WHO 分類(2008)ではNK 細胞腫瘍として,節外性NK/T 細胞リンパ腫,鼻型(extranodal NK/T-cell lymphoma, nasal type:ENKL),アグレッシブNK 細胞白血病(aggressive NK-cell leukemia:ANKL),慢性NK 細胞増多症(chronic lymphoproliferative disorders of NK cells:CLPD-NK)の3 病型が記載されている1)。いずれも稀少病型であり,ANKL の頻度はENKL の7分の1 以下であるため2),治療法に関するエビデンスは乏しい。このため本項ではENKL についてのみ取り扱う。
ENKL のほとんどはNK 細胞由来であり,鼻咽頭原発例においてT 細胞由来のリンパ腫が少数存在するとされている。パラフィン材料を用いた現在の病理組織学的手法ではNK 細胞型とT 細胞型の鑑別ができないため,NK/T との用語が採用されている。NK 細胞型とT 細胞型の識別はフローサイトメトリーあるいはT 細胞受容体再構成の遺伝子解析で可能であるため,十分な検体量を採取困難な鼻咽頭以外の原発例およびANKL では識別可能なことが多い。鼻咽頭原発例ではCD56 発現に加えてEB ウイルスの存在や細胞傷害性分子の存在で他のPTCL との鑑別を行っているのが現状である。
病期分類には,ほかの悪性リンパ腫と同様にAnn Arbor 分類が用いられる。日本および韓国から予後予測モデルがそれぞれ提唱されている2)3)。他のリンパ腫と異なり診断時年齢は予後因子とならない。臨床病期は治療法の選択に重要である。治療効果の判定に際しては,特に鼻腔周辺は解剖学的に複雑であること,腫瘍が消失しても粘膜肥厚などの非腫瘍組織の残存があり得ること,ENKL ではpositron emission tomography (PET) において高率に18 fluoro-2-deoxyglucose(FDG)の取り込みが認められることから4),FDG-PET が有用である。
【参考文献】
1) Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008.
2) Suzuki R, et al. Prognostic factors for mature natural killer(NK)-cell neoplasms : aggressive NK-cell leukemia and extranodal NK-cell lymphoma, nasal-type. Ann Oncol. 2010 ; 21(5): 1032-40.(3iiA)
3) Lee J, et al. Extranodal natural killer T-cell lymphoma, nasal-type : a prognostic model from a retrospective multicenter study. J Clin Oncol. 2006 ; 24(4) : 612-8.(3iiA)
4) Kako S, et al. FDG-PET in T-cell and NK-cell neoplasms. Ann Oncol. 2007 ; 18(10) : 1685-90.
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
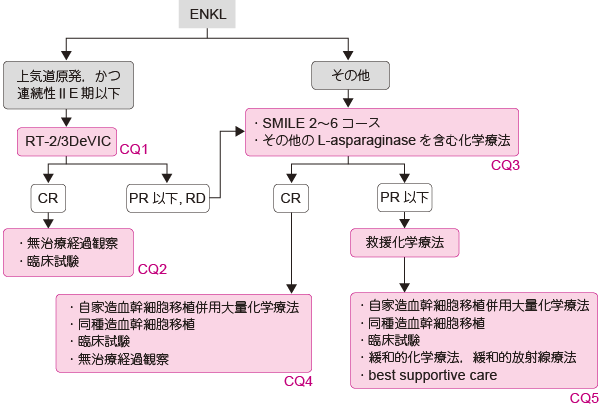
ENKL では3 分の2 を超える患者が鼻腔あるいはその周辺組織を中心とする限局期病変を有する。鼻咽頭原発例で病変が頸部リンパ節までにとどまっている患者では,わが国で実施された第Ⅰ/Ⅱ相試験の結果から同時化学放射線療法であるRT-2/3DeVIC 療法(DEX, ETP, IFM, CBDCA)を行うことが推奨される(CQ1)。RT-2/3DeVIC 療法で完全奏効(CR)を得た場合,地固め療法としての自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)を行うことは推奨されない(CQ2)。
鼻咽頭原発で病変が頸部リンパ節を超えて広がっている場合,鼻咽頭など上気道以外での発生例,初回治療後再発または部分奏効(PR)以下のENKL に対しては,第Ⅱ相試験の結果からSMILE 療法(DEX, MTX, IFM, L-Asp, ETP)を行うことが推奨される(CQ3)。
初発進行期ENKL の全例および初回再発/治療抵抗性ENKL で救援療法後CR 例では,現時点では前方視的臨床試験が存在しないためエビデンスレベルとしては低いものの,移植後長期奏効を得ている患者が存在することから,年齢や全身状態などの問題がなければ,自家または同種移植が推奨される(CQ4)。救援療法後PR 以下のENKL の予後は不良であり,年齢や全身状態などの問題がなければ,自家または同種造血幹細胞移植が推奨される(CQ5)。
| CQ1 | 初発鼻咽頭限局期(頸部リンパ節浸潤までのⅡE 期)ENKL における最も適した治療は何か |
|---|
-
推奨グレードカテゴリー2A
- 同時化学放射線療法であるRT-2/3DeVIC 療法が最も推奨される。
【解 説】
ENKL では3 分の2 を超える患者が鼻腔あるいはその周辺組織を中心とする限局期病変を有する。正常NK 細胞が多剤耐性(multi-drug resistance:MDR)に関与するP 糖蛋白を発現しているため,その腫瘍であるENKL ではP 糖蛋白で細胞外に能動輸送される抗がん剤であるドキソルビシン(DXR),ビンクリスチン(VCR)を含むCHOP 療法の有効性が低い。放射線治療単独での完全奏効(CR)割合は比較的良好(65%)であるが,照射野内外の再発割合が高いために長期予後は不良である1)。NCCN ガイドラインではⅠ期でリスク因子のない患者では放射線治療単独をオプションの一つとしているが,これを支持するエビデンスは不十分である。
鼻咽頭原発で病変が頸部リンパ節までの限局期ENKL に対し,唯一前方視的臨床試験で照射単独に優る効果が示唆された治療法は,国内多施設共同第Ⅰ/Ⅱ相試験(JCOG0211-DI)のデータに基づく同時化学放射線療法の一つであるRT-2/3DeVIC 療法(DEX, ETP, IFM, CBDCA)である2)。これは病変+2 cm 辺縁+浸潤臓器(鼻腔・鼻咽頭)全体に対する高線量照射(総線量50~50.4 Gy)と,DeVIC 療法において抗がん剤の用量を3 分の2 に減量した2/3DeVIC 療法とを同時に開始するものである。評価対象27 人における5 年全生存割合(OS)は70%であった3)。次いで韓国のSamsung Medical Center を中心とする研究グループが報告した同時化学放射線療法を組み入れた治療法[CCRT(RT, CDDP)-VIPD(ETP, IFM, CDDP, DEX)療法]4)の第Ⅱ相試験結果が報告され,解析上の多くの問題点が指摘されたものの,同時化学放射線療法の有用性を支持する結果であった。以上の結果およびわが国における治療実績から,RT-2/3DeVIC 療法が最も推奨される。
鼻咽頭原発で病変が鎖骨下リンパ節など頸部リンパ節領域を超えて認められる場合は,広範な照射野,縦隔が照射野に含まれるなど,安全性に懸念が残るため,進行期に準じた治療がより望ましいと考えられる。この場合,鼻咽頭病変に照射すべきか否かについてはエビデンスが乏しい。
【参考文献】
1) Kim GE, et al. Angiocentric lymphoma of the head and neck : patterns of systemic failure after radiation treatment. J Clin Oncol. 2000 ; 18(1) : 54-63.(3iiA)
2) Yamaguchi M, et al. Phase Ⅰ/Ⅱ study of concurrent chemoradiotherapy for localized nasal natural killer/ T-cell lymphoma : Japan Clinical Oncology Group Study JCOG0211. J Clin Oncol. 2009 ; 27(33) : 5594-600.(3iiiA)
3) Yamaguchi M, et al. Concurrent chemoradiotherapy for localized nasal natural killer (NK)/T-cell lymphoma : an updated analysis of the Japan Clinical Oncology Group Study, JCOG0211. J Clin Oncol. 2012 ; 30(32) : 4044-6.(Correspondence)(3iiiA)
4) Kim SJ, et al. Phase Ⅱ trial of concurrent radiation and weekly cisplatin followed by VIPD chemotherapy in newly diagnosed, stage IE to IIE, nasal, extranodal NK/T-cell lymphoma : Consortium for Improving Survival of Lymphoma study. J Clin Oncol. 2009 ; 27(35) : 6027-32.(3iiiDiv)
| CQ2 | 初発鼻咽頭限局期のRT-2/3DeVIC 療法後CR 例に対して地固め療法としての自家造血幹細胞移植併用大量化学療法は必要か |
|---|
-
推奨グレードカテゴリー4
- 初発鼻咽頭限局期例のRT-2/3DeVIC 療法後CR 例における地固め療法としての自家造血幹細胞移植併用大量化学療法の有用性を示すエビデンスは乏しく,推奨されない。
【解 説】
難治性リンパ腫として認識されてきたENKL において,鼻咽頭限局期で初回治療後完全奏効(CR)例において地固め療法として何らかの造血幹細胞移植を行うことは,これまで国内外で日常診療として試みられてきたが,十分なサンプルサイズでその有用性を評価した研究は少ない。ENKL 262 人を対象とした韓国の多施設共同後方視的研究の結果,限局期,NK-PI(NK/T-cell lymphoma prognostic index;Ann Arbor 分類におけるB 症状,病期ⅢまたはⅣ,高LDH 血症,所属リンパ節病変の4 項目の該当数で4 グループに分ける予後予測モデル)がGroup 1 または2,上気道発症例では自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)の実施意義が明らかでなかったことが2006 年に報告された1)。一方,その後,日本を含む東アジア多国間での後方視的研究(matched controlled study)の結果,自家移植は診断時NK-PI がGroup 3 または4 のCR 達成例で実施意義があることが2008 年に報告された2)。
いずれの研究成果も十分な観察期間で得られたデータであるが,その反面,現在広く一般的に実施されている診断後早期の放射線療法,DeVIC 療法(DEX, ETP, IFM, CBDCA)を代表とする多剤耐性(multi-drug resistance : MDR)克服を意図した化学療法,それらの併用による同時化学放射線療法の実施された患者の占める割合が低い。
CQ1 の記載に示すように,現在では初発鼻咽頭原発限局期ENKL においてはRT-2/3DeVIC 療法が推奨される。このエビデンスのソースとなったJCOG0211-DI 試験では,NK-PI は予後に関連しなかったことがサブグループ解析の結果から明らかになっている。同様に,韓国で行われた化学放射線療法[CCRT(RT, CDDP)-VIPD(ETP, IFM, CDDP, DEX)療法]の第Ⅱ相試験でもNK-PI は予後をよく反映しなかった。ただしこれらのデータは各々30 例規模の解析であり,今後検証される必要がある。
以上より現時点では鼻咽頭原発のENKL 限局期例において,初回治療に続く地固め療法としてのHDC/AHSCT の有用性は未確定である。しかし,RT-2/3DeVIC 療法で良好な治療成績が得られつつあること,後述されるように有望な救援化学療法が開発されていることなどから,現時点ではRT-2/3DeVIC 療法でCR となれば,地固め療法としてのHDC/AHSCT を行わず無治療経過観察することが推奨される。
【参考文献】
1) Kim HJ, et al. High-dose chemotherapy with autologous stem cell transplantation in extranodal NK/Tcell lymphoma : a retrospective comparison with non-transplantation cases. Bone Marrow Transplant. 2006 ; 37(9) : 819-24.(3iiA)
2) Lee J, et al. Autologous hematopoietic stem cell transplantation in extranodal natural killer/T cell lymphoma : a multinational, multicenter, matched controlled study. Biol Blood Marrow Transplant. 2008 ; 14(12) : 1356-64.(3iiA)
| CQ3 | 初発進行期および初回再発/治療抵抗性ENKL に適した治療は何か |
|---|
-
推奨グレードカテゴリー2A
- 多剤併用化学療法であるSMILE 療法が最も推奨される。
【解 説】
初発ENKL では,約25%が骨髄浸潤などの全身播種を示し,アントラサイクリンを含む化学療法が行われていた時代の完全奏効(CR)割合は15%,50%生存期間は4 カ月と極めて予後不良であった1)。多剤耐性(multi-drug resistance : MDR)に関与するP 糖蛋白の影響を受けない薬剤を主体とするSMILE 療法(DEX, MTX, IFM, L-Asp, ETP)がわが国を中心として東アジアで開発され,年齢15~69 歳,Performance Status (PS)0~2 の初発Ⅳ期,初回治療後再発・治療抵抗性ENKL を対象として第Ⅱ相試験が行われ,既存の治療成績と比較して優れたCR 割合,1 年全生存割合(OS)を示した2)。
NCCN ガイドラインでは本対象集団においてもRT-2/3DeVIC 療法(DEX, ETP, IFM, CBDCA)などの同時化学放射線療法,あるいはSMILE 療法などの後に放射線療法を追加する治療法を選択肢に挙げているが,進行期例でのエビデンスはない。
GELA/GOELAMS による初回再発/ 治療抵抗性ENKL を対象としたAspaMetDex 療法(L-Asp,MTX, DEX)の第Ⅱ相試験の結果が報告されているが,対象19 例中12 例が限局期例であり,17 例はCHOP またはCHOP 類似療法を受けている3)。日本の初回治療であれば再発/ 治療抵抗性とならないような予後良好な患者が含まれている可能性もあり,わが国における推奨治療としては疑問が残り,現時点ではSMILE 療法が最も推奨される。
【参考文献】
1) Suzuki R, et al. Prognostic factors for mature natural killer(NK)-cell neoplasms : aggressive NK-cell leukemia and extranodal NK-cell lymphoma, nasal-type. Ann Oncol. 2010 ; 21(5) : 1032-40.(3iiA)
2) Yamaguchi M, et al. Phase Ⅱ study of SMILE chemotherapy for newly diagnosed stage IV, relapsed, or refractory extranodal natural killer (NK)/T-cell lymphoma, nasal type : The NK-Cell Tumor Study Group study. J Clin Oncol. 2011 ; 29(33) : 4410-6.(3iiiDiv)
3) Jaccard A, et al. Efficacy of L-asparaginase with methotrexate and dexamethasone (AspaMetDex regimen)in patients with refractory or relapsing extranodal NK/T-cell lymphoma, a phase Ⅱ study. Blood. 2011 ; 117(6) : 1834-9.(3iiiDiv)
| CQ4 | 初発進行期ENKL 全例および初回再発/治療抵抗性ENKL で救援療法後CR 例では造血幹細胞移植を追加すべきか |
|---|
-
推奨グレードカテゴリー2B
- 初発進行期ENKL 全例および初回再発/治療抵抗性ENKL で,救援療法でCR に到達した場合は,年齢や全身状態などの問題がなければ,自家または同種造血幹細胞移植が推奨される。
【解 説】
予後不良とされてきた初回進行期および初回再発,治療抵抗性ENKL では,これまで造血幹細胞移植療法なしに長期生存は困難であった。後方視的解析の結果ではあるが自家移植1)~3)もしくは同種移植2)4)を受けた一部患者で長期生存が報告されている。
SMILE 療法(DEX, MTX, IFM, L-Asp, ETP)などL-アスパラギナーゼ(L-Asp)を含む新しい併用化学療法が行われる時代になってきたが,これまでに報告された臨床試験の成績は造血幹細胞移植が実施された患者を含むものである5)。選択バイアスの可能性もあるが,サブグループ解析では自家または同種移植を受けた患者の方が全生存割合(OS)は良好であった。化学療法のみで長期生存ないし奏効持続が得られるというデータはなく,現時点では前方視的臨床試験が存在しないためエビデンスレベルとしては低いが,患者の年齢や全身状態が問題なければ,自家または同種移植の実施が推奨される。
移植の種類に関しては,これも選択バイアスの可能性はあるが,自家移植の成績は同種移植と同等かそれ以上であり6)7),完全奏効(CR)で遂行可能な患者には自家移植実施の妥当性が示唆される。特に適切な同種骨髄・末梢血ドナーが存在しない場合,ドナー検索に時間をかけるより,CR での自家移植の実施が推奨される。なお臍帯血移植に関するデータは,今のところ乏しい。
【参考文献】
1) Au WY, et al. Autologous stem cell transplantation for nasal NK/T-cell lymphoma : a progress report on its value. Ann Oncol. 2003 ; 14(11) : 1673-6.(3iiiA)
2) Suzuki R, et al. Hematopoietic stem cell transplantation for natural killer-cell lineage neoplasms. Bone Marrow Transplant. 2006 ; 37(4) : 425-31.(3iiA)
3) Kim HJ, et al. High-dose chemotherapy with autologous stem cell transplantation in extranodal NK/Tcell lymphoma : a retrospective comparison with non-transplantation cases. Bone Marrow Transplant. 2006 ; 37(9) : 819-24.(3iiA)
4) Murashige N, et al. Allogeneic haematopoietic stem cell transplantation as a promising treatment for natural killer-cell neoplasms. Br J Haematol. 2005 ; 130(4) : 561-7.(3iiiA)
5) Yamaguchi M, et al. Phase Ⅱ study of SMILE chemotherapy for newly-diagnosed stage IV, relapsed or refractory extranodal natural killer(NK)/T-cell lymphoma, nasal type : The NK-cell Tumor Study Group(NKTSG) study. J Clin Oncol. 2011 ; 29(33) : 4410-6.(3iiiDiv)
6) Lee J, et al. Autologous hematopoietic stem cell transplantation in extranodal natural killer/T-cell lymphoma : a multinational, multicenter, matched controlled study. Biol Blood Marrow Transplant. 2008 ; 14(12) : 1356-64.(3iiA)
7) Suzuki R, et al. Hematopoietic stem cell transplantation for extranodal NK/T-cell lymphoma, nasal-type : The Japan Society for Hematopoietic Cell Transplantation(JSHCT) Lymphoma Working Party. Ann Oncol. 2011 ; 22(Suppl. 4) : iv95.(3iiA)
| CQ5 | 初発進行期および初回再発/治療抵抗性ENKL の救援療法後非CR 例において造血幹細胞移植を追加する意義はあるか |
|---|
-
推奨グレードカテゴリー3
- 救援療法後非CR のENKL は,患者の全身状態が良ければ自家または同種移植の検討対象になり得る。
【解 説】
救援療法後非完全奏効(CR)のENKL で造血幹細胞移植を行った前方視的臨床試験は存在しない。日本造血細胞移植学会のレジストリーデータには救援療法後非奏効ENKL 45 例が登録されており,その2 年全生存割合(OS)は同種移植・自家移植とも29%であった1)。選択バイアスの可能性はあるが,移植を実施しない場合のOS がゼロであることを考慮すると,何らかの造血幹細胞移植は選択肢になり得る。当然,議論の余地はあり,コンセンサスは得られていない。
【参考文献】
1) Suzuki R, et al. Hematopoietic stem cell transplantation for extranodal NK/T-cell lymphoma, nasal-type : The Japan Society for Hematopoietic Cell Transplantation(JSHCT) Lymphoma Working Party. Ann Oncol. 2011 ; 22(Suppl. 4) : iv95.(3iiA)
10
ホジキンリンパ腫
(Hodgkin lymphoma:HL)
(Hodgkin lymphoma:HL)
◆総論
ホジキンリンパ腫(Hodgkin lymphoma:HL)は,欧米では全悪性リンパ腫の約30%,わが国 では8~10%を占める。
年齢分布は,若年者層(20 歳代)と中年層(50~60 歳)にピークを有する二相性を呈する。
初発症状は多くは無症候性,無痛性表在リンパ節腫脹で,約75%が頸部・鎖骨上窩リンパ節腫脹で発見される。結節硬化型HL は約60%に縦隔病変を認める。
血液検査所見は,白血球増多,リンパ球減少,好酸球増多,貧血,アルカリフォスファターゼの上昇,血液沈降速度の亢進,CRP 異常高値,細胞性免疫能の低下などを認める。
病理組織学的には,Hodgkin/Reed-Sternberg(HRS)細胞,lymphocyte predominant(LP)細胞(popcorn 細胞)などの腫瘍細胞の増生を特徴とするリンパ腫である。WHO 分類(2008)においてHL は結節性リンパ球優位型HL(nodular lymphocyte-predominant Hodgkin lymphoma:NLPHL)と古典的HL(classical Hodgkin lymphoma:CHL)の2 つに大別されている1)2)。HRS 細胞はCHL,LP 細胞はNLPHL に特徴的とされる。CHL は結節硬化型HL(nodular sclerosis Hodgkin lymphoma),リンパ球豊富型HL(lymphocyte-rich classical Hodgkin lymphoma),混合細胞型HL(mixed cellularity Hodgkin lymphoma),リンパ球減少型HL(lymphocyte depleted Hodgkin lymphoma)の4 つの準疾患単位に分類される。
HL はAnn Arbor 病期分類によりⅠ~Ⅳ期に分類される。
1.限局期CHL の予後因子
限局期(Ⅰ,Ⅱ期)CHL の予後因子を表1 に示す。研究グループにより重視する予後因子が異なることに注意が必要である3)~5)。
| 研究グループ | GHSG | EORTC | NCIC/ECOG | NCCN2011 |
|---|---|---|---|---|
| 予後良好群 | 病期Ⅰ,Ⅱ期 リスク因子なし |
病期Ⅰ,Ⅱ期 (横隔膜上部病変) リスク因子なし |
病期Ⅰ,ⅡA 期 リスク因子なし |
病期Ⅰ,Ⅱ期 リスク因子なし |
| 予後不良群 | 病期Ⅰ,Ⅱ期 リスク因子あり 病期ⅡB 期ではbulky 縦隔病変,節外病変 があれば進行期 |
病期Ⅰ,Ⅱ期 (横隔膜上部病変) リスク因子あり |
病期Ⅰ,ⅡA 期 リスク因子あり ただし,bulky 病変, 腹腔内病変があると 進行期 |
病期Ⅰ,Ⅱ期 リスク因子あり |
| リスク因子 |
|
|
|
|
GHSG : German Hodgkin Study Group, EORTC : European Organization for the Research and Treatment of Cancer,
NCIC : National Cancer Institute of Canada, ECOG : Eastern Cooperative Oncology Group,
NCCN : National Comprehensive Cancer Network
2.進行期CHL の予後因子
進行期CHL(Ⅲ,Ⅳ期)に用いられる予後予測モデルとしてはInternational Prognostic Score(IPS)がある6)。これは15~65 歳までの進行期CHL でMOPP 療法[mechlorethamine(国内未承認),VCR, PCZ, PSL]やABVD 療法(DXR, BLM, VBL, DTIC)などによる治療を受けた4,695 例を対象とし解析を行い,無増悪期間(TTP)をエンドポイントとして7 つの予後因子を抽出した。これらの因子の数によってTTP の予測が可能とされている。このシステムでは5 年での予測TTP は,予後不良因子数0 の場合は84%であるのに対し,5 以上の場合は42%と不良である。
【参考文献】
1) Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC ; 2008.
2) Nogová L et al. Lymphocyte-predominant and classical Hodgkin’s lymphoma : a comprehensive analysis from the German Hodgkin Study Group. J Clin Oncol. 2008 ; 26(3) : 434-9.(3iiiDiii)
3) Noordijk EM, et al. Combined-modality therapy for clinical stageⅠor Ⅱ Hodgkin’s lymphoma : long-term results of the European Organisation for Research and Treatment of Cancer H7 randomized controlled trials. J Clin Oncol. 2006 ; 24(19) : 3128-35.(1iiDiii)
4) Engert A et al. German Hodgkin’s Lymphoma Study Group.Involved-field radiotherapy is equally effective and less toxic compared with extended-field radiotherapy after four cycles of chemotherapy in patients with early-stage unfavorable Hodgkin’s lymphoma : results of the HD8 trial of the German Hodgkin’s Lymphoma Study Group. J Clin Oncol. 2003 ; 21(19) : 3601-8.(1iiDiii)
5) Meyer RM, et al. Randomized comparison of ABVD chemotherapy with a strategy that includes radiation therapy in patients with limited-stage Hodgkin’s lymphoma : National Cancer Institute of Canada Clinical Trials Group and the Eastern Cooperative Oncology Group. J Clin Oncol. 2005. ; 23(21) : 4634-42.(1iiA)
6) Hasenclever D et al. A prognostic score for advanced Hodgkin’s disease. International Prognostic Factors Project on Advanced Hodgkin’s Disease. N Engl J Med. 1998 ; 339(21) : 1506-14.(3iiiDiii)
◆アルゴリズム
(※)CQ番号(ピンク色部分)をクリックすると,解説画面へ移動します
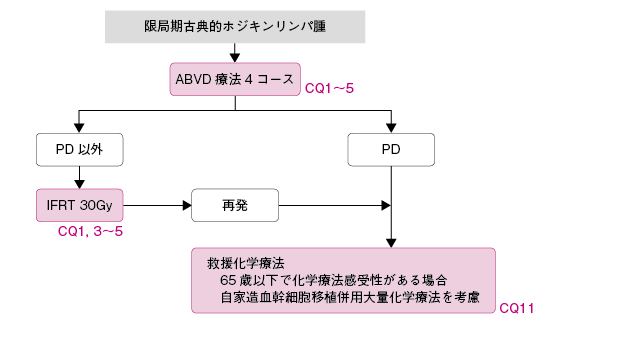
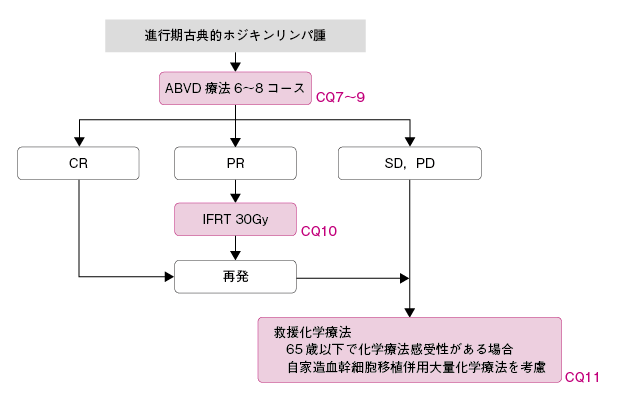
HL の治療法はCHL とNLPHL とで異なる。CHL においては限局期および進行期とも放射線療法単独で治療することは推奨されない。化学療法単独または化学療法と放射線療法の併用が推奨される。限局期NLPHL のうち,限局期例ではinvolved field radiotherapy(IFRT)が標準治療である(CQ6)。
化学療法はABVD 療法(DXR, BLM, VBL, DTIC)が標準である。
また,放射線療法においては拡大放射線療法(extended field radiotherapy:EFRT)であるマントル照射や全リンパ領域照射などに代表される系統的なリンパ節照射療法の採用は推奨されない。化学療法と併用される場合はIFRT が推奨される。
1.限局期症例
限局期CHL では初回治療として化学療法と放射線療法との併用療法(combined modality therapy:CMT)が行われる(CQ1)。現在,用いられている代表的なレジメンはABVD 療法である(CQ2)。限局期CHL に対するABVD 療法4 コース後のIFRT の治療成績は10 年無増悪生存割合(PFS)が90%以上である。放射線療法による晩期毒性,特に肺,乳房,消化管の二次がんや心血管系疾患による遅発性の死亡が問題となり,化学療法単独の治療方法も検討されている(CQ3)。近年,予後不良因子を持たない限局期CHL に対しては,有害事象の軽減のために化学療法の施行回数や照射量を減じる臨床試験が行われている。予後不良群に対してはABVD 療法4 コース後IFRT 30 Gy(CQ5)が推奨されるが,予後良好群に対してはABVD 療法2 コース後IFRT 20 Gy(CQ4)も推奨される治療法の一つである。CMT においてはABVD 療法終了時に明らかな進行(PD)と判定されない限り,IFRT を予定通り行い治療終了する。再発症例は進行期再発症例と同様の治療法がとられることが多い。
2.進行期症例
進行期CHL の初回治療としてはABVD 療法6~8 コースが推奨される(CQ7, CQ8)。IPS によるリスク分類を用いて層別化して治療法を選択することは推奨されない(CQ9)。化学療法終了時にCT およびPET にて完全奏効(CR)であれば治療は終了することが推奨される(CQ10)。部分奏効(PR)の場合にはIFRT の追加が考慮される(CQ10)。初回化学療法で安定(SD)以下あるいは化学療法後の再発症例では救援療法が施行されるが,65 歳以下で救援療法に感受性がある場合は臓器機能が保たれていれば大量化学療法は推奨される治療法である(CQ11)。また,進行期症例においては初回治療中のinterim PET は予後予測に有用であるが,その結果により治療変更することの是非は臨床試験での検討段階であり,一般診療としては推奨されない(CQ12)。
| CQ1 | 限局期予後良好CHL に対する化学療法と放射線療法の併用(CMT)は放射線単独療法より優れているか |
|---|
-
推奨グレードカテゴリー1
- 限局期予後良好CHL に対するCMT は放射線単独療法に比べ治療成績が優れており,拡大放射線療法による有害事象を軽減することができる。
【解 説】
限局期予後良好CHL に対する化学療法と放射線療法の併用(combined modality therapy : CMT)は,拡大放射線療法(extended field radiotherapy : EFRT)単独に比べ照射野を縮小する ことにより放射線療法の有害事象を減らすことができる。また,限局期CHL に対する少なくとも4 つのランダム化比較試験の結果では,CMT がEFRT に比べて治療成績が有意に優れていた1)~4)。
病期ⅠA, ⅡA 期CHL に対する化学療法(DXR, VBL)3 コース+亜全リンパ領域照射(subtotal lymphoid irradiation:STLI)併用(CMT)群とSTLI 単独群の比較試験では,CMT 群の3 年無進行生存割合がEFRT 単独群に比べ有意にCMT 群の方が優れていたが全生存割合(OS)は有意差を認めなかった1)。また,限局期予後良好CHL に対するEBVP 療法(EPI, BLM, VBL, PSL)6 コース施行後IFRT を併用したCMT 群とSTLI 単独群との比較試験では,OS には差を認めなかったが無イベント生存割合(EFS)では有意にCMT 群が優れていた2)。限局期予後良好CHL に対してABVD 療法(DXR, BLM, VBL, DTIC)2 コース後EFRT を施行するCMT 群とEFRT 単独群の比較試験の結果,7 年治療成功割合(FFTF)はEFRT 群に比しCMT 群が有意に優れていたが,7 年OS には差を認めなかった3)。限局期予後良好CHL を対象にしたランダム化比較試験では,3 コースのMOPP(HN2, VCR, PCZ, PSL)/ABV(DXR, BLM, VBL)+IFRT のCMT 群とSTLI 単独群とが比較された。5 年EFS および10 年OS に関してCMT 群が優れていた4)。VBM 療法(VBL, BLM, MTX)6 コース+ IFRT のCMT 群とEFRT 単独群を比較した21 年のフォローアップデータでは,21 年無増悪生存期間および全生存期間ともにCMT 群の方が有意に優れていた。この研究のEFRT の死亡原因は放射線による晩期毒性によるものがCMT 群より多かった5)。
これらの結果から,限局期予後良好CHL においてEFRT を用いた放射線単独療法と比較しCMT は効果が良好であり,晩期有害事象も少ないと考えられる。
【参考文献】
1) Press OW, et al. Phase Ⅲ randomized intergroup trial of subtotal lymphoid irradiation versus doxorubicin, vinblastine, and subtotal lymphoid irradiation for stage ⅠA to ⅡA Hodgkin’s disease. J Clin Oncol 2001 ; 19(22) : 4238-44 .(1iiDiii)
2) Noordijk EM, et al. Combined-modality therapy for clinical stageⅠor Ⅱ Hodgkin’s lymphoma : long-term results of the European Organisation for Research and Treatment of Cancer H7 randomized controlled trials. J Clin Oncol 2006 ; 24(19) : 3128-35.(1iiDiii)
3) Engert A, et al. Two cycles of doxorubicin, bleomycin, vinblastine, and dacarbazine plus extended-field radiotherapy is superior to radiotherapy alone in early favorable Hodgkin’s lymphoma : final results of the GHSG HD7 trial. J Clin Oncol 2007 ; 25(23) : 3495-502 .(1iiDiii)
4) Fermé C,et al. EORTC-GELA H8 Trial. Chemotherapy plus involved-field radiation in early-stage Hodgkin’s disease. N Engl J Med. 2007 ; 357(19) : 1916-27.(1iiDi)
5) Horning SJ, et al. A prospective trial of involved field radiation(IFRT)+chemotherapy compared to extended field (EFRT) radiation for favorable Hodgkin’s disease : survival differences and implications of mature follow-up for current combined modality therapy. Program and abstracts of the 43rd American Society of Clinical Oncology Annual Meeting ; June 1-5, 2007a ; Chicago, Illinois. Abstract 8014.(1iiA)
| CQ2 | 限局期CHL に対する最適な化学療法レジメンは何か |
|---|
-
推奨グレードカテゴリー2A
- 限局期CHL に対する化学療法は,良好な治療成績と遅発性有害事象が少ないため,ABVD 療法が推奨される。
【解 説】
進行期CHL では,ABVD 療法(DXR, BLM, VBL, DTIC)6~8 コースはMOPP 療法(HN2,VCR, PCZ, PSL)やMOPP/ABVD 療法と有効性は同等で急性毒性および晩期毒性が低いことが示され,現在の標準治療とみなされている1)。そのため,限局期CHL でも進行期に準じてABVD 療法が推奨されている。
限局期CHL に対するABVD 療法4 コース後IFRT を行うCMT の12 年無増悪生存割合(PFS)は94%と良好な治療成績が示され,ABVD 療法4 コース後IFRT 療法が有効であることが報告されている2)。また,Japan Clinical Oncology Group(JCOG)は病期Ⅱ~Ⅳ期のCHL に対してABVd 療法(国内でのpilot study で観察された悪心を主とする消化器毒性の軽減のため,ダカルバジン(DTIC)を250 mg/m2 に減量)6~8 コース施行し,bulky 病変が治療前に存在した場合には30~40 Gy のIFRT を追加する第Ⅱ相試験を行った。この臨床試験における病期Ⅱ期の5 年PFS は86.8%,全生存割合(OS)97.4%と良好な治療成績であった(JCOG9305 試験)3)。
また,限局期予後不良群CHL に対してABVD 療法4 コースとBEACOPP 療法(BLM, ETP,DXR, CPA, VCR, PCZ, PSL)4 コース,その後にIFRT 20 Gy あるいは30 Gy を行う2×2 ランダム化比較第Ⅲ相試験が行われ,治療効果は同等であったが,急性毒性がBEACOPP 療法で有意に多いことが示された。この結果から,限局期予後不良群CHL に対してもABVD 療法4 コース後の30 Gy IFRT(1.8~2.0 Gy/回,週5 回)が推奨された(HD11 試験)4)。
これらの結果,および近年における支持療法の進歩(より有効な制吐剤およびG-CSF の導入)を考慮すると,限局期CHL に対する化学療法としてはABVD 療法が推奨される。
【参考文献】
1) Canellos GP, et al. Chemotherapy of advanced Hodgkin’s disease with MOPP, ABVD, or MOPP alternating with ABVD. N Engl J Med 1992 ; 327(21) : 1478-84.(1iiDiii)
2) Bonadonna G, et al. ABVD plus subtotal nodal versus involved-field radiotherapy in early-stage Hodgkin’s disease : long-term results. J Clin Oncol.2004 ; 22(14) : 2835-41.(1iiDiii)
3) Ogura M,et al. Phase Ⅱ study of ABVd therapy for newly diagnosed clinical stage Ⅱ-Ⅳ Hodgkin lymphoma : Japan Clinical Oncology Group study (JCOG 9305). Int J Hematol. 2010 ; 92(5) : 713-24.(3iiiDiv)
4) Eich HT, et al. Intensified chemotherapy and dose-reduced involved-field radiotherapy in patients with early unfavorable Hodgkin’s lymphoma : final analysis of the German Hodgkin Study Group HD11 trial. J Clin Oncol. 2010 ; 28(27) : 4199-206.(1iiDiii)
| CQ3 | Bulky 病変を認めない限局期(予後良好)CHL に対する化学療法後に放射線療法は必要か |
|---|
-
推奨グレードカテゴリー2B
- Bulky 病変を認めない限局期(予後良好)CHL に対する化学療法後のIFRT の選択は,放射線療法の晩期毒性を勘案して行う必要がある。
【解 説】
Bulky 病変を認めない限局期CHL に対する化学療法と放射線療法の併用(combined modality therapy:CMT)と化学療法単独のいくつかのランダム化比較試験の結果,CMT は化学療法単独に比べて,無増悪生存期間が有意に良好であるものの,全生存期間では有意差がないことが示されている1)~4)。
カナダ国立がん研究所によるbulky 病変を認めない限局期CHL を対象にしたランダム化比較試験では,ABVD 療法(DXR, BLM, VBL, DTIC)4~6 コースの化学療法単独群とABVD 療法2 コース+拡大放射線療法(extended field radiotherapy : EFRT)(CMT 群)とが比較され,無増悪生存期間はCMT 群の方が優れていたが,全生存期間における有意差が認められなかった2)。
Bulky 病変を認めない限局期CHL を対象としてEBVP 療法(EPI, BLM, VBL, PSL)後の放射線療法について検討した試験では,20 Gy のIFRT 施行群に比べてIFRT 非施行群で無イベント生存割合が不良だった4)。
放射線療法による重大な晩期毒性である二次がん,心血管イベント,脳血管障害の発生率が経時的に増加し,約2~7 倍に達する5)6)。照射総線量を低減あるいは照射野を縮小しても,化学療法との併用で乳がんの発生リスクを高めることが報告されている6)。
一方,bulky 病変を認めない限局期CHL に対するABVD 療法6 コースのみ[involved field radiotherapy(IFRT)を施行しない]の報告では,5 年無増悪生存割合は約85~90%とCMT と遜色ない結果が報告されている7)8)。
以上の結果から,限局期患者に対して,IFRT を行わず化学療法単独で治療することの有用性についての結論は得られていないが,心血管障害や脳血管障害および二次がんのリスクを勘案して治療方針を決定する必要がある。また,化学療法単独で行う場合の対象は限局期CHL の中でもbulky 病変を認めない症例であり,ABVD 療法も6 コース施行することが推奨される7)8)。二次性固形腫瘍および心血管系疾患による晩期合併症を最小化するために,化学療法後の放射線療法を省略できるかは今後の比較試験の結果が待たれるところである。
【参考文献】
1) Nachman JB, et al. Randomized comparison of low-dose involved-field radiotherapy and no radiotherapy for children with Hodgkin’s disease who achieve a complete response to chemotherapy. J Clin Oncol. 2002 ; 20(18) : 3765-71.(1iiDi)
2) Meyer RM, et al. Randomized comparison of ABVD chemotherapy with a strategy that includes radiation therapy in patients with limited-stage Hodgkin’s lymphoma : National Cancer Institute of Canada Clinical Trials Group and the Eastern Cooperative Oncology Group. J Clin Oncol. 2005 ; 23(21) : 4634-42.(1iiA)
3) Straus DJ, et al. Results of a prospective randomized clinical trial of doxorubicin, bleomycin, vinblastine, and dacarbazine(ABVD) followed by radiation therapy(RT) versus ABVD alone for stages Ⅰ, Ⅱ, and ⅢA nonbulky Hodgkin disease. Blood. 2004 ; 104(12) : 3483-9.(1iiDi)
4) Eghbali H, et al. Comparison of three radiation dose levels after EBVP regimen in favorable supradiaphragmatic clinical stages (CS) Ⅰ-Ⅱ Hodgkin’s lymphoma (HL) : preliminary results of the EORTCGELA H9-F trial. Program and abstracts of the 47th Annual Meeting of the American Society of Hematology ; December 10-13, 2005 ; Atlanta, Georgia. Abstract 814.(1iiDiii)
5) Brusamolino E, et al. Long-term events in adult patients with clinical stage ⅠA-ⅡA nonbulky Hodgkin’s lymphoma treated with four cycles of doxorubicin, bleomycin, vinblastine, and dacarbazine and adjuvant radiotherapy : a single-institution 15-year follow-up. Clin Cancer Res. 2006 ; 12(21) : 6487-93.(3iiiDi)
6) De Bruin ML, et al. Breast cancer risk in female survivors of Hodgkin’s lymphoma : lower risk after smaller radiation volumes. J Clin Oncol. 2009 ; 27(26) : 4239-46.(3iiC)
7) Rueda Domínguez A , et al. Treatment of stage Ⅰ and Ⅱ Hodgkin’s lymphoma with ABVD chemotherapy : results after 7 years of a prospective study. Ann Oncol. 2004 ; 15(12) : 1798-804.(3iiiDiii)
8) Canellos GP, et al. Treatment of favorable, limited-stage Hodgkin’s lymphoma with chemotherapy without consolidation by radiation therapy. J Clin Oncol. 2010 ; 28(9) : 1611-5.(3iiiDiii)
| CQ4 | 予後良好限局期CHL ではABVD 療法2 コース後のIFRT が推奨されるか |
|---|
-
推奨グレードカテゴリー2B
- 予後良好限局期CHL では,ABVD 療法2 コース後のIFRT が推奨される治療の一つである。
【解 説】
限局期CHL は,予後不良因子[巨大縦隔腫瘤,リンパ節病変数(3 あるいは4 つ以上),節外病変,B 症状,血沈亢進,高齢など]の有無で,予後不良因子を持たない「予後良好群」と予後不良因子を持つ「予後不良群」に分類され,それぞれに至適な治療法の開発が進められている。German Hodgkin Study Group(GHSG)では,巨大縦隔腫瘤(胸郭横径比≧1/3),節外病変,血沈亢進(B 症状あり;≧30 mm/h,B 症状なし;≧50 mm/h),3 カ所以上の病変領域を限局期CHL の予後不良因子としている。予後良好限局期CHL では長期生存が得られるため,有害事象の軽減のために化学療法の施行回数や放射線照射量を減じる臨床試験が行われている。
GHSG は予後良好限局期CHL に対して,ABVD 療法(DXR, BLM, VBL, DTIC)2 コース対4 コースの比較と,その後のinvolved field radiotherapy(IFRT) 20 Gy vs 30 Gy との比較を行う2×2 ランダム化第Ⅲ相試験(HD10 試験)を行った1)。5 年全生存期間(OS)および治療成功期間(FFTF)は4 群間でほぼ同等であったが,毒性はABVD 療法4 コースで急性毒性および急性毒性死亡の発現頻度が高く,30 Gy IFRT は20 Gy に比べ急性毒性が多かった。そのため,毒性を考慮すると,今後ABVD 療法2 コース+IFRT 20 Gy が予後良好限局期CHL の新たな標準治療となると思われる。
一方,European Organization for Research and Treatment of Cancer-Groupe d’Etude des Lymphomes de l’Adulte(EORTC-GELA)のH8 試験では,予後良好限局期群(H8-F)に対してMOPP(HN2, VCR, PCZ, PSL)/ABV(DXR, BLM, VBL) 療法 3 コースとIFRT(36 Gy) のCMT と放射線単独療法[亜全リンパ領域照射(subtonal lymphoid irradiation : STLI)]のランダム化比較試験が行われた。H8-F 群においては10 年の無イベント生存割合(EFS),全生存割合(OS)においてMOPP/ABV 3 コース+IFRT 群がSTLI 単独群に優り,化学療法3 コースとIFRT(36 Gy)が予後良好限局期群に対する推奨療法であるとした2)。
上記およびCQ1 にあるように,予後良好限局期群では短縮コースの化学療法とIFRT のCMT が推奨されるものの,化学療法のコース数,IFRT の照射量に関しては完全なコンセンサスが得られていない。このため現時点では,良好な治療成績が報じられたABVD 療法2 コース+IFRT 20Gy は,日常診療における治療選択肢の一つとして推奨される。
【参考文献】
1) Engert A, et al. Reduced treatment intensity in patients with early-stage Hodgkin’s lymphoma. N Engl J Med. 2010 ; 363(7) : 640-52.(1iiDiii)
2) Fermé C,et al. EORTC-GELA H8 Trial. Chemotherapy plus involved-field radiation in early-stage Hodgkin’s disease.N Engl J Med. 2007 ; 357(19) : 1916-27.(1iiDi)
| CQ5 | 予後不良限局期CHL に対して推奨される治療法は何か |
|---|
-
推奨グレードカテゴリー2A
- 予後不良限局期CHL では,ABVD 療法4 コース後のIFRT が推奨される。
【解 説】
予後不良限局期CHL では,MOPP(HN2, VCR, PCZ, PSL)/ABV(DXR, BLM, VBL)療法6 コース,MOPP/ABV 療法4 コース+involved field radiotherapy(IFRT)(30Gy),MOPP/ABV 療法4 コース+亜全リンパ領域照射(subtonal lymphoid irradiation : STLI)の3 群を比較したH8-U 試験において,MOPP/ABV 療法4 コース+ IFRT の有効性は他の2 群と同等であることが示され,短期間の化学療法とIFRT のCMT が標準治療となるとしている1)。GHSG は,CQ4 の予後不良因子を一つ以上認める症例を予後不良限局期CHL と定義して,この群に対してABVD 療法(DXR, BLM, VBL, DTIC)4 コース対BEACOPP 療法(BLM, ETP, DXR, CPA, VCR, PCZ,PSL)4 コース,その後にIFRT 20 Gy vs 30 Gy を行う2×2 の比較試験を施行した。その結果,治療成功期間(FFTF)がABVD 療法4 コース+20 Gy IFRT で短い傾向(有意差はない)があり,30 Gy IFRT が化学療法の種類にかかわらず同等であったが,急性毒性はBEACOPP 群で有意に多いことが報告された。この結果から,予後不良限局期CHL においてはABVD 療法4 コース後の30 Gy IFRT が推奨された2)。
以上の結果から,予後不良限局期CHL に対してはABVD 療法4 コース後のIFRT が推奨される治療法と考えられる。
【参考文献】
1) Fermé C, et al. EORTC-GELA H8 Trial. Chemotherapy plus involved-field radiation in early-stage Hodgkin’s disease. N Engl J Med. 2007 ; 357(19) : 1916-27.(1iiDi)
2) Eich HT, et al. Intensified chemotherapy and dose-reduced involved-field radiotherapy in patients with early unfavorable Hodgkin’s lymphoma : final analysis of the German Hodgkin Study Group HD11 trial. J Clin Oncol. 2010 ; 28(27) : 4199-206.(1iiDiii)
| CQ6 | 限局期結節性リンパ球優位型HL(NLPHL)に対して推奨される治療法は何か |
|---|
-
推奨グレードカテゴリー2B
- 限局期NLPHL では,IFRT が推奨される。
【解 説】
Joint Center for Radiation Therapy で治療された限局期NLPHL の後方視的解析が報告され,放射線療法のみの症例では10 年無増悪生存割合および10 年全生存割合は良好であった1)。また,照射野に関してはinvolved field radiotherapy(IFRT),マントル照射または逆Y 照射,拡大放射線療法(extended field radiotherapy : EFRT)の比較では無増悪生存期間と全生存期間のいずれにおいても有意差はなかった。CMT は放射線療法単独に比べ無増悪生存期間,全生存期間の改善はもたらさなかった。
GHSG で行われたHD4(EFRT),HD7(EFRT vs EFRT+2×ABVD),HD10(CMT における化学療法コースとIFRT の照射量の比較試験)に登録されたNLPHL とGHSG において臨床試験外でIFRT により治療されたNLPHL で臨床病期ⅠA を対象とした後方視的解析では,すべての治療法で95%以上のCR 割合が得られ,治療成功割合,全生存期間では治療群間で有意差がなかった。限局期NLPHL においてIFRT はEFRT およびCMT と同等の治療効果が得られ,至適治療であることが示唆された2)。またNLPHL と診断された426 例を対象に病理組織学的に再診断を行い,NLPHL とCHL(リンパ球豊富型,lymphocyte-rich:LR)に再分類し,NLPHL とLR の2 群を比較した後方視的研究の報告(European Task Force on Lymphoma Project on Lymphocyte-Predominant Hodgkin’s Disease)では,これら2 つのサブグループの間には,標準的な治療に対する治療反応性または予後に有意差が認められないことが示された3)。死亡原因はHL によるものより治療の有害事象(特に二次発がんや心血管障害などの晩期毒性)によるものが多かった。
以上の結果から,限局期NLPHL ではIFRT が推奨される治療法であり,IFRT は30 Gy で施行されることが多い。
また,臨床病期Ⅰ期NLPHL で完全に病変が切除された症例においては注意深い経過観察が可能とされている3)。
【参考文献】
1) Chen RC, et al. Early-stage, lymphocyte-predominant Hodgkin’s lymphoma : patient outcomes from a large, single-institution series with long follow-up. J Clin Oncol. 2010 ; 28(1) : 136-41.(3iiiDiii)
2) Nogová L, et al. Extended field radiotherapy, combined modality treatment or involved field radiotherapy for patients with stage ⅠA lymphocyte-predominant Hodgkin’s lymphoma : a retrospective analysis from the German Hodgkin Study Group(GHSG). Ann Oncol. 2005 ; 16(10) : 1683-7.(3iiiDiii)
3) Diehl V, et al. Clinical presentation, course, and prognostic factors in lymphocyte-predominant Hodgkin’s disease and lymphocyte-rich classical Hodgkin’s disease : report from the European Task Force on Lymphoma Project on Lymphocyte-Predominant Hodgkin’s Disease. J Clin Oncol. 1999 ; 17(3) : 776-83.(3iiiA)
| CQ7 | 進行期CHL の標準療法はABVD 療法か |
|---|
-
推奨グレードカテゴリー1
- ABVD 療法は進行期CHL の標準療法である。
【解 説】
進行期CHL は化学療法が標準である。1960 年代にMOPP 療法(HN2, VCR, PCZ, PSL)が開発され,80%程度の奏効割合と約50%の長期生存が報告された1)。MOPP 療法と非交差耐性の薬剤で構成されたABVD 療法(DXR, BLM, VBL, DTIC)が開発され,Cancer and Leukemia Group B(CALGB)において,進行期CHL を対象としMOPP 療法,ABVD 療法,MOPP/ABVD 交替療法の3 群間の第Ⅲ相比較試験が実施された。ABVD 療法及びMOPP/ABVD 療法はMOPP 療法に比べ治療成功生存割合(FFS)が優ることが報告された2)。この臨床試験の長期経過観察(観察期間中央値14.1 年)においてもFFS においてABVD 療法の優位性が示された3)。全生存割合(OS)に有意差は認められなかったが,ABVD 療法はMOPP 療法およびMOPP/ABVD 療法に比べ血液毒性・感染症などの有害事象の発症頻度が有意に低く,進行期CHL の標準療法として確立された2)。
その後ABVD 療法と他の治療法の比較試験の結果が報告された。MOPP/ABV hybrid 療法4),Stanford V 療法(DXR, VBL, HN2, ETP, VCR, BLM, PSL)5),MOPPEBVCAD 療法(HN2,CCNU, VDS, MEL, PSL, EPI, VCR, PCZ, VBL, BLM),Multidrug regimen[ChIVPP/PABIOE 交替療法(CLB, VBL, PCZ, PSL, DXR, BLM, VCR, ETP),ChIVPP/EVA hybrid 療法(CLB, VBL,PCZ, PSL, ETP, VCR, DXR)]6),CEC 療法(CPA, CCNU, VDS, MEL, PSL, EPI, VCR, PCZ, VBL,BLM)7),BEACOPP 療法7)8)などの治療法はABVD 療法とのランダム化比較試験において,いずれの治療法もOS の改善は示されなかった。無増悪生存割合(PFS)ではABVD 療法より優れている治療法も報告されているが,治療強度を上げることにより有害事象は増強することが示されている。ダカルバジン(DTIC)の消化器毒性の軽減目的で考案されたABVd 療法(DTIC を2/3 に減量)の良好な治療成績が本邦から報告された9)。単アームの臨床第Ⅱ相試験であり,ABVD 療法との比較はなされていない。また,DTIC の消化器毒性は近年の制吐剤の進歩により軽減されてきている。
以上より進行期CHL における標準療法はABVD 療法と考えられる。投与回数は4 コースまでに完全奏効(CR)に至った症例は2 コース追加し6 コースで終了,6 コースまででCR に至った症例は2 コース追加し8 コースまで行うことが推奨されている。
【参考文献】
1) DeVita VT, et al. Curability of advanced Hodgkin’s disease with chemotherapy. Long-term follow-up of MOPP-treated patients at the National Cancer Institute. Ann Intern Med. 1980 ; 92(5) : 587-95.(3iiiDiii)
2) Canellos GP, et al. Chemotherapy of advanced Hodgkin’s disease with MOPP, ABVD, or MOPP alternating with ABVD. N Engl J Med. 1992 ; 327(21) : 1478-84.(1iiDiii)
3) Canellos GP, Niedzwiecki D. Long-term follow-up of Hodgkin’s disease trial. N Engl J Med. 2002 ; 346(18): 1417-8.(1iiDiii)
4) Duggan DB, et al. Randomized comparison of ABVD and MOPP/ABV hybrid for the treatment of advanced Hodgkin’s disease : report of an intergroup trial. J Clin Oncol. 2003 ; 21(4) : 607-14.(1iiDiii)
5) Gobbi PG, et al. ABVD versus modified stanford V versus MOPPEBVCAD with optional and limited radiotherapy in intermediate- and advanced-stage Hodgkin’s lymphoma : final results of a multicenter randomized trial by the Intergruppo Italiano Linfomi. J Clin Oncol. 2005 ; 23(36) : 9198-207.(1iiDiii)
6) Johnson PW, et al. Comparison of ABVD and alternating or hybrid multidrug regimens for the treatment of advanced Hodgkin’s lymphoma : results of the United Kingdom Lymphoma Group LY09 Trial (ISRCTN97144519). J Clin Oncol. 2005 ; 23(36) : 9208-18.(1iiDi)
7) Federico M, et al. ABVD compared with BEACOPP compared with CEC for the initial treatment of patients with advanced Hodgkin’s lymphoma : results from the HD2000 Gruppo Italiano per lo Studio dei Linfomi Trial. J Clin Oncol. 2009 ; 27(5) : 805-11.(1iiDiii)
8) Viviani S, et al. ABVD versus BEACOPP for Hodgkin’s lymphoma when high-dose salvage is planned. N Engl J Med. 2011 ; 365(3) : 203-12.(1iiDiii)
9) Ogura M,et al. Phase Ⅱ study of ABVd therapy for newly diagnosed clinical stage Ⅱ-Ⅳ Hodgkin lymphoma : Japan Clinical Oncology Group study (JCOG 9305). Int J Hematol. 2010 ; 92(5) : 713-24.(3iiiDiv)
| CQ8 | 進行期CHL において増量BEACOPP 療法はABVD 療法より臨床的に有用性が高いか |
|---|
-
推奨グレードカテゴリー2B
- 進行期CHL において増量BEACOPP 療法のABVD 療法に対する有用性は証明されていない。
【解 説】
BEACOPP 療法(BLM, ETP, DXR, CPA, VCR, PCZ, PSL)はGHSG が開発した治療強度を高めたレジメンである。GHSG は標準BEACOPP 療法(8 コース),増量BEACOPP 療法(8 コース),COPP(CPA, VCR, PCZ, PSL)/ABVD 療法(DXR, BLM, VBL, DTIC)(8 コース)の比較試験を報告した(HD9 試験)1)。対象は臨床病期ⅡB 以上で15~65 歳の進行期症例である。この臨床試験はABVD 療法類似のCOPP/ABVD 療法に比べBEACOPP 療法群(標準BEACOPP 療法,増量BEACOPP 療法)が5 年治療成功割合(FFTF)において有意に優っていることを示した。また,5 年全生存割合(OS)においても増量BEACOPP 療法がCOPP/ABVD 療法より優れていた。長期の観察においても同様の結果が得られている2)。しかし,進行期CHL の標準療法であるABVD 療法と当試験で採用されたCOPP/ABVD 療法が同等の有効性を示すかは不明である。急性期の有害事象は増量BEACOPP 療法にて高頻度に発生した。二次性MDS,AML の発症は標準BEACOPP 療法群と増量BEACOPP 療法群はCOPP/ABVD 療法群と比較して有意に頻度が高かった2)。その後,他のグループで行われたBEACOPP 療法の変法(4 コース増量レジメン+2 コース標準量レジメン,4 コース増量レジメン+4 コースの標準量レジメン)とABVD 療法の2 つの第Ⅲ相比較試験では,BEACOPP 療法(変法)はABVD 療法に対してOS で優位性が示されなかった3)4)。
以上の臨床試験研究から,増量BEACOPP 療法がABVD 療法に臨床的に優っていると結論することはできない。
高齢者(65 歳以上)を対象とした標準BEACOPP 療法とCOPP/ABVD 療法の比較試験では両群でFFTF,OS に有意差はなく,標準BEACOPP 療法群において血液毒性などの有害事象が高頻度で治療関連死亡(TRM)も多い傾向にあった。高齢者でのBEACOPP 療法の有用性は示されていない5)。
本邦で標準BEACOPP 療法の臨床第Ⅱ相試験が施行された。69 歳までの症例が対象であり,Grade 4 の好中球減少を約60%に認めたものの,90%近い3 年無増悪生存割合(PFS)が報告されている6)。
【参考文献】
1) Diehl V, et al. Standard and increased-dose BEACOPP chemotherapy compared with COPP-ABVD for advanced Hodgkin’s disease. N Engl J Med. 2003 ; 348(24) : 2386-95.(1iiDiii)
2) Engert A, et al. Escalated-dose BEACOPP in the treatment of patients with advanced-stage Hodgkin’s lymphoma : 10 years of follow-up of the GHSG HD9 study. J Clin Oncol. 2009 ; 27(27) : 4548-54.(1iiDiii)
3) Federico M, et al. ABVD compared with BEACOPP compared with CEC for the initial treatment of patients with advanced Hodgkin’s lymphoma : results from the HD2000 Gruppo Italiano per lo Studio dei Linfomi Trial. J Clin Oncol. 2009 ; 27(5) : 805-11.(1iiDiii)
4) Viviani S, et al. ABVD versus BEACOPP for Hodgkin’s lymphoma when high-dose salvage is planned. N Engl J Med. 2011 ; 365(3) : 203-12.(1iiDiii)
5) Ballova V, et al. A prospectively randomized trial carried out by the German Hodgkin Study Group(GHSG) for elderly patients with advanced Hodgkin’s disease comparing BEACOPP baseline and COPPABVD(study HD9elderly). Ann Oncol. 2005 ; 16(1) : 124-31.(3iiiDiii)
6) Niitsu N, et al. Multicentre phase Ⅱ study of the baseline BEACOPP regimen for patients with advancedstage Hodgkin’s lymphoma. Leuk Lymphoma. 2006 ; 47(9) : 1908-14.(3iiiDiii)
| CQ9 | 進行期CHL において国際予後スコアに従った治療法選択は必要か |
|---|
-
推奨グレードカテゴリー3
- 国際予後スコアによる治療層別化の有用性を示唆する根拠はない
【解 説】
国際予後スコア(International Prognostic Score:IPS)により,進行期CHL を低リスク,高リスク2 グループに分類できることが報告されている。スコア0~2 と3~7 で分けた場合,無増悪期間の差が明瞭に認められ,両群にほぼ同数の症例が分布することが報告されている1)。IPS のリスク分類に基づいて治療効果のサブグループ解析を行っている第Ⅲ相比較試験の結果がいくつか報告されている。
GHSG のHD9 の報告ではIPS スコア0~1,2~3,4~7 の3 グループに分類し,増量BEACOPP 療法(BLM, ETP, DXR, CPA, VCR, PCZ, PSL)群,標準BEACOPP 療法群,COPP/ABVD 療法(CPA, VCR, PCZ, PSL, DXR, BLM, VBL, DTIC)群の5 年治療成功割合(FFTF)と全生存割合(OS)を評価している2)。この3 つの予後グループのすべてでFFTF,OS ともCOPP/ABVD 療法と比較し増量BEACOPP が優っていることが示され,増量BEACOPP 療法はIPS のリスクグループによらず有効であるとされた。ABVD 療法(DXR, BLM, VBL, DTIC)とBEACOPP 療法(変法),CEC 療法(CPA, CCNU, VDS, MEL, PSL, EPI, VCR, PCZ, VBL, BLM)を比較したHD2000 試験3)およびMultidrug regimen とABVD 療法との比較試験4)では,IPS が高い群で高強度の治療がABVD 療法に比べ治療成功生存割合(FFS)が良好な傾向が認められたが,OS の改善は示されなかった。また,これらの研究はすべてサブ解析でありエビデンスレベルは高くない。このようにIPS の特定のリスクグループで特定の治療法が有用であるという結果は示されていない。IPS での治療層別化の有用性については今後なお検証が必要であるが,現時点では推奨されない。
【参考文献】
1) Hasenclever D, et al. A prognostic score for advanced Hodgkin’s disease. International Prognostic Factors Project on Advanced Hodgkin’s Disease. N Engl J Med. 1998 ; 339(21) : 1506-14.(3iiiDiii)
2) Diehl V, et al. Standard and increased-dose BEACOPP chemotherapy compared with COPP-ABVD for advanced Hodgkin’s disease. N Engl J Med. 2003 ; 348(24) : 2386-95.(1iiDiii/2Diii)
3) Federico M, et al. ABVD compared with BEACOPP compared with CEC for the initial treatment of patients with advanced Hodgkin’s lymphoma : results from the HD2000 Gruppo Italiano per lo Studio dei Linfomi Trial. J Clin Oncol. 2009 ; 27(5) : 805-11.(1iiDiii/2Diii)
4) Johnson PW, et al. Comparison of ABVD and alternating or hybrid multidrug regimens for the treatment of advanced Hodgkin’s lymphoma : results of the United Kingdom Lymphoma Group LY09 Trial (ISRCTN97144519). J Clin Oncol. 2005 ; 23(36) : 9208-18.(1iiDi/2Di)
| CQ10 | 進行期CHL で化学療法によりCR(CT 効果判定)に至った症例において地固め療法としてのIFRT は必要か |
|---|
-
推奨グレードカテゴリー4
- 進行期CHL で化学療法によりCR(CT 効果判定)が得られた症例に対する IFRT は推奨されない。
【解 説】
これまでのCHL に対する多くの臨床試験での治療効果判定はCT で行われている。化学療法後に効果判定をCT で行い完全奏効(CR),部分奏効(PR)が得られた症例における地固め療法としての照射の意義についての検討結果が報告されている。化学療法でCR を得た症例に対するinvolved field radiotherapy(IFRT)追加の有用性に関してはEORTC から第Ⅲ相比較試験が報告されている。MOPP(HN2, VCR, PCZ, PSL)/ABV(DXR, BLM, VBL) hybrid 療法で治療された進行期CHL 739 症例でCR となった症例が地固め目的のIFRT(24 Gy)施行群と観察群に割り付けられた。両群において5 年無イベント生存割合(EFS)に有意差は認められなかった1)。この臨床試験の長期観察においても同様の結果が得られている2)。Southwest Oncology Group (SWOG)からも化学療法後CR 例をIFRT 追加群と観察群に割り付けた臨床試験結果が報告されている。この試験においてもIFRT の追加による無再発生存割合(RFS),全生存割合(OS)の改善は示されなかった3)。また,治療終了後の効果判定目的のPET のnegative predictive value(NPV)は良好であり4)5),比較試験の結果はないが,PET 判定によるCR 例にIFRT を追加することは推奨されない。以上より,進行期CHL においてCR(CT およびPET での診断)を示した症例に対する地固め療法目的のIFRT は推奨されない。
PR 例に対するIFRT 追加の有用性を検討した比較試験は報告されていない。前述のEORTC の臨床試験においてPR 例に30 Gy のIFRT が施行されていた1)2)。そのOS とEFS はCR 例と有意差がなかった。進行期CHL において初回化学療法後(IFRT なし)のPR 例はCR 例と比べ再発割合が高いと報告されており,このEORTC の報告はPR 例にIFRT を施行することにより,CR 例と同等のEFS をもたらしていることを示した。このことから,初回化学療法後のPR 例に対するIFRT 追加の有用性が示唆される。
【参考文献】
1) Aleman BM, et al. Involved-field radiotherapy for advanced Hodgkin’s lymphoma. N Engl J Med. 2003 ; 348(24) : 2396-406.(1iiDii)
2) Aleman BM, et al. Involved-field radiotherapy for patients in partial remission after chemotherapy for advanced Hodgkin’s lymphoma. Int J Radiat Oncol Biol Phys. 2007 ; 67(1) : 19-30.(2Di)
3) Fabian CJ, et al. Low-dose involved field radiation after chemotherapy in advanced Hodgkin disease. A Southwest Oncology Group randomized study. Ann Intern Med. 1994 ; 120(11) : 903-12.(1iiDiii)
4) Kobe C, et al. Positron emission tomography has a high negative predictive value for progression or early relapse for patients with residual disease after first line chemotherapy in advanced-stage Hodgkin lymphoma. Blood. 2008 ; 112(10) : 3989-94.(2Diii)
5) Terasawa T, et al. 18F-FDG PET for posttherapy assessment of Hodgkin’s disease and aggressive Non-Hodgkin’s lymphoma : a systematic review. J Nucl Med. 2008 ; 49(1) : 13-21.
| CQ11 | 若年者再発CHL に対して自家造血幹細胞移植併用大量化学療法は有効か |
|---|
-
推奨グレードカテゴリー2A
- 若年者初回再発CHL では,救援化学療法に対して感受性が認められた場合,自家造血幹細胞移植併用大量化学療法は推奨される治療法である。
【解 説】
再発時は救援化学療法を施行する。救援化学療法レジメンは非ホジキンリンパ腫と基本的に変わりはない。Dexa-BEAM 療法[DEX, BCNU(国内未承認),ETP, AraC, MEL]1),Mini-BEAM 療法[BCNU(国内未承認),ETP, AraC, MEL]2),ICN 療法(IFM, CBDCA, ETP)3),ESHAP 療法(ETP, mPSL, AraC, CDDP)4)等が比較的高頻度に選択される救援療法レジメンであり,いずれも奏効割合は70%以上である。
再発CHL に対する通常量の救援化学療法と自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)の比較に関する臨床試験結果が報告されている。GHSG とEuropean Group for Blood and Marrow Transplantation (EBMT)の共同研究として,救援療法(Dexa-BEAM 療法)を4 コース施行する群とDexa-BEAM 療法2 コース後にHDC/AHSCT(大量化学療法:BEAM)を施行する群との比較試験が行われた。化学療法感受性があると判断された症例を対象にした場合,治療成功割合がHDC/AHSCT 群で有意に優れていた。全生存割合(OS)における有意差は認められなかった。ただし,複数再発以降の症例ではHDC/AHSCT は優位性が示されていない。また,British Lymphoma National Investigation(BLNI)での比較試験は40 例のみの登録で早期終了となっているが,無イベント生存割合(EFS)と無増悪生存割合(PFS)においてHDC/AHSCT が良好な傾向を示した5)。Stanford 大学からは後方視的解析でHDC/AHSCT の有用性(初回再発または初回非奏効例)を示した研究も報告されている6)。以上より65 歳以下のCHL の初回再発で救援化学療法に感受性がある場合,HDC/AHSCT は推奨される治療法である。ただし,初発時限局期で短縮化学療法を用いたCMT により治療された症例の再発においては,HDC/AHSCT の有用性のエビデンスはないため,適応は慎重に判断されなければならない。
【参考文献】
1) Schmitz N, et al. Aggressive conventional chemotherapy compared with high-dose chemotherapy with autologous haemopoietic stem-cell transplantation for relapsed chemosensitive Hodgkin’s disease : a randomised trial. Lancet. 2002 ; 359(9323) : 2065-71.(1iiDiii)
2) Martín A, et al. Long-term follow-up in patients treated with Mini-BEAM as salvage therapy for relapsed or refractory Hodgkin’s disease. Br J Haematol. 2001 ; 113(1) : 161-71.(3iiiDiii)
3) Moskowitz CH, et al. A 2-step comprehensive high-dose chemoradiotherapy second-line program for relapsed and refractory Hodgkin disease : analysis by intent to treat and development of a prognostic model. Blood. 2001 ; 97(3) : 616-23.(3iiiDi)
4) Aparicio J, et al. ESHAP is an active regimen for relapsing Hodgkin’s disease. Ann Oncol. 1999 ; 10(5) : 593-5.(3iiiDiv)
5) Linch DC, et al. Dose intensification with autologous bone-marrow transplantation in relapsed and resistant Hodgkin’s disease : results of a BNLI randomised trial. Lancet. 1993 ; 341(8852) : 1051-4.(3iiiDi)
6) Yuen AR, et al. Comparison between conventional salvage therapy and high-dose therapy with autografting for recurrent or refractory Hodgkin’s disease. Blood. 1997 ; 89(3) : 814-22.(3iiiDi)
| CQ12 | 進行期CHL において初回治療中間でのPET 検査(interim PET)は予後予測に有用か |
|---|
-
推奨グレードカテゴリー2A
- Interim PET は進行期CHL の予後予測に有用であるが,日常診療においてはその結果を治療介入の根拠とすることは推奨されない。
【解 説】
CHL においては治療中間でのPET 所見(interim PET)の改善が予後予測に有効であると報告されている。これら研究の多くは初発進行期CHL で6~8 コースの化学療法を施行した症例を対象としてinterim PET を前方視的に評価している。ほとんどの試験でのinterim PET 評価は2 コース後に施行されている。最も多くの症例が登録され解析された研究はGallamini 等により報告されており(260 例:病期ⅡB-Ⅳおよび予後不良因子を有するⅡA),interim PET の陰性症例と陽性症例の2 年の無増悪生存割合(PFS)はそれぞれ95%と12.8%と有意差がみられた1)。CHL におけるinterim PET の予後予測(進行および再発を評価)におけるメタアナリシスでは,感度および特異度はそれぞれ81%と97%であった2)。しかし,限局期症例でCMT にて治療された場合のpositive predictive value(PPV)は15%と不良であるとの報告もある3)。進行期と比べ限局期ではinterim PET のPPV は不良である傾向があるため注意を要する。Interim PET は一般的にPET 効果判定に用いられるInternational Harmonization Project in Lymphoma の規準を使用する4)。近年,interim PET に特化した判定方法が報告されているが,未だ研究段階である5)。また,interim PET の結果を治療介入に用いる手法は臨床試験中であり,一般臨床では推奨されない6)。
【参考文献】
1) Gallamini A, et al. Early interim 2-fluoro-2-deoxy-D-glucose positron emission tomography is prognostically superior to international prognostic score in advanced-stage Hodgkin’s lymphoma : a report from a joint Italian-Danish study. J Clin Oncol. 2007 ; 25(24) : 3746-52.(3iiiDiii)
2) Terasawa T, et al. Fluorine-18-fluorodeoxyglucose positron emission tomography for interim response assessment of advanced-stage Hodgkin’s lymphoma and diffuse large B-cell lymphoma : a systematic review. J Clin Oncol. 2009 ; 27(11) : 1906-14.
3) Sher DJ, et al. Prognostic significance of mid- and post-ABVD PET imaging in Hodgkin’s lymphoma : the importance of involved-field radiotherapy. Ann Oncol. 2009 ; 20(11) : 1848-53.(3iiiDiii)
4) Juweid ME, et al. Use of positron emission tomography for response assessment of lymphoma : consensus of the Imaging Subcommittee of International Harmonization Project in Lymphoma. J Clin Oncol. 2007 ; 25(5) : 571-8.
5) Meignan M, et al. Report on the Second International Workshop on interim positron emission tomography in lymphoma held in Menton, France, 8-9 April 2010. Leuk Lymphoma. 2010 ; 51(12) : 2171-80.
6) Gallamini A, et al. Early chemotherapy intensification with BEACOPP in advanced-stage Hodgkin lymphoma patients with a interim-PET positive after two ABVD courses. Br J Haematol. 2011 ; 152(5) : 551-60.(3iiiDiii)
| 追加CQ | 再発・難治性CD30陽性CHLに対してブレンツキシマブベドチンは有効か |
|---|
-
推奨グレードカテゴリー2B
- ブレンツキシマブベドチンは再発・難治性CD30 陽性CHL に対して高い奏効率が報告されており、治療法の一つとして考慮される。
【解 説】
ブレンツキシマブベドチンは、CD30 を標的とする抗体薬物複合体であり、第Ⅰ相試験にてCD30 陽性の再発・難治性CHL 患者において有効性が報告された1)。自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation: HDC/AHSCT)の治療歴を有する再発または難治性CD30 陽性CHL 患者102 例を対象とした第Ⅱ相多施設共同試験では、全奏効割合は75%であり、34%の症例で完全奏効(CR)が得られた。全患者における無増悪生存期間の中央値は5.6 ヵ月であり、CR が得られた症例の奏効期間の中央値は20.5 ヵ月であった2)。本邦では第Ⅰ/Ⅱ相試験が施行され、再発または難治性CD30 陽性CHL 患者14 例における全奏効割合は67%(CR;56%)であった。3)
再発・難治性のCD30 陽性CHL においては、HDC/AHSCT が不成功であった患者およびHDC/AHSCT の適応にかかわらず2 レジメン以上の化学療法による前治療が不成功であった患者の治療選択肢として、ブレンツキシマブベドチンが考慮される。
【参考文献】
1) Younes A, et al. Brentuximab Vedotin (SGN 35) for Relapsed CD30 Positive Lymphomas. N Engl J Med 2010(363)1812 21.(3ⅲDⅳ)
2) Younes A, et al. Results of a Pivotal Phase II Study of Brentuximab Vedotin for Patients With Relapsed or Refractory Hodgkin's Lymphoma. J Clin Oncol 2012(30)2183 9.(3ⅲDⅳ)
3) Ogura M, et al.Phase I/II study of brentuximab vedotin in Japanese patients with relapsed or refractory CD30-positive Hodgkin's lymphoma or systemic anaplastic large-cell lymphoma.Cancer Sci. 2014 (105):840-6.(3ⅲDiv)