�X����@�`�f�ÃK�C�h���C��
�K�C�h���C�������̕����ԍ�����C�Y�����镶�����X�g�փ����N����܂�
1 �f�f�@
CQ 1-1�@�X���̃��X�N�t�@�N�^�[�Ƃ͉����H
| ����
|
|
|---|
�� �G�r�f���X
�X�����҂�3�`9�����X���̉Ƒ���������C���̏ꍇ���X���̑����X�N��1.6�`3.4 �{�ł��� 1�j�i���x��Ⅰ�j2�j�i���x��Ⅳa�j�B�킪���ł̃��X�N�����ĂƂقړ����ł��� 3, 4�j�i���x��Ⅳb�j�B���x�ߐe�ҁi���e�C�Z��o���C�q�j��2 �l�ȏ���X���늳�҂�����Ƒ����X���ƌn�̕W�����늳��͈�ʐl����6.79 �{�ŁC�U�����X���ƌn��2.41 �{�Ɣ�ׂėL�ӂɍ����C�Ƒ����X���ƌn��50 �Ζ����̎�N���ǂ�����ꍇ�ɂ͂���Ƀ��X�N���オ�� 2�j�i���x��Ⅳa�j�B�Ƒ����X���C��`���X���C�Ƒ����咰�B��ǁC��`����|���|�[�V�X�咰���iLynch �nj�Q�j�CPeutz-Jeghers �nj�Q�C�Ƒ����ٌ^����������F��nj�Q�ifamilial atypical multiple mole melanoma�GFAMMM�j�C��`�������������nj�Q�ihereditary breast and ovarian cancer syndrome�GHBOC�j�͈�`���X���nj�Q�ƌĂ�C�X�������������� 5, 6�j�i���x��Ⅰ�j7�j�i���x��Ⅳa�j�B
�킪�����X���o�^�� 3�j�i���x��Ⅳb�j�ɂ��ƁC�X�����҂̊������ł͓��A�a��25.9���ƍł��p�x�������C���A�a�ɂ������X�����X�N�͖�2 �{�ł��� 8�j�i���x��Ⅰ�j�B�X���̔��ǂ͓��A�a�̔���1�`3�N�ȓ��ōł����� 8�j�i���x��Ⅰ�j�C���A�a�̐V�K���ǂ��X�������̃}�[�J�[�ƂȂ蓾��B�얞�͓��A�a�ɂ������X�����X�N�������� 9�j�i���x��Ⅳa�j�B���A�a�ɂ������X���̔����ɂ͍��C���X�������� 10�j�i���x��Ⅰ�j�C�C���X������R�� 11�j�i���x��Ⅳa�j�Cinsulin-like growth factor�iIGF�j�̈�`�q���^ 12�j�i���x��Ⅳb�j���֗^���Ă���Ƃ̕�����B���A�a�̎��ÂƂ��ăC���X�����A�i���O��C���X�������呣�i����X�����X�N�������邪�C���g�t�H���~�����X���̔����Ǝ��S����ቺ������ 13�j�i���x��Ⅰ�j�B
�얞���X���ɂ��āC�킪���ōs��ꂽ��K�̓R�z�[�g�����ɂ��ƁC20 �Α��body mass index�iBMI�j��30kg/m2�ȏ�̒j���ł́C����BMI�ɔ���X���댯����3.5 �{�������邱�Ƃ������ꂽ 14�j�i���x��Ⅳa�j�B����C�ق���2 �̃R�z�[�g�����ł��X����BMI �ɑ��ւ��F�߂��Ă��Ȃ� 15, 16�j�i���x��Ⅳa�j�B���O���ł́CBMI ��5kg/m2 ����������X���댯����1.12 �{�㏸����Ƃ̕����� 17�j�i���x��Ⅰ�j�B�܂��C�X���댯����BMI 35kg/m2 �ȏ��2.61 �{�C�����ł�BMI 40kg/m2 �ȏ��2.76 �{�ƒ������� 18�j�i���x��Ⅳa�j�B���Ɏ�N���ɉߑ̏d��얞�ł���ꍇ�ɂ��X�����X�N���ł��������� 19�j�i���x��Ⅳb�j�B
�����X��������X�������p�x�͖�5���ŁC�킪���ɂ����锭���p�x��4.1���ƕ���Ă��� 20�j�i���x��Ⅳb�j�B�����X�����X���������͈�ʐl���ɔ��13 �{�������C2 �N�ȓ����X���Ɛf�f���ꂽ���̂�������5.8 �{�ł��� 5�j�i���x��Ⅰ�j�B
��`���X���́C�u����ƌn��2 ����ȏ�ɂ킽�蕡�����X�����҂����āC��N���ǂŒ_��A���R�[���̊֗^���Ȃ��X���v�ƒ�`�����B��`���X����60�`70���ɁC�J�`�I�j�b�N�g���v�V�m�[�Q���iPRSS1�j��`�q��p.R122H �ψق��邢��p.N29I �ψق��F�߂��� 7�j�i���x��Ⅳa�j�B�X���̗ݐσ��X�N��50 ��75 �ł��ꂼ��10.0���C53.5���ŁC��ʐl������60�`87 �{�����ł��� 5�j�i���x��Ⅰ�j7�j�i���x��Ⅳa�j�B
�X�Ǔ������S�t����ᇁiintraductal papillary mucinous neoplasm�GIPMN�j���X���̔�����n�ł���\������������Ă���B���{�X���w��ɂ��킪���̏W�v�ł́CIPMN �ɗR������Z�����͎��X�nj^IPMN �ɑ����C�g�D�^�ł͔S�t������1/3 ���߁CIPMN �ɕ��������ʏ�^�X�NJ��͕��}�^IPMN �ɑ����C�g�D�^�͊Ǐ�B������1/3 ���߂� 21�j�i���x��Ⅳb�j�B�܂��C�Ǎ��߂̂Ȃ����}�^IPMN 349 �l��1�`16.3 �N�Ԍo�ߊώ@�������{���������ł́C62�l�i17.8���j��嚢�E�a�C���X�nja�C�Ǎ��߂̑���Ȃǂ̌`�Ԋw�I�ω�������C�X�؏�����22 �ᒆ9 �l�����C13 �l���B��ł���CIPMN �Ƃ͗��ꂽ���ʂł��X���̔�����2���ɔF�߂�ꂽ 22�j�i���x��Ⅳa�j�B���}�^IPMN �ɂ��āC1cm �����̕��}�^IPMN 60 ���87 �J���o�ߊώ@�������ʁCIPMN �̕��ʂ�2 ��i3���j�CIPMN �Ƃ͗��ꂽ���ʂ�5 ��i8���j�����������C�N�Ԃ��X����������1.1���ŁC70 �Έȏ���X���̔�������19.5����69 �Έȉ���荂�����Ƃ����ꂽ 23�j�i���x��Ⅳa�j�B�O�ȓI�؏����{�s���ꂽIPMN 283 �l�ɂ�����IPMN �̑g�D�w�I�����ނƗՏ��a���w�I�����̌����ł́C���}�^IPMN ��gastric type�C���X�nj^��intestinal type �̕p�x�������C�Ǐ�B���̔�����pancreatobiliary type ���ł������C5 �N���������ł��s�ǂł������ƕ��ꂽ 24�j�i���x��Ⅳb�j�BIPMN �Ɛf�f����Ȃ��X嚢�E�ɑ��Ă��C���}�^IPMN 80 ��Ɣ�IPMN 嚢�E117 ���3.8 �N�ǐՂ��������ł́CIPMN �̊�����2 ��C�Z���^�X�NJ���5 ��F�߁C���̂�����IPMN 嚢�E��3 �Ⴉ���X�����������C�X嚢�E���҂��X���������X�N�͈�ʐl����22.5 �{�ł��邱�Ƃ����ꂽ 25�j�i���x��Ⅳa�j�B���������āCIPMN �݂̂Ȃ炸IPMN �Ɛf�f����Ȃ��X嚢�E�ɂ��Ă��X���̍����X�N�Q�Ƃ��ĐT�d�Ȍo�ߊώ@���K�v�ł���B
�i�����X���̃��X�N�������邱�Ƃ͑����̕łقڈ�v���������ł���B�i���ɂ���X���̃n�U�[�h���1.3 �` 3.9 �� 15, 16, 26�j�i���x��Ⅳa�j27�j�i���x��Ⅰ�j�C�i���{����40 �{/ ���ȏ�̒j�����X���ɂ�鎀�S��3.3 �{�ɑ������邱�Ƃ������ꂽ 26�j�i���x��Ⅳa�j�B�։���10 �N�ȏ�ł��X���̃��X�N�͍��� 27�j�i���x��Ⅰ�j�B�i���͈�`���X���ⓜ�A�a�C�얞�Ȃǂ̑��̊댯���q�ɂ���X���̔������X�N�������� 5�j�i���x��Ⅰ�j7, 15�j�i���x��Ⅳa�j�B
�A���R�[�����X���̃��X�N�ł��邩�ۂ��͕ɂ���ĈقȂ�B�ŋ߂̃��^�A�i���V�X��O���������ɂ���X�������̑����X�N�́C�K�ʂ̈����ł̓��X�N�̑����͔F�߂��Ȃ����C�A���R�[��3 �h�����N�ȏ�i1 �h�����N���G�^�m�[��12.5g�j�̑��ʈ����҂ł��X���̃��X�N��1.2�{��������ƕ���Ă��� 28�j�i���x��Ⅰ�j�B
ABO ���t�^���X���ɂ��ĉ��Đl��ΏۂƂ��������ł́CO �^�ɔ�ׂĔ�O �^�̐l���X���̕p�x���L�ӂɍ��� 29�j�i���x��Ⅰ�j���C���{�l�ł����l�Ȍ��ʂ��͕s���ł���B�w���R�o�N�^�[�E�s�����������X�����X�N��������Ƃ���������C�w���R�o�N�^�[�E�s�����ɑ��錌���w�I�z�����X�������ɂ��Ẵ��^�A�i���V�X�ł͊֘A��������Ƃ������ʂ�������Ă��� 30�j�i���x��Ⅰ�j�B�č��̑�K�̓R�z�[�g�����ł́C��������ᇂ̂Ȃ��l�ɔ�ׂĈݒ�ᇂ̊���������ꍇ���X���������X�N��1.83�{�������C�\��w����ᇂ̊������X�����X�N�Ƃ̊֘A���͂Ȃ��������Ƃ����ꂽ 31�j�i���x��Ⅳa�j�BB �^�̉��E�C���X�����ɂ����āCHBs �R���z���҂̂����CHBe �R���z���CHBV-DNA �����l�̏ꍇ���X�����X�N����������Ƃ��������� 32�j�i���x��Ⅳa�j�B�E�Ƃ̕���ł͉��f���Y�����f�ւ̖\�I�Ɋւ��E�ƂŃ��X�N����������\�������� 33�j�i���x��Ⅰ�j�B
��`���X���nj�Q��Ƒ����X���̍����X�N�Q�ɑ���O���������ŁC���̌����CEUS�CMRI/MRCP �ɂ��6�`12 �J�����Ƃ̃X�N���[�j���O�����͑O���a�ς�؏��\�X���̔����ɗL�p�ł���Ƃ̕����� 34-36�j�i���x��Ⅳa�j�B�������C�����Ԃ̌o�ߊώ@�ƂȂ�̂ŁC��p�Ό��ʂƐ��_�I�ȕ��S�ɂ��Ă��\���l������K�v������ 35, 36�j�i���x��Ⅳa�j�B�܂��C�X���̊�����������ꍇ�C���ǂ���3 �N�ȓ����X�����X�N�������̂ŁC�X���Ɛf�f�����ꍇ�ɂ��X����O���ɓ���ĐT�d�ɐ������ׂ��ł��� 37�j�i���x��Ⅳb�j�B
�� �����ւ̒�
����f�Âɂ����āC�Ƒ����C�������C�i�����C������Ȃǂ��ڍׂɒ��悵�C�X���̃��X�N�t�@�N�^�[���E���グ�邱�Ƃ��C�X���̑��������̑����ł���B��`���X���nj�Q�C��`���X���Ȃǂ̈�`�������C�Ƒ����X���C�����X���CIPMN ���X���̑O���a�ς��`������\��������̂ŁC���̌�����摜�����ɂ�����I�Ȍ��f�����߂���B���f�̕��@�ɂ��Ă͊m�����ꂽ���̂͂Ȃ����C��p�Ό��ʂ̂悢���́C���҂̐��_�I���S�����Ȃ����̂��]�܂����B���A�a���X�������̃}�[�J�[�Ƃ��Ē��ӂ�v����̂ŁC���A�a��f�Â����t�ƍL���m�������L���邱�Ƃ��d�v�ł���B�얞�C�i���C���ʈ������X�����X�N�����߂���q�ł���̂ŁC���Ɉ�`�I�w�i�⍇�������̂����X���̍����X�N�Q�ɑ��āC��N���l����̔얞�̗\�h�C�։��C�K�ʔ͈͓��̈����Ȃǂ̐����K���̎w�����d�v�ł���B
�� ���p����
1�j Permuth-Wey J, Egan KM. Family history is a significant risk factor for pancreatic cancer�Fresults from a systematic review and meta-analysis. Fam Cancer 2009�G8�F109-117.
2�j Brune KA, Lau B, Paimisano E, et al. Importance of age of onset in pancreatic cancer kindreds. J Nat Cancer Inst 2010�G102�F119-126.
3�j ���{�X���w���X���o�^�ψ���D�X���o�^��2007�D�X�� 2007�G22�Fe1-e94.
4�j Matsubayashi H, Maeda A, Kanemoto H, et al. Risk factors of familial pancreatic cancer in Japan�Fcurrent smoking and recent onset of diabetes. Pancreas 2011�G40�F974-978.
5�j Raimondi S, Lowenfels AB, Morselli-Labate AM, et al. Pancreatic cancer in chronic pancreatitis�Gaetiology, incidence, and early detection. Best Prac Res Clin Gastroenterol 2010�G24�F349-358.
6�j van Lier MG, Wagner A, Mathus-Vliegen EM, et al. High cancer risk in Peutz-Jeghers syndrome�Fa systematic review and surveillance recommendations. Am J Gastroenterol 2010�G105�F1258-1264.
7�j Rebours V, Boutron-Ruault MC, Schnee M, et al. Risk of pancreatic adenocarcinoma in patients with hereditary pancreatitis�Fa national exhaustive series. Am J Gastroenterol 2008�G103�F111-119.
8�j Ben Q, Xu M, Ning X, et al. Diabetes mellitus and risk of pancreatic cancer�FA meta-analysis of cohort studies. Eur J Cancer 2011�G47�F1928-1937.
9�j Meinhold CL, Berrington de Gonzalez A, Albanes D, et al. Predictors of fasting serum insulin and glucose and the risk of pancreatic cancer in smokers. Cancer Causes Control 2009�G20�F681-690.
10�j Guh DP, Zhang W, Bansback N, et al. The incidence of co-morbidities related to obesity and overweight�Fa systematic review and meta-analysis. BMC Public Health 2009�G9�F88.
11�j Stolzenberg-Solomon RZ, Graubard BI, Chari S, et al. Insulin, glucose, insulin resistance, and pancreatic cancer in male smokers. JAMA 2005�G294�F2872-2878.
12�j Suzuki H, Li Y, Dong X, et al. Effect of insulin-like growth factor gene polymorphisms alone or in interaction with diabetes on the risk of pancreatic cancer.Cancer Epidemiol Biomarkers Prev 2008�G17�F3467-3473.
13�j Decensi A, Puntoni M, Goodwin P, et al. Metformin and cancer risk in diabetic patients�Fa systematic review and meta-analysis.Cancer Prev Res�iPhila�j2010�G3�F1451-1461.
14�j Lin Y, Kikuchi S, Tamakoshi A, et al. Obesity, physical activity and the risk of pancreatic cancer in a large Japanese cohort. Int J Cancer 2007�G120�F2665-2671.
15�j Luo J, Iwasaki M, Inoue M, et al. Body mass index, physical activity and the risk of pancreatic cancer in relation to smoking status and history of diabetes�Fa large-scale population-based cohort study in Japan--the JPHC study. Cancer Causes Control 2007�G18�F603-612.
16�j Nakamura K, Nagata C, Wada K, et al. Cigarette smoking and other lifestyle factors in relation to the risk of pancreatic cancer death�Fa prospective cohort study in Japan. Jpn J Clin Oncol 2011�G41�F225-231.
17�j Larsson SC, Orsini N, Wolk A. Body mass index and pancreatic cancer risk�FA meta-analysis of prospective studies. Int J Cancer 2007�G120�F1993-1998.
18�j Stolzenberg-Solomon RZ, Adams K, Leitzmann M, et al. Adiposity, physical activity, and pancreatic cancer in the National Institutes of Health-AARP Diet and Health Cohort. Am J Epidemiol 2008�G167�F586-597.
19�j Li D, Morris JS, Liu J, et al. Body mass index and risk, age of onset, and survival in patients with pancreatic cancer.JAMA 2009�G301�F2553-62.
20�j �c����v�C��c����C������O. �����X�����X���̊֘A���ɂ��Ă̒�������. �����J���ȉȊw������⏕���E������������������� 2009�G����X�����Ɋւ��钲�������i����20 �N�x �����E���S�������j�F155-160.
21�j Yamaguchi K, Kanemitsu S, Hatori T, et al. Pancreatic ductal adenocarcinoma derived from IPMN and pancreatic ductal adenocarcinoma concomitant with IPMN. Pancreas 2011�G40�F571-580.
22�j Maguchi H, Tanno S, Mizuno N, et al. Natural history of branch duct intraductal papillary mucinous neoplasms of the pancreas�Fa multicenter study in Japan. Pancreas 2011�G40�F364-370.
23�j Uehara H, Nakaizumi A, Ishikawa O, et al. Development of ductal carcinoma of the pancreas during follow-up of branch duct intraductal papillary mucinous neoplasm of the pancreas. Gut 2008�G57�F1561-1565.
24�j Furukawa T, Hatori T, Fujita I, et al. Prognostic relevance of morphological types of intraductal papillary mucinous neoplasms of the pancreas. Gut 2011�G60�F509-516.
25�j Tada M, Kawabe T, Arizumi M, et al. Pancreatic cancer in patients with pancreatic cystic lesions�Fa prospective study in 197 patients. Clin Gastroenterol Hepatol 2006�G4�F1265-1270.
26�j Qiu D, Kurosawa M, Lin Y, et al. Overview of the epidemiology of pancreatic cancer focusing on the JACC Study. J Epidemiol 2005�G15�FS157-S167.
27�j Iodice S, Gandini S, Maisonneuve P, et al. Tobacco and the risk of pancreatic cancer�Fa review and meta-analysis. Langenbecks Arch Surg 2008�G393�F535-545.
28�j Tramacere I, Scotti L, Je Nab M, et al. Alcohol drinking and pancreatic cancer risk�Fa meta-analysis of the dose-risk relation. Int J Cancer 2010�G126�F1474-1486.
29�j Iodice S, Maisonneuve P, Botteri E, et al. ABO blood group and cancer. Eur J Cancer 2010�G46�F 3345-3350.
30�j Trikudanathan G, Philip A, Dasanu CA, et al. Association between Helicobacter pylori infection and pancreatic cancer. A cumulative meta-analysis. JOP 2011�G12�F26-31.
31�j Bao Y, Spiegelman D, Li R, et al. History of peptic ulcer disease and pancreatic cancer risk in men.Gastroenterology 2010�G138�F541-549.
32�j Iloeje UH, Yang HI, Jen CL, et al. Risk of pancreatic cancer in chronic hepatitis B virus infection�Fdata from the REVEAL-HBV cohort study. Liver Int 2010�G30�F423-429.
33�j Ojajäevi A, Partanen T, Ahlbom A, et al. Estimating the relative risk of pancreatic cancer associated with exposure agents in job title data in a hierarchical Bayesian meta-analysis. Scand J Work Environ Health 2007�G33�F325-335.
34�j Poley JW, Kluijt I, Gouma DJ, et al. The yield of first-time endoscopic ultrasonography in screening individuals at a high risk of developing pancreatic cancer. Am J Gastroenterol 2009�G104�F2175-2181.
35�j Langer P, Kann PH, Fendrich V, et al. Five years of prospective screening of high-risk individuals from families with familial pancreatic cancer. Gut 2009�G58�F1410-1418.
36�j Vasen HFA, Wasser M, van Mil A, et al. Magnetic resonance imaging surveillance detects early- stage pancreatic cancer in carriers of a p16-Leiden mutation. Gastroenterology 2011�G140�F850-856.
37�j Bracci PM, Wang F, Hassan MM, et al. Pancreatitis and pancreatic cancer in two large pooled case-control studies. Cancer Causes Control 2009�G20�F1723-1731.
CQ 1-2�@�X���̔����͂ǂ̂悤�ɂ�����悢���H
| ����
|
|
|---|
�� �G�r�f���X
- �Ǐ�
�����Ǐ�Ƃ��ĕ��ɁC���t�C���w���ɂ������C�����ő̏d�����C�����s�ǂȂǂ����� 1-3�j�i���x��Ⅳb�j�B�X���̋Ǎݕ��ʂɂ�錟���ł́C�������ł̏Ǐ����������C���ɂ�64���C���t��63���C�̏d������53���݂��C�̕����ł͕��ɂ�93���ƍł����� 4�j�i���x��Ⅳb�j�B�X������305 ��ɑ���ʐڒ����ɂ��C���ɂ≩�t�����ǂ���6 �J���ȏ�O�ɁC�H�~�ቺ�i4.6���j�C�R�[�q�[��i���C���C���������ɂȂ�Ƃ����n�D�̕ω��i3.6���j���C�Ώ�305 ��ɔ�חL�ӂɑ����F�߂� 5�j�i���x��Ⅳb�j�B�킪�����X���W�v�ɂ��ƁC�����Ǐ�̂Ȃ��X����15.4���ł��� 2�j�i���x��Ⅳb�j�C2cm �ȉ����X���Ɍ���Ə����Ǐ�Ƃ��ĕ��ɂ�24.5���ƍł��������C18.1�������Ǐ�ł����� 6�j�i���x��Ⅳb�j�B�Ö������ǐ��NJ��҂ł��X���̃��X�N��6 �{���� 7�j�i���x��Ⅰ�j�B���^�A�i���V�X�ɂ��Ɠ��A�a���X����60�`81���ɍ������C���������A�a�f�f��2 �N�ȓ����X���Ɛf�f���ꂽ 8�j�i���x��Ⅰ�j�B�X������187 ��ł̌����œ��A�a�̍�����48 ��i29.3���j�ɔF�߁C���̂�����s2 �N�ȓ���21/40 ��i52.5���j�C��s5 �N�ȏオ14/40 ��i35���j�ɂ݂�ꂽ 9�j�i���x��Ⅳb�j�B2cm �ȉ����X���ł͓��A�a�̑�����8���ɔF�߂�ꂽ 6�j�i���x��Ⅳb�j�B50 �Έȏ�̓��A�a��������2,122 ����0.85����3 �N�ȓ����X���ǂ����Ƃ����� 10�j�i���x��Ⅳa�j��C55 �Έȍ~�ɓ��A�a�ǂ��C���A�a�����C�̏d�����C�����A�~���[�[�㏸�CCA19-9 �㏸�CUS ���X�_���n�ُ̈�̂����ꂩ��F�߂����_��ERCP ���s�����Ƃ���C7�����X���Ɛf�f����C���ɓ��A�a����3 �N�ȓ��̌Q�ł�13.9�����X���Ɛf�f���ꂽ�Ƃ̕� 11�j�i���x��Ⅳb�j������B�܂����A�a���ǎ����X����f�f����ΐ؏��\�ł���\���������Ƃ̕����� 12�j�i���x��Ⅳb�j�B
- �����X�y�f
�X�^�A�~���[�[�C���p�[�[�C�G���X�^�[�[1�C�g���v�V���Ȃǂ��X���ɓ��ٓI�ł͂Ȃ��B�X���ł̌����A�~���[�[�C�G���X�^�[�[1 �ُ̈헦��20�`50��2�j�i���x��Ⅳb�j�ł���C�X���ɂ���X�Nj���ɔ����X�����N���邽�߂ƍl�����Ă���B�X�������f�f�ɂ������X�y�f�̗L�p���Ɋւ��ẮC��ᇌa3.5cm �ȉ����X���ł�6 ��S��ŃG���X�^�[�[1 ���l�C��ᇌa4cm �ȏ���X���ł�5/14���G���X�^�[�[1���l�ł����� 13�j�i���x��Ⅳa�j�Ƃ�����C�G���X�^�[�[1 ���l���X���ł�10/17 �Ⴊ�؏��\�ł������̂ɑ��āC�G���X�^�[�[1 ����l���X��5 ��͐؏��s�\�ł����� 14�j�i���x��Ⅳa�j�Ƃ���������B����C�X���o�^�ɂ��C2cm �ȉ����X���ł��X�y�f���l�̕p�x��CA19-9 ���l�̕p�x�����Ⴉ���� 6�j�i���x��Ⅳb�j�B
- ��ᇃ}�[�J�[
�e��ᇃ}�[�J�[���X�����o���x�́CCA19-9 ��70�`80 ���CSpan-1 ��70�`80 ���CDupan-2 ��50�`60���CCEA ��30�`60���CCA50 ��60���ƕ� 2, 15, 16�j�i���x��Ⅳb�j����Ă��邪�C�i�s���������Ɨz�����͒Ⴍ�C2cm �ȉ����X���ł�CA19-9 �̗z������52���ł��� 6�j�i���x��Ⅳb�j�C�X���̑������o�ɂ͗L�p�ł͂Ȃ��BCA19-9 ���Y�����ꂸ�U�A��������Lewis ���t�^�A����ł�Dupan-2 ���L�p�ł��� 6�j�i���x��Ⅳb�j�B
Tumor M2 pyruvate kinase�iTu-M2-PK�j* ���X�����o���x��55���CCA19-9 �ł�86���C���ٓx��Tu-M2-PK ��52���CCA19-9 ��73���ł���CTu-M2-PK ��CA19-9 �����X���̃}�[�J�[�Ƃ��ė���Ă������C�_�`������Lewis ���t�^�̉e�����Ȃ����Ƃ��D��Ă��� 17�j�i���x��Ⅳb�j�B�܂��C�ʂ̕ɂ��CTu-M2-PK �͖����X�����Stage Ⅲ�`Ⅳ�X����ԂɗL�Ӎ������������C�����X�����Stage Ⅰ�`Ⅱ�X����Ԃɂ͗L�Ӎ��͂Ȃ��C�����X���Ɩ����X���Ƃ̊ӕʂɂ͗L�p�łȂ����� 18�j�i���x��Ⅳb�j�B
���A�a�����X���ł�CEA ��5ng/ml �ȏ�CCA19-9 ��500U/ml �ȏ�̗Ⴊ���A�a���X����ɔ�חL�ӂɑ��������BCA19-9 and/or CEA ���l���V���ɔ��ǂ������A�a���҂��X���̃X�N���[�j���O�̑ΏۂƂ��ׂ��ł��� 19�j�i���x��Ⅳb�j�B
����matrix metalloproteinase-9�iMMP-9�j* ���X���̗\��\���ɗL�p�ŁC����tissue inhibitor of metalloproteinase-1�iTIMP-1�j* �͖����X���ł̗z������56���C����҂�13���ł���C���ِ��ɖ�肪����ƕ���Ă��� 20�j�i���x��Ⅳb�j�B
�v���e�I�[����͂ɂ�蔭�����ꂽ�V�K��ᇃ}�[�J�[*�Ffibrinogen fragment ��DR-70 ���X�����Ҍ����ŗL�ӂɏ㏸���Ă������CCA19-9 �P�Ƃ̐��т𗽉킵�Ȃ����� 21�j�i���x��Ⅳb�j�BProlyl-hydroxylated ��-fibrinogen �����o���ꂽ���C�����X���ł͏㏸���Ă��Ȃ����� 22�j�i���x��Ⅳb�j�B
�X�����҂��X�t����MMP-9�Concogene DJ1�iDJ-1�j�Calpha-1B-glycoprotein precursor�iA1BG�j�����o����C�㏸���Ă��邱�Ƃ�western blot �Ŋm�F���ꂽ�BA1BG ���X���̃o�C�I�}�[�J�[�Ƃ��ď��߂Č��o����C����MMP-9 ���X���ɂ����āC�����X���⌒��l�ɔ䂵�L�ӂɏ㏸���Ă��� 23�j�i���x��Ⅳb�j�B
�Ɖu�n�̃}�[�J�[*�FG-CSF�CM-CSF�Cmacrophage inhibitory cytokine 1�iMIC-1�j�Ȃǂ̃T�C�g�J�C�����X���f�f�ł̗L�p�������ꂽ 24, 25�j�i���x��Ⅳb�j�B
- ���������g�����iultrasonography�GUS�j
�ȕւŐN�P�̂Ȃ����S�Ȍ����Ƃ��āC�O���f�Â⌟�f�ɂ����ėL�p�ł��邪�C�����ǃK�X��얞�ɂ�钴���g�̌����ɂ���X���`�o����ȏꍇ������B�����X�������X�b���͌��o����Ȃ��Ƃ������B�E�ꌟ�f�ł�US �ɂ���X�̗L�������͖�1���ŁC�X����������0.01���ȉ��ƒႢ 26-28�j�i���x��Ⅳb�j�B
�X�NJg�����X嚢�E��1,000 ��ȏ�̌o�ߊώ@�ɂ�蓯�Q�����X�������p�x�Ɍ��o���� 29, 30�j�i���x��Ⅳa�j�CIPMN 80 ����܂��X嚢�E��197 ��̌����ł��X�������p�x�Ɍ��o���ꂽ 31�j�i���x��Ⅳa�j�B���������āC���̂悤�ȏ������݂�ꂽ�ꍇ�͐����ɐi�ނׂ��ł���iCQ1-3�CCQ1-4�Q�Ɓj�B���̎��_���X���Ɛf�f����Ȃ��ꍇ���C����I�ȉ摜�������X���̑������o�ɗL�p�ł��� 32�j�i���x��Ⅳb�j�B����C3mm �����̎��X�NJg��114 ���5.8 �N�o�ߊώ@�������C1 ����X���͔��ǂ��Ȃ������Ƃ̕����� 33�j�i���x��Ⅳb�j�B
- ������`�q�ُ�*
�X���g�D�ł͍��p�x��K-ras ��p53 �̈�`�q�ُ킪�m�F����Ă���B�X�����҂Ō���K-ras �̈�`�q�ُ��p53 �`���E�Rp53 �R�̂̏㏸���F�߂���Ƃ̕� 34-36�j�i���x��Ⅳb�j�����邪�C�܂��]���͒�܂��Ă��Ȃ��BMicroarray analysis �ɂ��C���A�a�����X�����҂ɓ��ٓI�Ȉ�`�q�̂���Vanin-1 ��MMP-9 �̑g�ݍ��킹�ŁC�X���ɔ������A�a��2 �^���A�a���ł��悭�ӕʂł����i���x95.8���C���ٓx76���j�Ƃ̕����� 37�j�i���x��Ⅳb�j�B
* �ی������ڂ̌����E����
�� �����ւ̒�
�X���͓��ٓI�ȏǏ�ɖR�����B�G�r�f���X�̑啔���͐i�s�X���ɂ����镪�͂Ɋ�Â������̂ňꕔ�ɂ͖��Ǐ�̏Ǘ������B���������āC�Տ��Ǐ���X�����������̎w�W�ɂ͂Ȃ�Ȃ����C���ɂȂǂ̕����Ǐ��F�߂�ꍇ��C���A�a���ǂ��݂�ꂽ�ꍇ�ɂ́C�X���̉\�����l�����Č������s�����Ƃ��]�܂����B���̍ہC��ᇃ}�[�J�[���������X���łُ͈�l�������Ȃ����Ƃ��������Ƃɗ��ӂ��K�v�ł���BUS ���X�NJg����嚢�E��F�߂���⌌���X�y�f���l��ɑ��Ă�MRCP ��EUS ���s���C�X�Nj����F�߂��ꍇ�́C�X��ᎂ��Ȃ��Ƃ�ERCP ���s�����Ƃ��]�܂����B�댯���q���L���鑽�댯�Q�ɑ��āC���t������US���������I�ɍs�����Ƃɂ��C�X���̑��������������シ��B1cm �ȉ��̎�ᎂ����o�����ꍇ�C���eCT �Ŏ�ᎂ����o�ł��Ȃ��Ƃ��X����ے肵�Ă͂����Ȃ����Ƃɂ����ӂ��ׂ��ł���B
�� ���p����
1�j Pâlsson B, Masson P, Andre�Ln-Sandberg A. Tumour marker CA 50 levels compared to signs and symptoms in the diagnosis of pancreatic cancer. Eur J Surg Oncol 1977�G23�F151-156.
2�j ���{�X���w���X���o�^�ψ���D�X���o�^��2007�D�X��2007�G22�Fe1-e94.
3�j �]��V��C���c�a���C���R�����C���D�X���o�^����݂��X���̃��X�N�t�@�N�^�[�D�́E�_�E�X2004�G48�F547-554.
4�j Bakkevold KE, Arnesjø�GB, Kambestad B. Carcinoma of the pancreas and papilla of Vater�Fpresenting symptoms, signs, and diagnosis related to stage and tumour site. A prospective multicentre trial in 472 patients. Norwegian Pancreatic Cancer Trial. Scand J Gastroenterol 1992�G27�F317-325.
5�j Gullo L, Tomassetti P, Migliori M, et al. Do early symptoms of pancreatic cancer exist that can allow an earlier diagnosis�H Pancreas 2001�G22�F210-213.
6�j �]��V��C���c�a���C�ԓc���T�C���D���X���̑S���W�v�̉�́D�X�� 2004�G19�F558-566.
7�j Iodice S, Gandini S, Löhr M, et al. Venous thromboembolic events and organ-specific occult cancers�Fa review and meta-analysis. J Thromb Haemost 2008�G6�F781-788.
8�j DiMagno EP, Reber HA, Tempero MA. AGA technical review on the epidemiology, diagnosis, and treatment of pancreatic ductal adenocarcinoma. American Gastroenterological Association. Gastroenterology 1999�G117�F1464-1484.
9�j �R�쐳�K�C���c��v�C�R����j�C���D�X���Ǘ�ɂ������X���댯���q�̌����D�X�� 2003�G18�F479-488.
10�j Chari ST, Leibson CL, Rabe KG, et al. Probability of pancreatic cancer following diabetes�Fa population-based study.Gastroenterology 2005�G129�F504-511.
11�j Ogawa Y, Tanaka M, Inoue K, et al. A prospective pancreatographic study of the prevalence of pancreatic carcinoma in patients with diabetes mellitus. Cancer 2002�G94�F2344-2349.
12�j Pelaez-Luna M, Takahashi N, Fletcher JG, et al. Resectability of presymptomatic pancreatic cancer and its relationship to onset of diabetes�Fa retrospective review of CT scans and fasting glucose values prior to diagnosis. Am J Gastroenterol 2007�G102�F2157-2163.
13�j Nakaizumi A, Tatsuta M, Uehara H, et al. A prospective trial of early detection of pancreatic cancer by ultrasonographic examination combined with measurement of serum elastase 1. Cancer 1992�G69�F936-940.
14�j Hayakawa T, Kondo T, Shibata T, et al. Prospective trial for early detection of pancreatic cancer by elevated serum immunoreactive elastase. Gastroenterol Jpn 1990�G25�F727-731.
15�j Satake K, Chung YS, Yokomatsu H, et al. A clinical evaluation of various tumor markers for the diagnosis of pancreatic cancer. Int J Pancreatol 1990�G7�F25-36.
16�j Nazli O, Bozdag AD, Tansug T, et al. The diagnostic importance of CEA and CA19-9 for the early diagnosis of pancreatic carcinoma. Hepatogastroenterology 2000�G47�F1750-1752.
17�j Joergensen MT, Heegaard NH, Schaffalitzky de Muckadell OB. Comparison of plasma Tu-m2-PK and CA19-9 in pancreatic cancer. Pancreas 2010�G39�F243-247.
18�j Novotný�GI, Dítê�GP, Dastych M, et al. Tumor marker m2-pyruvate-kinase in differential diagnosis of chronic pancreatitis and pancreatic cancer. Hepatogastroenterology 2008�G55�F1475-1477.
19�j Guo Q, Kang M, Zhang B,et al. Elevated levels of CA 19-9 and CEA in pancreatic cancer-associated diabetes. J Cancer Res Clin Oncol 2010�G136�F1627-1631.
20�j Mroczko B, Lukaszewicz-Zajac M, Wereszczynska-Siemiatkowska U, et al. Clinical significance of the measurements of serum matrix metalloproteinase-9 and its inhibitor�itissue inhibitor of metalloproteinase-1�jin patients with pancreatic cancer�Fmetalloproteinase-9 as an independent prognostic factor. Pancreas 2009�G38�F613-618.
21�j Ward DG, Wei W, Buckels J, et al. Detection of pancreatic adenocarcinoma using circulating fragments of fibrinogen. Eur J Gastroenterol Hepatol 2010�G22�F1358-1363.
22�j Ono M, Matsubara J, Honda K, et al. Prolyl 4-hydroxylation of alpha-fibrinogen�Fa novel protein modification revealed by plasma proteomics. J Biol Chem 2009�G284�F29041-29049.
23�j Tian M, Cui YZ, Song GH, et al. Proteomic analysis identifies MMP-9, DJ-1 and A1BG as overexpressed proteins in pancreatic juice from pancreatic ductal adenocarcinoma patients. BMC Cancer 2008�G8�F241.
24�j Groblewska M, Mroczko B, Wereszczyńska-Siemiatkowska U, et al. Serum levels of granulocyte colony-stimulating factor�iG-CSF�jand macrophage colony-stimulating factor�iM-CSF�jin pancreatic cancer patients. Clin Chem Lab Med 2007�G45�F30-34.
25�j Koopmann J, Rosenzweig CN, Zhang Z, et al. Serum markers in patients with resectable pancreatic adenocarcinoma�Fmacrophage inhibitory cytokine 1 versus CA19-9. Clin Cancer Res 2006�G12�F442-446.
26�j ����M�i�C�����@�B�C���X�؍G�q�C���D�����g���f�ɂ����鐸�x����̐헪�D�����W���� 2001�G39�F231-236.
27�j �O���C��C�g�����q�C�ʓc�^�R���C���D�W�c���f�ɂ�����_嚢���f�f�̌����D�_���X 2005�G26�F801-804.
28�j ���{�����킪�f�w��S���W�v�ψ���D����22�N�x�����킪�f�S���W�v2012�D
http://jsgcs.or.jp/files/uploads/iinkai_h22.pdf
29�j Tanaka S, Nakao M, Ioka T, et al. Slight dilatation of the main pancreatic duct and presence of pancreatic cysts as predictive signs of pancreatic cancer�Fa prospective study. Radiology 2010�G254�F965-972.
30�j ���F�C�c���K�q�D�X���f�̗L�p���ƌ��E�D�X�� 2009�G24�F594-602.
31�j Tada M, Kawabe T, Arizumi M, et al. Pancreatic cancer in patients with pancreatic cystic lesions�Fa prospective study in 197 patients. Clin Gastroenterol Hepatol 2006�G4�F1265-1270.
32�j Tanaka S, Nakaizumi A, Ioka T, et al. Periodic ultrasonography checkup for the early detection of pancreatic cancer�Fpreliminary report. Pancreas 2004�G28�F268-272.
33�j ���䏺�`�C���쎛���`�C��藲�Y�C���D���������g���f�ɂ����錟�f��̔�����Ɋւ��钲���F�_�����X���̏����ɂ��āD���{�����킪�f�w��G�� 2009�G47�F552-558.
34�j Dianxu F, Shengdao Z, Tianquan H, et al. A prospective study of detection of pancreatic carcinoma by combined plasma K-ras mutations and serum CA19-9 analysis. Pancreas 2002�G25�F336-341.
35�j Uemura T, Hibi K, Kaneko T, et al. Detection of K-ras mutations in the plasma DNA of pancreatic cancer patients. J Gastroenterol 2004�G39�F56-60.
36�j Ohshio G, Suwa H, Imamura M. Clinical implication of anti-p53 antibodies and p53-protein in pancreatic disease. Int J Gastrointest Cancer 2002�G31�F129-135.
37�j Huang H, Dong X, Kang MX, et al. Novel blood biomarkers of pancreatic cancer-associated diabetes mellitus identified by peripheral blood-based gene expression profiles. Am J Gastroenterol 2010�G105�F1661-1669.
CQ 1-3�@�X�����^�����ꍇ�C�܂��s���ׂ������͉����H
| ����
|
|
|---|
�� �G�r�f���X
- CT�icomputed tomography�C���e���܂ށj
CT �͕a�ς̑傫���C�ʒu��L���肪�����������łȂ��C���e�܂̑��e���ʂ��a�ς̌������Ԃ��c���ł��邱�Ƃ���C���I�f�f�ɂ����Č������Ƃ̂ł��Ȃ������ł���B�������C���e�܂��g�p���Ȃ��P��CT �̒P�Ǝg�p���X���̐f�f�ɂ͓K���Ȃ��BUS �͒�N�P�ł���CT ��蕪��\���������ƁC������x�̎��I�f�f���\�ł��邱�Ƃ���ŏ��ɍs���錟���ł���B
US��CT�Ƃقړ����̐��� 1�j�i���x��Ⅴ�j 2�j�i���x��Ⅳb�j 3�j�i���x��Ⅰ�j�ƍl�����邪�C�����g���e�܂̎g�p�⏬�a�ς̕`�o�ɂ͗L���ł���B���eUS* �̕a�ό��o�\��87���CCT ��79���ł������ƕ� 4�j�i���x��Ⅳb�j����Ă���B�܂��C2cm �ȉ��̕a�ς́C���e�܂�p���Ȃ�US ��CT �̔�r�ɂ����āCUS �̊��x��57���CCT �̊��x��50���ł���5�j�i���x��Ⅳb�j�C���eUS*�ł͊��x��95����CT �̊��x68���ɔ䂵�L�ӂɍ��� 6�j�i���x��Ⅴ�j�B����CCT�͐f�f���u�̔��B�ɂ��C�������X���C�X����dynamic CT �̎B�����\�ƂȂ�C���e�܂�p���Ȃ�US��荂���f�f�\��L����Ƃ̕� 1�j�i���x��Ⅴ�j 2�j�i���x��Ⅳb�j 3�j�i���x��Ⅰ�j������B���̂悤��US ��CT �͒�N�P�ō����a�ό��o�\��L���邱�Ƃ���C�X���̎��I�f�f�̍ŏ��ɍs���ׂ������ƍl������B
���emultidetector row CT �͂��ڍׂȐf�f���\�ƂȂ��Ă���C�X���̑��ݐf�f�݂̂Ȃ炸���ǐZ���Ȃǂ̐i�W�x�f�f�Ɋւ��Ă����x85�`100���C���ٓx82�`92��7�j�i���x��Ⅰ�j 8, 9�j�i���x��Ⅳb�j�ƕ���Ă���B
- MRI�imagnetic resonance imaging�j�CMRCP�imagnetic resonance cholangiopancreatography�j
�ȑO�͋�ԕ���\��CT �̂��������邽�߁C��ʓI�ɂ��X���f�f�Ƃ��Ă�CT ������������Ă��Ȃ������B�������C�ߔN3 �e�X����MRI �ɂ��`�o�\�����サ�C���̗L�p��������Ă��� 10�j�i���x��Ⅲ�j�BMRI �̗D�ꂽ�Ƃ����CT �ƈقȂ�C�Z���Ԃł̌J��Ԃ��̌����ł�X ���픘���Ȃ����Ƃł���C�n�C���X�N�Q�ɑ��Ē���I��MRI �����ɂ���X�����f�f�\�ł������Ƃ�����Ȃ���Ă��� 10�j�i���x��Ⅲ�j 11�j�i���x��Ⅳb�j�B
���̂悤�ɍŋ߂̍�����\��dynamic MRI �ɂ���X���f�f�\�͑��eCT �Ƃقړ����̊��x�C���ٓx�ł���ƕ���Ă���CMRI ��CT �͂قړ����̈ʒu�Â��Ƃ��Đ����̂��߂̌����ƍl������ 12, 13�j�i���x��Ⅳb�j 14�j�i���x��Ⅳa�j�B�܂��ʏ��dynamic MRI �ł͂Ȃ��C�g�U�������idiffusion-weighted MRI�j��MDCT�Ɠ����i84��vs 86���j���X�����f���ł������ƕ���Ă��� 15�j�i���x��Ⅳb�j�B
������X�Ǒ���悷���X����3�������ł���ƕ� 16�j�i���x��Ⅴ�j����Ă���CMRCP ��CT�EUS �Ȃǂ̂ق��̌����ɂ����Đf�f�ł��Ȃ��ꍇ�Ɏ{�s�����ׂ������ł���B����C�X���ɂ����Ă��X�Ǒ��ɕω����݂��邱�Ƃ���CERCP �ɂ����銴�x��70�`86���C���ٓx��67�`94���ƕ� 17�j�i���x��Ⅲ�j 18�j�i���x��Ⅳb�j����Ă���BMRCP ��ERCP �Ƃ̔�r�����ɂ����Ċ��x����ѓ��ٓx�ɗL�Ӎ����F�߂��Ȃ����C��N�P�ł��邱�Ƃ𗝗R��MRCP �𐄏������ 17�j�i���x��Ⅲ�j���Ȃ���Ă���B�܂��CMRCP �P�Ƃ̌����ł��邪���x��95���C���ٓx��82���Ƃ̕� 19�j�i���x��Ⅳb�j�����邱�Ƃ���CMRCP �̐f�f�\��ERCP �Ƃقړ����ƍl������B
- ����ȕ��������g�����iUS�j
�̊OUS �͊ȕւŔ�N�P�Ȍ����Ƃ��āC�O���f�Â⌟�f�ɂ����ėL�p�ł���B�ߔN�C��q�����ꐢ�㒴���g���e��*��p����US 4�j�i���x��Ⅳb�j 6�j�i���x��Ⅴ�j�C��㒴���g���e��*��p����US 20�j�i���x��Ⅳb�j��g�D�̍d�x��\���ł���elastography* 21�j�i���x��Ⅳa�j�Ȃǂ��C�ʏ�̃t�@���_�����^���C���[�W�ɕt�����邱�Ƃ��X���̐f�f�\�����コ���邱�Ƃ�����Ă���B�܂��C���w�Ö@�̌��ʂɂ��đ��e�܂�p����US �ŗ\�����鎎�݂��s���Ă��� 22�j�i���x��Ⅳb�j�B���eUS* ���X���ɑ��Ă͕ی����ڂ���Ă��Ȃ������ł��邪�CCT ��MRI �ɂ����đ��e�܃A�����M�[�Ȃǂő��e�܂��g�p�ł��Ȃ��ꍇ�ɂ͓��ɗL�p�ł���B
�� �����ւ̒�
���eCT�CMRI�i���ɑ��e�j���X���̑��ݐf�f�ɗL�p�ł���C�����X�y�f�C��ᇃ}�[�J�[�CUS ���X�����^����Ύ��ɍs���ׂ������ł���B�������C�������X���ł͎�ᎂ̕`�o������Ȃ��Ƃ�����CEUS ��EUS-FNA�C�����X�Ǐ������ɑ��Ă�ERCP �ƂƂ��ɁC�זE�f��g�D�f�ɂ��m��f�f����{�݂ɂ����čs�����Ƃ��]�܂����B
�� ���p����
1�j Bakkevold KE, Arnesjø�GB, Kambestad B. Carcinoma of the pancreas and papilla of Vater�Fpresenting symptoms, signs, and diagnosis related to stage and tumour site. A prospective multicentre trial in 472 patients. Norwegian Pancreatic Cancer Trial. Scand J Gastroenterol 1992�G27�F317-325.
2�j DelMaschio A, Vanzulli A, Sironi S, et al. Pancreatic cancer versus chronic pancreatitis�Fdiagnosis with CA 19-9 assessment, US, CT, and CT-guided fine-needle biopsy. Radiology 1991�G178�F95-99.
3�j Bipat S, Phoa SS, van Delden OM, et al. Ultrasonography, computed tomography and magnetic resonance imaging for diagnosis and determining resectability of pancreatic adenocarcinoma�Fa meta-analysis. J Comput Assist Tomogr 2005�G29�F438-445.
4�j Sofuni A, Iijima H, Moriyasu F, et al. Differential diagnosis of pancreatic tumors using ultrasound contrast imaging. J Gastroenterol 2005�G40�F518-525.
5�j ��◘�j�C����L���C�����M�V�C��. EUS�ɂ��TS1�X���̐f�f. �_���X 2005�G26�F539-543.
6�j Kitano M, Kudo M, Maekawa K, et al. Dynamic imaging of pancreatic diseases by contrast enhanced coded phase inversion harmonic ultrasonography. Gut 2004�G53�F854-859.
7�j Zhao WY, Luo M, Sun YW, et al. Computed tomography in diagnosing vascular invasion in pancreatic and periampullary cancers�Fa systematic review and meta-analysis. Hepatobiliary Pancreat Dis Int 2009�G8�F457-464.
8�j Furukawa H, Uesaka K, Boku N. Treatment decision making in pancreatic adenocarcinoma�Fmultidisciplinary team discussion with multidetector-row computed tomography. Arch Surg 2008�G143�F275-280.
9�j Zamboni GA, Kruskal JB, Vollmer CM, et al. Pancreatic adenocarcinoma�Fvalue of multidetector CT angiography in preoperative evaluation. Radiology 2007�G245�F770-778.
10�j Shin SS, Armao DM, Burke LM, et al. Comparison of the incidence of pancreatic abnormalities between high risk and control patients�Fprospective pilot study with 3 Tesla MR imaging. J Magn Reson Imaging. 2011�G33�F1080-1085.
11�j Vasen HF, Wasser M, van Mil A, et al. Magnetic resonance imaging surveillance detects early-stage pancreatic cancer in carriers of a p16-Leiden mutation. Gastroenterology 2011�G140�F850-856.
12�j Rao SX, Zeng MS, Cheng WZ, et al. Small solid tumors�i�� or �� 2cm�jof the pancreas�Frelative accuracy and differentiation of CT and MR imaging. Hepatogastroenterology. 2011�G58�F996-1001.
13�j ���c���j�C���Z�~�C��������. �_���E�X�������������Ƃ��Ă�3T 3D Dynamic MRI �̗L�p��. J Gastroenterol Cancer Screen 2009�G47�F357-366.
14�j Koelblinger C, Ba-Ssalamah A, Goetzinger P, et al. Gadobenate dimeglumine-enhanced 3. 0-T MR imaging versus multiphasic 64-detector row CT�Fprospective evaluation in patients suspected of having pancreatic cancer. Radiology 2011�G259�F757-766.
15�j Takakura K, Sumiyama K, Munakata K, et al. Clinical usefulness of diffusion-weighted MR imaging for detection of pancreatic cancer�Fcomparison with enhanced multidetector-row CT. Abdom Imaging. 2011�G36�F457-462.
16�j Freeny PC. Radiologic diagnosis and staging of pancreatic ductal adenocarcinoma. Radiol Clin North Am 1989�G27�F121-128.
17�j Adamek HE, Albert J, Breer H, et al. Pancreatic cancer detection with magnetic resonance cholangiopancreatography and endoscopic retrograde cholangiopancreatography�Fa prospective controlled study. Lancet 2000�G356�F190-193.
18�j Furukawa T, Tsukamoto Y, Naitoh Y, et al. Differential diagnosis between benign and malignant localized stenosis of the main pancreatic duct by intraductal ultrasound of the pancreas. Am J Gastroenterol 1994�G89�F2038- 2041.
19�j Lopez Hänninen E, Amthauer H, Hosten N, et al. Prospective evaluation of pancreatic tumors�Faccuracy of MR imaging with MR cholangiopancreatography and MR angiography. Radiology 2002�G224�F34-41.
20�j Kersting S, Konopke R, Kersting F, et al. Quantitative perfusion analysis of transabdominal contrast-enhanced ultrasonography of pancreatic masses and carcinomas. Gastroenterology 2009�G137�F1903-1911.
21�j Uchida H, Hirooka Y, Itoh A, et al. Feasibility of tissue elastography using transcutaneous ultrasonography for the diagnosis of pancreatic diseases. Pancreas 2009�G38�F17-22.
22�j Sofuni A, Itoi T, Itokawa F, et al. Usefulness of contrast-enhanced ultrasonography in determining treatment efficacy and outcome after pancreatic cancer chemotherapy. World J Gastroenterol 2008�G14�F7183-7191.
CQ 1-4�@�X���̐f�f���m�肷�邽�߂̎��̃X�e�b�v�͂ǂ����邩�H
| ����
|
|
|---|
�� �G�r�f���X
- EUS�iendoscopic ultrasonography�j
�����g�������͏����ǂ̃K�X�̉e�����邱�Ƃ��قƂ�ǂȂ����Ƃ�����C���x86�`100���C���ٓx58.3�`97���C���f��93���Ɣ�r�I�ǍD�Ȑ��� 1-3�j�i���x��Ⅳb�j 4�j�i���x��Ⅴ�j������Ă���B�h�v���[�ɂ�錌���̕]����t������EUS ��CT �Ƃ̔�r�������s������dynamic CT ��EUS �Ƃ̔�r�ł����҂ɍ��͔F�߂Ă��Ȃ��B��㒴���g���e��* 5�j�i���x��Ⅴ�j��elastography* 6�j�i���x��Ⅳb�j�̕��p�ɂ���Ď��I�f�f�\�̌���ɗL�p�ł���Ƃ̕�����B
- ERCP�iendoscopic retrograde cholangiopancreatography�j
- PET
PET�͑����X��ᇂ̗Lj����̊ӕʂɗp�����Ă���C���x��82�`92���ƕ� 9�j�i���x��Ⅴ�j 10�j�i���x��Ⅳb�j����Ă���BCT ���邢��MRI �Ɣ�r���ėǍD�Ȏ��I�f�f�\���� 11�j�i���x��Ⅳa�j����Ă��邪�C2cm �ȉ��̏��X���ɑ���f�f�\�͏\���Ȍ������Ȃ���Ă��炸�]���͒�܂��Ă��Ȃ��BPET ��CT ��g�ݍ��킹��PET/CT ��PET �P�Ƃɔ�אf�f�\���D���Ƃ����� 12�j�i���x��Ⅳb�j������B
- �זE�f�E�g�D�f
- 1�j�����g�����������h�z���זE�f�iendoscopic ultrasonography-fine needle aspiration�GEUS-FNA�j
�V�X�e�}�e�B�b�N�E���r���[���ЂƂ���CEUS-FNA ���X��᎐��a�ςɑ����X���f�f�̊��x��54�`95���C���ٓx��72�`100���ł��� 13�j�i���x��Ⅰ�j�B�����ǂ�1.2�`6.3���ɔ������Ă���C�}���X���C�뚋���x���C���ɁC�����Ǐo���Ȃǂ�F�߂����C�d�Ăȍ����ǂ͔F�߂Ă��Ȃ� 14-18�j�i���x��Ⅴ�j�B
- 2�j�����g�K�C�h�����h�z���זE�f�iUS-FNA�j�ECT �K�C�h�����h�z���זE�f�iCT-FNA�j
�V�X�e�}�e�B�b�N�E���r���[���ЂƂ���CUS�CCT �̋�ʂȂ���������Ă���_��������C�̊O���iUS ���邢��CT�jFNA ���X��᎐��a�ςɑ����X���f�f�̊��x��45�`100���C���ٓx��91�`100���ł��� 13�j�i���x��Ⅰ�j�B�����ǂ�1.6�`4.9���ɔ������Ă���C���̂قƂ�ǂ��{�s�����u�ɂł���C���̑��ɋ}���X���C�����_�o���ˁC嚢�E�o���C���nj���Ȃǂ����� 19-21�j�i���x��Ⅴ�j�B
US-FNA �����CT-FNA �̓K���͉摜�f�f���X�����^�����X��᎐��a�ςł���C�Lj����̊ӕʂ�ړI�Ɏ{�s�����B���᎕a�ςɑ��銴�x��17��22�j�i���x��Ⅴ�j�ƒቺ���C�L�p�Ƃ͂����Ȃ��B
- 3�jEUS-FNA �Ƒ̊O��FNA �̔�r
EUS-FNA ��̊O��FNA �ƒ��ڔ�r���������ł́CEUS-FNA �Ƒ̊O��FNA �Ƃ̊ԂŐf�f�\�ɍ��͂Ȃ������ƕ���Ă��� 23�j�i���x��Ⅱ�j���CEUS-FNA �͑̊O��FNA �ɔ䂵�����d��̕p�x���Ⴍ 24�j�i���x��Ⅳb�j�C���h�j�̉��ǂɂ����h���e�ՂɂȂ��� 25�j�i���x��Ⅱ�j�B����ɕی����ڂ��ꂽ���Ƃ��l�������EUS-FNA ����I���ƍl���Ă��悢�B
- 4�j���̑�
�p��FNA 26�j�i���x��Ⅴ�j�CERCP ���זE�f 27�j�i���x��Ⅴ�j�C�X�ǃu���b�V���O�זE�f 28�j�i���x��Ⅴ�j�C�o���X�Ǔ������זE�f 29�j�i���x��Ⅴ�j�CPTBD ���_�`�זE�f 30�j�i���x��Ⅴ�j�Ȃǂ��܂��܂ȃA�v���[�`�ɂ��זE�f���s���Ă���C���x��53�`93���ł��邪�C�]���͂܂��m�肵�Ă��Ȃ��B
- 1�j�����g�����������h�z���זE�f�iendoscopic ultrasonography-fine needle aspiration�GEUS-FNA�j
- ��`�q����
�X���̐f�f�ɂ����āC�̎悳�ꂽ���̂ɑ�K-ras��`�q�ψ� 31�j�i���x��Ⅴ�j�̌����������邱�ƂŊ��x���㏸���C�f�f�\�̌���Ɋ�^����ƍl������B���̑��CMUC* 32�j�i���x��Ⅴ�j�Cp53* 33�j�i���x��Ⅴ�j�C�X�t�e�������[�[����* 34�j�i���x��Ⅴ�j�C�X�t��DNA �̃��`����* 35�j�i���x��Ⅴ�j�Ȃǂ��f�f�ɗL�p�ł���Ƃ̕����邪�C�]���͂܂��m�肵�Ă��Ȃ��B
��`�q�f�f�̓K���͌��̗ʂ����Ȃ��ꍇ��זE�f�A����ɂ����ĕ⏕�f�f�Ƃ��ėL�p�ł��� 31�j�i���x��Ⅴ�j�B�������C�ǐ������ɂ����Ă��z�����������Ƃ����邽�߁C���̈����ɒ��ӂ��K�v�ł��� 22, 36�j�i���x��Ⅴ�j�B
- �ŏI�a���f�f
�� �����ւ̒�
US�CCT �ȂǂŎ��I�f�f�Ɏ���Ȃ��ꍇ�ɂ́CEUS�CERCP�CPET �Ȃǂ̌�����K�v�ɉ����đg�ݍ��킹�����I�ɐf�f���Ă����ׂ��ł���B�������X���ł́C�����̌�������g���Ă����݂̉摜��͔\�͂ł͎�ᎂ̕`�o������Ȃ��Ƃ������B�Ԑڏ������X���������^����ꍇ�ɂ́C�זE�f��g�D�f�ɂ��m��f�f����{�݂ɂ����čs�����Ƃ��]�܂����B
��X�̉摜�f�f�ɂ���X���Ɛf�f����؏����ꂽ�a�ςɂ����ėǐ������� 5�`10�����݂��邱�ƁC�X�����҂ɑ����p�N�P���傫�����Ƃ��l������ƁC���Ȃ��Ƃ��摜�f�f���X���̐f�f�ɓ�a����ꍇ�ɂ͕a���g�D�w�I�Ȋm��f�f�����݂邱�Ƃ��]�܂����B�g�D�̎�ɔ��������ǂ����݂��邪�C���̒��x��p�x�Ǝ�p�N�P�����Ă���Αg�D�̎悪���߂���B���ɉ��w�Ö@�i���w���ː��Ö@�j���s���ۂ́C�K�Ȗ�ܑI���̂��߂ɂ��a���f�f���s�����Ƃ��������߂���B�g�D�̎�̕��@�͂��������݂��邪�C���҂̕a�Ԃ��l�����čł����S�Ŋm���ȕ��@��I�����邱�Ƃ��d�v�ł���B�̎���@�̗D����������炩�ȃG�r�f���X�͂Ȃ����Ƃ��C�g�D�̎�̎�i�͊��҂���ю厡��ɂ���Č��肳���ׂ��ł���B��`�q�����ɂ��Ă͂��܂������i�K�ł��荡��̔��W�����҂����B
�� ���p����
1�j Furukawa T, Tsukamoto Y, Naitoh Y, et al. Differential diagnosis between benign and malignant localized stenosis of the main pancreatic duct by intraductal ultrasound of the pancreas. Am J Gastroenterol 1994�G89�F2038-2041.
2�j ���c�����C����T��C��������C���D�����g�����������̓_���]���ɂ���X������ю�ᎌ`�����X���̊ӕʐf�f�D�X�� 1996�G11�F430-434.
3�j Legmann P, Vignaux O, Dousset B, et al. Pancreatic tumors�Fcomparison of dual-phase helical CT and endoscopic sonography. AJR Am J Roentgenol. 1998�G170�F1315-1322.
4�j Akahoshi K, Chijiiwa Y, Nakano I, et al. Diagnosis and staging of pancreatic cancer by endoscopic ultrasound. Br J Radiol. 1998�G71�F492-496.
5�j Napoleon B, Alvarez-Sanchez MV, Gincoul R, et al. Contrast-enhanced harmonic endoscopic ultrasound in solid lesions of the pancreas�Fresults of a pilot study. Endoscopy 2010�G42�F564-570.
6�j Giovannini M, Thomas B, Erwan B, et al. Endoscopic ultrasound elastography for evaluation of lymph nodes and pancreatic masses�Fa multicenter study. World J Gastroenterol 2009�G15�F1587-1593.
7�j Freeny PC. Radiologic diagnosis and staging of pancreatic ductal adenocarcinoma. Radiol Clin North Am 1989�G27�F121-128.
8�j Adamek HE, Albert J, Breer H, et al. Pancreatic cancer detection with magnetic resonance cholangiopancreatography and endoscopic retrograde cholangiopancreatography�Fa prospective controlled study. Lancet 2000�G356�F190-193.
9�j Koyama K, Okamura T, Kawabe J, et al. Diagnostic usefulness of FDG PET for pancreatic mass lesions. Ann Nucl Med 2001�G15�F217-224.
10�j Rose DM, Delbeke D, Beauchamp RD, et al. 18 Fluorodeoxyglucose-positron emission tomography in the management of patients with suspected pancreatic cancer. Ann Surg. 1999�G229�F729-737�Gdiscussion 737-738.
11�j Kauhanen SP, Komar G, Seppänen MP, et al. A prospective diagnostic accuracy study of 18F-fluorodeoxyglucose positron emission tomography/computed tomography, multidetector rowcomputed tomography, and magnetic resonance imaging in primary diagnosis and staging of pancreatic cancer. Ann Surg 2009�G250�F957-963.
12�j Strobel K, Heinrich S, Bhure U, et al. Contrast-enhanced 18F-FDG PET/CT�F1-stop-shop imaging for assessing the resectability of pancreatic cancer. J Nucl Med 2008�G49�F1408-1413.
13�j Hartwig W, Schneider L, Diener MK, et al. Preoperative tissue diagnosis for tumours of the pancreas. Br J Surg 2009�G96�F5-20.
14�j Eloubeidi MA, Chen VK, Eltoum IA, et al. Endoscopic ultrasound-guided fine needle aspiration biopsy of patients with suspected pancreatic cancer�Fdiagnostic accuracy and acute and 30-day complications. Am J Gastroenterol 2003�G98�F2663-2668.
15�j Eloubeidi MA, Jhala D, Chhieng DC, et al. Yield of endoscopic ultrasound-guided fine-needle aspiration biopsy in patients with suspected pancreatic carcinoma. Cancer 2003�G99�F285-292.
16�j ���{�w��C�R�Y�����C�勴�v�F�C���D�X�����ɑ��钴���g�����������h�z���@�̗L�p���̌���. �X�� 2002�G17�F485-491.
17�j O�fToole D, Palazzo L, Arotcarena R, et al. Assessment of complications of EUS-guided fine-needle aspiration. Gastrointest Endosc. 2001�G53�F470-474.
18�j Eloubeidi MA, Gress FG, Savides TJ, et al. Acute pancreatitis after EUS-guided FNA of solid pancreatic masses�Fa pooled analysis from EUS centers in the United States. Gastrointest Endosc 2004�G60�F385-389.
19�j Di Stasi M, Lencioni R, Solmi L, et al. Ultrasound-guided fine needle biopsy of pancreatic masses�Fresults of a multicenter study. Am J Gastroenterol 1998�G93�F1329-1333.
20�j Sperti C, Pasquali C, Di Prima F, et al. Percutaneous CT-guided fine needle aspiration cytology in the differential diagnosis of pancreatic lesions. Ital J Gastroenterol 1994�G26�F126-131.
21�j Zech CJ, Helmberger T, Wichmann MW, et al. Large core biopsy of the pancreas under CT fluoroscopy control�Fresults and complications. J Comput Assist Tomogr 2002�G26�F743-749.
22�j Urgell E, Puig P, Boadas J, et al. Prospective evaluation of the contribution of K-ras mutational analysis and CA 19.9 measurement to cytological diagnosis in patients with clinical suspicion of pancreatic cancer. Eur J Cancer 2000�G36�F2069-2075.
23�j Horwhat JD, Paulson EK, McGrath K, et al. A randomized comparison of EUS-guided FNA versus CT or US-guided FNA for the evaluation of pancreatic mass lesions. Gastrointest Endosc 2006�G63�F966-975.
24�j Micames C, Jowell PS, White R, et al. Lower frequency of peritoneal carcinomatosis in patients with pancreatic cancer diagnosed by EUS-guided FNA vs. percutaneous FNA. Gastrointest Endosc 2003�G58�F690-695.
25�j Siddiqui UD, Rossi F, Rosenthal LS, et al. EUS-guided FNA of solid pancreatic masses�Fa prospective, randomized trial comparing 22-gauge and 25-gauge needles. Gastrointest Endosc 2009�G70�F1093-1097.
26�j Schramm H, Urban H, Arnold F, et al. Intrasurgical pancreas cytology. Pancreas 2002�G24�F210-214.
27�j ���F�D�X�_�njn��ᇂ̑����f�f�ɍזE�f�͕s���ł���D���{�Տ��זE�w���B�A����G�� 2005�G36�F1-4.
28�j �ɓ������C�Ίې����C���䐟�C���D�X�ǃu���b�V���O�זE�f�����p53 ���F���X���f�f�ɂ�����L�p���̌����D�L����w 1995�G47�F1250-1251.
29�j �㌴�G�V�C���F�C���c�����C���D�o���X�Ǔ��������X�Ǔ��������זE�f�ɂ���X�������̐f�f�D���l�a 1998�G38�F37-40.
30�j ���r�Y�C�����m�C�N��M�i�D���D�X���ɑ���PTCD �_�`�זE�f�̗z�����Ɋ֗^������q�ɂ��āD���{�Տ��זE�w��G�� 1998�G37�F455-459.
31�j Ogura T, Yamao K, Sawaki A, et al. Clinical impact of K-ras mutation analysis in EUS-guided FNA specimens from pancreatic masses. Gastrointest Endosc 2012�G75�F769-774.
32�j Chhieng DC, Benson E, Eltoum I, et al. MUC1 and MUC2 expression in pancreatic ductal carcinoma obtained by fine-needle aspiration. Cancer 2003�G99�F365-371.
33�j �R���u�D�X�t��p53 ���}����`�q�ψق̌��o�Ƃ����X���f�f�ւ̉��p�Ɋւ��錤���D�����w�\�S��w��G�� 1997�G106�F533-544.
34�j �㌴�G�V�C���F�C����C�C���D�X�t�e�������[�[�������o�ɂ���X���̐f�f�iK-ras �ψقƂ̔�r�j�D���l�a 2000�G40�F33-34.
35�j Matsubayashi H, Canto M, Sato N, et al. DNA methylation alterations in the pancreatic juice of patients with suspected pancreatic disease. Cancer Res 2006�G66�F1208-1217.
36�j �|�������C�㌴�G�V�C���F�C���D�y�זE�f�ւ̃t�B�[�h�o�b�N��ڂ����V������@�z�X���̐f�f�ɂ������X�tK-ras �_�ˑR�ψق̈Ӌ`�F�X�t�זE�f�����Ƃ̑Δ䂩��D���{�Տ��זE�w��G��1997�G36�F92-97.
37�j Abraham SC, Wilentz RE, Yeo CJ, et al. Pancreaticoduodenectomy�iWhipple resections�jin patients without malignancy�Fare they all �echronic pancreatitis�f�H Am J Surg Pathol 2003�G27�F110-120.
38�j Smith CD, Behrns KE, van Heerden JA, e al. Radical pancreatoduodenectomy for misdiagnosed pancreatic mass. Br J Surg 1994�G81�F585-589.
39�j DeWitt J, Jowell P, Leblanc J, et al. EUS-guided FNA of pancreatic metastases�Fa multicenter experience. Gastrointest Endosc 2005�G61�F689-696.
40�j Hosoda W, Takagi T, Mizuno N, et al. Diagnostic approach to pancreatic tumors with the specimens of endoscopic ultrasound-guided fine needle aspiration. Pathol Int 2010�G60�F358-364.
CQ 1-5�@�X���̕a���͂ǂ̂悤�Ɍ��肷�邩�H
| ����
|
�X���̕a���f�f�iTNM ���q�j�ɂ�MDCT ��EUS �����߂���i�O���[�hB�j�B |
|---|
�� �G�r�f���X
�X����TNM �f�f�Ɋւ���O�����̕�4 �҂ɉ߂����i�\1�j�C�V�X�e�}�e�B�b�N�E���r���[��1 �҂ł���B
EUS ����̂Ƃ����X����TNM �f�f�Ɋւ��������������C���̂Ȃ��őO�����̕�3 �҂������B2 �҂�EUS ��CT �̔�r 1, 2�j�i���x��Ⅲ�j�C����1 �҂�EUS�C�w���J��CT�CMRI�C���Ǒ��e�̔�r 3�j�i���x��Ⅱ�j�̕ł���B151 ��̘A�������Ǘ�̂���81 ��̎�p���ΏۂƂ��āCTN ���q�C���ǐZ���C�؏��\�\���̐��f�����r�����Ƃ���C���ׂ�EUS ��CT ���������Ƃ̕����� 1�j�i���x��Ⅲ�j�B����C80 ����X�����܂�120 ����X���^���Ō��������ł́C��ᇌ��o���ᇂ�staging �ɂ�MDCT�imulti-detector-row CT�j���EUS �̂ق����D��Ă��邪�C�����p�ߓ]�ڂ�؏��\�̐f�f�ɂ��Ă͓����ł���Ƃ��Ă��� 2�j�i���x��Ⅲ�j�B3 �Җڂ�62 ��̊J�����ΏۂƂ��Č������C�Ǐ��i�W�C���ǐZ���C���u�]�ځCTNM �X�e�[�W�C�؏��\�\���̐��f�����r�����Ƃ���C�������C�Ǐ��i�W�C���ǐZ���C���u�]�ځCTNM �X�e�[�W�C�؏��\�\���Ńw���J��CT ���ł��������f���C��ᇌa�C�����p�ߓ]�ڂ̕]����EUS ���ł��������f���ł���C�����͂ɂ����āC���̗��҂��ł��M���ł��C�R�X�g�̂�����Ȃ��f�f�@�ƕ��Ă��� 3�j�i���x��Ⅱ�j�B������EUS �Ɋւ��Ă͌������̌�������89 ���ΏۂƂ��āCTN ���q�̐��f�������ꂼ��69���C34���ł��������C��ɉߐf�f�̂��ߐ؏��\�\������46���ɉ߂����C���m�ł͂Ȃ��Ƃ̕������� 4�j�i���x��Ⅳb�j�B
���̌����@�ł́C���o���{�������o����US ������p�����X����TNM �f�f�Ɋւ��������������������̂Ȃ���1 �҂͑̊O��US�C���o��US�CCT �̑O�����Ȕ�r 5�j�i���x��Ⅲ�j�i�\1�j�C����1 �҂͒P�ƌ��� 6�j�i���x��Ⅲ�j�̕ł���B�O�҂�50 ����X�����܂��X�����̈����ΏۂƂ��āCT ���q�̓��ٓx�͂��ꂼ��64���C100���C47���CM ���q�̓��ٓx�͂��ꂼ��29���C94���C33���ŁC�����I�Ȑ؏��\�\���̐��f����CT ��79���ɑ��ĕ��o��US ��97���ƍł��M���ł��錟���ƕ��Ă��� 5�j�i���x��Ⅲ�j���҂�CT ���ʼn��u�]�ڂ������X��35 ���ΏۂƂ��āCTNM �e���q�����TNM �X�e�[�W�̓��ٓx�����ꂼ��80���C76���C68���C68���ƕ��Ă��� 6�j�i���x��Ⅲ�j�B���������o����US �͌����_�ł͍L���s���Ă��Ȃ��B�ŋ߁C���u�]�ڂł���̓]�ڂɑ��đ��e�����g����*�ł̌������i�߂��Ă���B
�܂��C�V�X�e�}�e�B�b�N�E���r���[��1 �҂�CT �ɂ�錌�ǐZ���̕]���C���m�ȕ��ː��w�I�f�f����ю�p�܂��͕a���ɂ��m��f�f�C�z���C�U�z���C�A���C�U�A�����\�ɂȂ��Ă����X������ѓ������̈���Ɋւ���18 �̕�1,231 ���ΏۂɃ��^�A�i���V�X�����ŁC�S�̂�CT �ɂ�錌�ǐZ���̊��x��77���C���ٓx��81���ł��������CCT ���\�����P���ꂽ2004�`2008 �N�̕ł͂��ꂼ��85���C82���Ɍ��サ�Ă����B����ɁC���Ǎ\�z�����ꍇ�͂��Ȃ��ꍇ���ǍD�Ŋ��x84���C���ٓx85���ł������ƕ���Ă��� 7�j�i���x��Ⅰ�j�B
CQ2-1�ɂ���悤�ɁC�O�ȓI��p�K���̋��E�ƂȂ�Stage Ⅳa �ł̊O�Ȑ؏���p�Ɖ��w���ː��Ö@��RCT �ɂ�錟���ŁC�p�O�摜�f�f��Stage Ⅳa �Ƃ��ꂽ81 �ᒆ39 ��i49.4���j���J�������ʼnߏ�������͉ߏ��f�f�������X���ɂ���C�p�O�摜�ł̐i�s�x�f�f������ł��邱�Ƃ������Ă���B
�X���̕a���f�f�Ƃ��Ċ��҂����V���������@�Ƃ��ẮCCT ��PET ��Z������PET-CT �X�L���������邪 8�j�i���x��Ⅳb�j�C���f���̓_�ł܂��L�����p������Ă��Ȃ��B�܂��C�R�����o���ʼn��u�]�ڂ��m�F����؏�������ł����ǗႪ27.6������CCT �ƐR�����o����K�Ɏ{�s���邱�Ƃ��X���̐؏��\���̕]���ɗL���ł���Ƃ̕��������� 9�j�i���x��Ⅳa�j�C�W�����͂���Ă��Ȃ��B���ǁC�X����TNM �f�f�Ɋւ���O�����ȕ͏�L��4 �҂����Ȃ��C�����_���X���̕a���f�f�iTNM ���q�j�ɂ́CMDCT�CEUS �����߂���ƍl������
| �� | �����@ | ���x | ���ٓx | ���f�x |
|---|---|---|---|---|
Gress F.G. et al.1�j |
EUS |
95�� | 92�� | 93�� |
CT |
97�� | 19�� | 60�� | |
DeWitt J, et al2�j |
EUS |
98�� | 90�� | 97�� |
MDCT |
86�� | 90�� | 87�� | |
Sorinano A. et al.3�j |
EUS |
23�� | 100�� | 67�� |
CT |
67�� | 97�� | 83�� | |
MRI |
57�� | 90�� | 75�� | |
Angio |
37�� | 100�� | 71�� | |
John T.G. et al.5�j |
US |
23�� | 56�� | 80�� |
CT |
66�� | 54�� | 79�� | |
Lap US |
83�� | 93�� | 97�� | |
Angio |
62�� | 64�� | 82�� |
�� �����ւ̒�
���m�ȕa���f�f�͂��܂��ɍ���ł��邪�CMDCT�CEUS �𒆐S��US�CMRI �Ȃǂ������̉摜�f�f��g�ݍ��킹�đ����I�ɔ��f����̂������I�ł���B�܂��C�G�r�f���X�͂Ȃ����̂́C���u�]�ڐf�f�ł�FDG-PET/CT ��R�����o�����L�p�ł��邱�Ƃ�����C�Ǘ��K�ɑI������Εa���f�f�̌���̈ꏕ�ɂȂ邩������Ȃ��B
�� ���p����
1�j Gress FG, Hawes RH, Savides TJ, et al. Role of EUS in the preoperative staging of pancreatic cancer�Fa large single-center experience. Gastrointest Endosc 1999�G50�F786-791.
2�j DeWitt J, Devereaux B, Chriswell M, e al. Comparison of endoscopic ultrasonography and multidetector computed tomography for detecting and staging pancreatic cancer. Ann Intern Med 2004�G16�F753-763,
3�j Soriano A, Castells A, Ayuso C, et al. Preoperative staging and tumor resectability assessment of pancreatic cancer�Fprospective study comparing endoscopic ultrasonography, helical computed tomography, magnetic resonance imaging, and angiography. Am J Gastroenterol 2004�G99�F492-501.
4�j Ahmad NA, Lewis JD, Ginsberg GG, et al. EUS in preoperative staging of pancreatic cancer. Gastrointest Endosc 2000�G52�F463-468.
5�j John TG, Wright A, Allan PL, et al. Laparoscopy with laparoscopic ultrasonography in the TNM staging of pancreatic carcinoma. World J Surg 1999�G23�F870-881.
6�j Durup Scheel-Hincke J, Mortensen MB, Qvist N, et al. TNM staging and assessment of resectability of pancreatic cancer by laparoscopic ultrasonography. Surg Endosc 1999�G13�F967-971.
7�j Zhao WY, Luo M, Sun YW, et al. Computed tomography in diagnosing vascular invasion in pancreatic and periampullary cancers�Fa systematic review and meta-analysis. Hepatobiliary Pancreat Dis Int 2009�G8�F457-464.
8�j Beyer T, Townsend DW, Brun T, et al. A combined PET/CT scanner for clinical oncology. J Nucl Med 2000�G41�F1369-1379.
9�j Morak MJ, Hermans JJ, Smeenk HG, et al. Staging for locally advanced pancreatic cancer. Eur J Surg Oncol 2009�G35�F963-968.
CQ 1-6�@Borderline resectable�X���̐f�f�F�킪���ɂ�����borderline resectable�Ƃ́H
| ����
|
|
|---|
�wNCCN �K�C�h���C���x�i2012 �N�Łj�ɂ�����Tumors considered borderline resectable �̒�`
|
�� �G�r�f���X
�X���͏Ǐ�ɖR�����C�f�f���ɂ��łɐ؏��s�\�ȏǗႪ�����̂������Ƃ�����B�f�f���ɉ��u�]�ڂ�L���邽�ߐ؏��s�\�ƂȂ邾���łȂ��C���o������㒰�Ԗ������Ȃǂւ̋Ǐ��i�s�̂��ߐ؏����s���̂��C�؏��s�\�Ƃ��ĉ��w���ː��Ö@�≻�w�Ö@���s���̂����Õ��j�̌���ɓ�a����Ǘ���o�����邱�Ƃ�����B���̂悤�ȏǗႪborderline resectable �Ǘ�ƂȂ邪�C������X���̋Ǐ��Z���ɂ��O�ȓI�؏����{�s���Ă������Ɋ�����c���i�g�D�w�I����c�FR1�C����I����c�FR2�j�C�؏��ɂ�鐶�����ԉ������ʂ邱�Ƃ��ł��Ȃ��\����������̂ƒ�`����� 1�j�i���x��Ⅵ�j�B
�wNCCN�K�C�h���C���x�i2012�N�Łj�ł�tumors considered borderline resectable �Ƃ��āC��L�̂悤�ɒ�`���Ă���B����͓��{�́w�X���戵���K��x�i��6 �Łj�ł����Ƃ���̐_�o�p�Z�������x�ł��邪�����Z���̂Ȃ��Ǘ���Ӗ����Ă�����̂ƍl���邱�Ƃ��ł���B
Borderline resectable �Ǘ�̐f�f�ɂ�����CT ���S�g�������܂ߗL�p�ł��邪 2-4�j�i���x��Ⅵ�j�C�B�e���̑��e�܂̎�����X���C�X���Ȃǂ̎B�e�����ɒ��ӂ��K�v������Cborderline resectable �X���̐f�f�́CMD-CT �ŒP�������łȂ��C�������E�X�������E�喬����3 ���ł���3mm ��thin slice �ł̎B�e���s�����Ƃ��]�܂����B�܂��Cborderline resectable �Ǘ�͔����̓]�ڂ╠���d��ɂ��؏��s�\�ƂȂ�\��������C�s�K�v�ȊJ���p������邽�߂ɐR�����o���͗L�p�ł��� 5�j�i���x��Ⅱ�j 2, 3, 6�j�i���x��Ⅵ�j���C�؏��s�\���q��L�����X���Ǘ�̍��댯�Q��I�ʂ�����@���l���Ȃ���Ȃ�Ȃ��B
�p�O�摜�Ŗ喬�܂��͏㒰�Ԗ��Ö��Z����F�߂��X������109 ��ɂ����āC�p�O���w���ː��Ö@����Q��R0 ����59���ł���C�Ȃ��Q��R0 ��11���Ɣ�r���ėL�ӂ�R0 ���������ł������ip��0.0001�j 7�j�i���x��Ⅳb�j�B�wNCCN�K�C�h���C���x�i2012 �N�Łj�ɂ�����borderline resectable �Ǘ�͎�p��s�ł͊��̈�c�iR1�CR2�j�������ɔF�߂��邱�Ƃ���C�č��ł́wNCCN �K�C�h���C���x�i2012 �N�Łj�ɂ�����borderline resectable �̒�`�͗L�p�ł���B
�� �����ւ̒�
�X���͐����X���̂��ߓ������͂̎��b�g�D�Z�x�̏㏸���ꍇ������C�摜�ł͐��������X���ɂ�鉊�ǐ��ω��Ȃ̂��X���ɂ��_�o�p�Z���Ȃ̂��ӕʐf�f�ɋꗶ����ꍇ������BBorderline resectable �f�f���@�̂���Ȃ���P���X���Ǘ�̎��Õ��j����ɕK�v�ł���B����ɁC����Տ��̏p�O�f�f�ɂ����āC�����㒰�Ԗ������ɖ��ɐڂ��Ă��Ă�encasement ���Ȃ��ꍇ�́C�킪���́w�X���戵���K��x�i��6 �Łj��Asm�|, PL�{�ɂ����邪�C�p�O�摜�f�f�̏㒰�Ԗ������Z���̗L���Ɋւ��鐸�x�ɂ��܂���肪����C�p�O�f�f���@�̂���Ȃ���P���K�v�ł���B
�� ���p����
1�j Adams RB, Allen PJ. Surgical treatment of resectable and borderline resectable pancreatic cancer�Fexpert consensus statement by Evans et al. Ann Surg Oncol 2009�G16�F1745-1750.
2�j Callery MP, Chang KJ, Fishman EK, et al. Pretreatment assessment of resectable and borderline resectable pancreatic cancer�Fexpert consensus statement. Ann Surg Oncol 2009�G16�F1727-1733.
3�j Choti MA, Dixon E, Tyler D. Pretreatment assessment of resectable and borderline resectable pancreas cancer�Fexpert consensus statement by Callery et al. Ann Surg Oncol 2009�G16�F1734-1735.
4�j Crane CH, Varadhachary G, Settle SH, et al. The integration of chemoradiation in the care of patient with localized pancreatic cancer. Cancer Radiother 2009�G13�F123-143.
5�j Satoi S, Yanagimoto H, Toyokawa H, et al. Selective use of staging laparoscopy based on carbohydrate antigen 19-9 level and tumor size in patients with radiographically defined potentially or borderline resectable pancreatic cancer. Pancreas 2011�G40�F426-432.
6�j Vauthey JN, Dixon E. AHPBA/SSO/SSAT Consensus Conference on Resectable and Borderline Resectable Pancreatic Cancer�Frationale and overview of the conference. Ann Surg Oncol 2009�G16�F1725-1726.
7�j Chun YS, Milestone BN, Watson JC, et al. Defining venous involvement in borderline resectable pancreatic cancer. Ann Surg Oncol 2010�G17�F2832-2838.
CQ 1-7�@�����\�オ���҂ł��鑁�����X����f�f����ɂ͂ǂ����邩�H
| ����
|
|
|---|
�� �G�r�f���X
�X���ɂ͑����X���̊T�O�����݂��Ȃ��B�]���C�X�����������̎�ᇌa��2cm �ȉ��iTS1�j���ЂƂ̖ڈ��Ƃ���Ă����B����C���{�X���w�2007 �N�ɏW�v�����X���o�^�ł́C��ᇌa2cm �ȉ��iTS1�j�Ǘ�̂����CStage Ⅰ�k�w�X���戵���K��x�i��6 �Łj�l 1�j��5 �N��������54.6���ł��������CTS1 �ǗႪStage Ⅰ�ɑ������銄���́C�X�������ł킸��15.3���C�X�̔�������33.3���ƒᗦ�ł����� 2�j�i���x��Ⅴ�j�B�܂��؏��\��ɂ������ᇌa2cm �ȓ��̂��̂�2cm ������̂Ƃ̔�r�����ł́C��ᇌa�ł͂Ȃ���ᇕ����x���Ɨ������\����q�Ƃ��Ĉʒu�Â�����Ƃ̕��݂�� 3�j�i���x��Ⅳb�j�C�����f�f�̖ڕW�Ƃ��Ď�ᇌa2cm �͏\���ł͂Ȃ��\������������Ă���B���݂܂ł�TS1�X���Ɋւ���ł́C�����Ǐ�Ƃ���20�`38���ɕ��ɁC���t 4, 5�j�i���x��Ⅳb�j�C7���ɓ��A�a�̈��� 4�j�i���x��Ⅳb�j���݂��C17�`50�������Ǐ� 4, 5�j�i���x��Ⅳb�j�ł������B�摜�f�f�Ɋւ��ẮC���������g�̎�ᇕ`�o����52�`63���ƒᗦ�ł��� 6, 7�j�i���x��Ⅳb�j�BMDCT �ł̑��ݐf�f����88�`100���ŁC�X�NJg�����̊Ԑڏ����̕`�o����86�`88���ł��邪 8, 9�j�i���x��Ⅳb�j�C��ᇕ`�o����43�`65���Ƃ��ᗦ�ł��� 6-11�j�i���x��Ⅳb�j�C�Ԑڏ�����L���Ȃ��Ǘ�ł͎��I�Ȑf�f������ȏꍇ������B�����g�������iEUS�j�͍�������\��L���邽�߁C�댯���q��L����Ǘ�ɂ������X���̏E���グ�Ɋ��҂���Ă��� 12�j�i���x��Ⅳb�j�BEUS �̎�ᇕ`�o����92�`97���ƍ����ł��� 6, 7, 10, 11�j�i���x��Ⅳb�j�C���eEUS �p���邱�ƂŐf�f�������シ��\��������Ă��� 11�j�i���x��Ⅳb�j�BERCP �Ɋւ��Ă̓o���[��ERP �̗L�p��������Ă���C91�����X�ǂُ̈폊�����F�߂��邪 13�j�i���x��Ⅳb�j�C�X�ǐ����C�X�t�זE�f�̐f�f���͂��ꂼ��50�`75���C44�`70���ƕ���Ă��� 7, 14�j�i���x��Ⅳb�j�C�����g�����������h�z���זE�f�iEUS-FNA�j�̕��p�ɂ��f�f�������シ��\�������� 7�j�i���x��Ⅳb�j�B
��ᇌa1cm �ȉ��̏Ǘ�́C62�`75����Stage Ⅰ�ɊY������ƕ���Ă��� 15, 16�j�i���x��Ⅳb�j�B���{�X���w����X���o�^�ɂ�����13 ��̉�͂ł́C39���͖��Ǐ�ł���CCEA�CCA19-9 �̏㏸��15���C39���ƒᗦ�ł������B��ᇌa11�`20mm �̏Ǘ�Ƃ̔�r�ł́C�i�s�x���L�ӂɑ����ŁC�����p�ǐZ���C�Ö��Z���C�_�o���͐Z�������Ȃ��X���ł���C�p�㐶�����������X���ɂ����� 16�j�i���x��Ⅳb�j�B�摜�f�f�̓����́C�قڑS��Ԑڏ����ł�����X�NJg����US �ŕߑ�����C��ᇕ`�o����US ��17�`70���CMDCT ��33�`75���ƕɂ�荷���݂��邪�CEUS ��86�`100���ƗǍD�Ȑ��т�����Ă��� 17, 18�j�i���x��Ⅳb�j�B����CT �ŏ��^�X��ᇂ��w�E������EUS ���{�s����132 ��̌����ŁC3 ���1cm �ȉ����X����f�f�����Ƃ̕��݂��� 19�j�i���x��Ⅳb�j�BEUS-FNA �͐��f��92�`96���C���x75�`95���C���ٓx98�`100���ƗǍD�Ȑ��т�����Ă��� 20, 21�j�i���x��Ⅳb�j�B�X�������f�f�ɂ�����EUS�͔��ɗL�͂Ȑf�f�@�Ɉʒu�Â�����B
�X�������iStage 0�j�Ɋւ���ڍׂȕ͏��Ȃ��B�摜�̓����Ƃ��ĕ��80�`83���Ŏ��X�ǂ܂��͕��}�X�ǂɌ��ǓI����E�g�����݂���B�唼�̏ǗႪ�����Ǐ�ɖR�������̂́C�}���X������s����ꍇ������B�f�f�̌_�@�ƂȂ����摜�����́CUS�CCT �ɂ��y�����X�NJg�����邢�͊g���X�nja��嚢�E�a�̕ω����唼�ł���BMRCP�CERCP �ňُ폊�����m�F�̌�C�ǎ����X�Ǒ��e�C����ѓ������I�o�@�X�ǃh���i�[�W�iENPD�j�𗯒u������������X�t�זE�f���{�s���邱�Ƃ��f�f�ɗL�p�ł���Ƃ̕��݂��� 22, 23�j�i���x��Ⅳb�j�B
����US ���X�nja2.5mm �ȏ�܂���5 mm �ȏ��嚢�E��L����1,058 ��̑O�����o�ߊώ@�̌����ł́C����75.5 �J���̊ώ@���ԂŁC12 ����X�����������C42����Stage Ⅰ�܂łŐf�f����Ă��� 24�j�i���x��Ⅳa�j�C�y�����X�NJg���C嚢�E��L����Ǘ�̌o�ߊώ@�������f�f�̎肪����ƂȂ�\�������� 25�j�i���x��Ⅳa�j�B�X�Ǔ������S�t����ᇁiIPMN�j���X���̊댯���q�Ɉʒu�Â����C���������X����2�`8���ƕ���Ă��� 26, 29�j�i���x��Ⅳb�j 27, 28�j�i���x��Ⅳa�j�CIPMN�����Ȃ��X���Ɣ�r���đ����ɐf�f�����\�� 30�j�i���x��Ⅳb�j�CIPMN �̌o�ߊώ@���ʏ�^�X���̑����f�f�ɂȂ���\��������Ă��� 27, 28�j�i���x��Ⅳa�j�B����C�ʏ�^�X���̔�����O���ɂ������XIPMN�̌o�ߊώ@�̑̐��\�z���K�v�ł��낤�B
�� �����ւ̒�
�댯���q��L����Ǘ�ɑ���X�N���[�j���O�����������ɂȂ��邩�̌����ł́C�Ƒ����X���C�Ƒ����ٌ^����������F��nj�Q�iFAMMM�j�C��`�������������nj�Q�iHBOC�j�CPeutz-Jeghers �nj�Q�Ȃǂ̊댯���q��L���閳�Ǐ��44 ��ɂ����鏉��EUS �̌����ɂ����āC3 ��i6.8���j���X�����F�߂��C1 ���Stage Ⅰ�ł����� 31�j�i���x��Ⅳa�j�B�܂�p-16Leiden �ψق�F�߂銳��79 ��ɂ�����1 �N���Ƃ�MRCP �{�s�̌����ł́C�ώ@���Ԓ����l4 �N��7 ��i9���j���X�����݂��C����4 �ႪTS1 �Ǘ�ł����� 32�j�i���x��Ⅳa�j�B����C�����ł���`���X���nj�Q�Ȃǂ̊댯���q��L����Ǘ�ɑ��ĉ摜�f�f���܂߂�����I�Ȍ����̌n�̍\�z���]�܂�邪�C�����̊Ԋu�C�ǂ̉摜�f�f�@��I�����ׂ����Ȃǂ͖������ł��荡��̌����ۑ�ł���B
���������Ɋւ���n��A�g�̏d�v���̕��U������Ă��� 33�j�i���x��Ⅳb�j�B�댯���q��L����Ǘ�ɑ���X�N���[�j���O�C�����C�o�ߊώ@�̑̐���a�f�ŘA�g���C�n��A�g�N���j�J���p�X����p���đS���̊e�n��ō\�z���Ă������Ƃ��]�܂��B����C���҂̌������S�C��p�Ό��ʁCX ���픚�̖����l�����������I�Ȑ헪�̊m����ڎw������K�͂ȑO�����������]�܂��B
 |
 |
 |
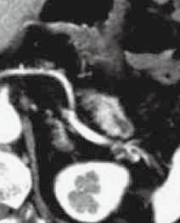
�` ����CT �ɂĔ����X�ǂ̌y���Ȋg����F�߂邪�C���炩�Ȏ�ᇐ��a�ς݂͂��Ȃ��B |
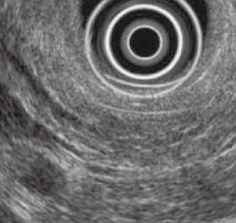
�a EUS �ł͑̕����X�ǂ̋��݂���B |
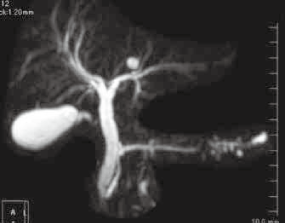
�b&emsp�GMRCP �ł͑̕����X�ǂ̕s���ȋ��݂��C����������̕��}�X�ǂ��g�����Ă���B |
 |
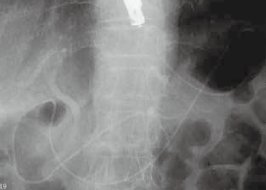 |
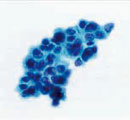 |
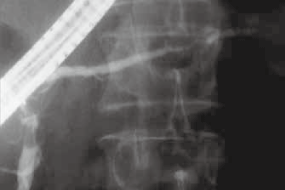
�c ERCP �ł͑̕����X�ǂ̕s���ȋ��݂��C�����̕��}�X�ǂ͕`�o���s�ǂł���B |
�d RCP �Ɉ��������������I�o�@�X�ǃh���i�[�W�iENPD�j���{�s���C��������X�t�זE�f���{�s�B |
�e �זE�f�͊��z���ł������B |
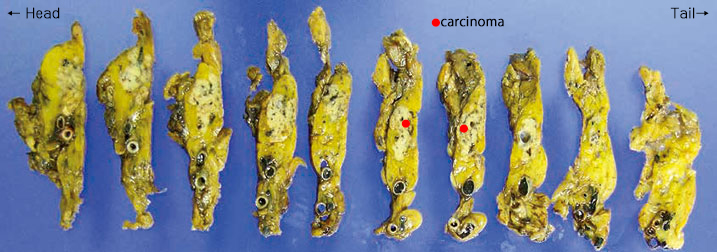 |
�f |
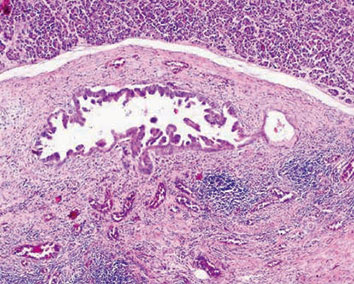 |
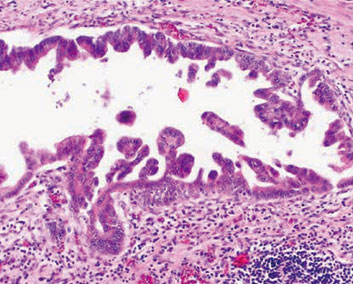 |
�g |
�h |
G�`I �̔����؏����{�s���ꂽ���ʁC�ԐF�̕��ʂ̎��X�ǂɌ��ǂ��ď�������F�߂��B
�� ���p����
1�j ���{�X���w��ҁD�X���戵���K��i��6�Łj�D�����o�ŁC2009.
2�j ���{�X���w��D�X���o�^�� 2007�D�X�� 2007�G22�Fe1-e427.
3�j Pongprasobchai S, Pannala R, Smyrk TC, et al. Long-term survival and prognostic indicators in small�i��or��2cm�jpancreatic cancer. Pancreatology 2008�G8�F587-592.
4�j Egawa S, Takeda K, Fukuyama S, et al. Clinicopathological aspects of small pancreatic cancer. Pancreas 2004�G28�F235-240.
5�j Shimizu Y, Yasui K, Matsueda K, et al. Small carcinoma of the pancreas is curable�Fnew computed tomography finding, pathological study and postoperative results from a single institute. J Gastroenterol Hepatol 2005�G20�F1591-1594.
6�j Maguchi H, Takahashi K, Osanai M, et al. Small pancreatic lesions�Fis there need for EUS-FNA preoperatively�H What to do with the incidental lesions�H Endoscopy 2006�G38�FS53-S56.
7�j ���ؒ��V�C���V�Ďu�C�V�ؖ��C���D�����X�������ւ̐V���ȃA�v���[�`-�g�D�f�f�FEUS-FNA. �̒_�X�摜 2008�G10�F569-576.
8�j Yoon SH, Lee JM, Cho JY, et al. Small�i�� 20mm�jpancreatic adenocarcinomas�Fanalysis of enhancement patterns and secondary signs with multiphasic multidetector CT. Radiology 2011�G259�F442-452.
9�j ����N�Y�C���ʖF���C�^���G��C���DMDCT���X�E�_�����̐f�f�ɂǂ��܂Ŕ���邩 MDCT�ŏ��X���̐f�f�͉\���D�̒_�X�摜 2008�G10�F133-138.
10�j Irisawa A, Sato A, Sato M, et al. Early diagnosis of small pancreatic cancer�Frole of endoscopic ultrasonography. Dig Endosc 2009�G21�FSuppl 1�FS92-S96.
11�j Sakamoto H, Kitano M, Suetomi Y, et al. Utility of contrast-enhanced endoscopic ultrasonography for diagnosis of small pancreatic carcinomas. Ultrasound Med Biol 2008�G34�F525-532.
12�j Bhutani MS, Verma D, Guha S, et al. Is endoscopic ultrasound �gsound�h for pancreatic cancer screening�H J Clin Gastroenterol 2009�G43�F797-802.
13�j Ikeda S, Maeshiro K, Ryu S, et al. Diagnosis of small pancreatic cancer by endoscopic balloon-catheter spot pancreatography�Fan analysis of 29 patients.Pancreas 2009�G38�Fe102-113.
14�j Takasawa O, Fujita N, Noda Y, et al. Clinicopathological study on the intraductal spread of small pancreatic cancer. J Gastroenterol 2007�G42�F957-961.
15�j �ԓc�h�m�C�ѐ��m���C���싐�ʁC���D1cm �ȉ��̏��X���ɂ�����EUS �̈ʒu�Â��D�_���X 2009�G30�F343-348.
16�j �]��V��D�X���o�^���ꂽ1cm�ȉ��̏��X���̉�́D�_���X 2009�F30�F311-316.
17�j ���q�@�O�C���쓿�V�C������O�D�p�O�f�f���ꂽStage Ⅰ�X���̏Ǘ�Ɖ��- Stage Ⅰ�X���̏E���グ�Ɖ摜�f�f�̌���-�e�{�݂̒Ǘ��ʂ��āD�̒_�X�摜 2008�G10�F545-550.
18�j ��{�m��C�k���V�C�|�R�X�T�C���D1cm �ȉ����X���̐f�f�̂��߂̃A�v���[�`�\�e�摜�f�f�̔�r-�D�_���X 2009�G30�F335-341.
19�j Yasuda I, Iwashita T, Doi S, et al. Role of EUS in the early detection of small pancreatic cancer. Dig Endosc 2011�G23 Suppl 1�F22-25.
20�j Uehara H, Ikezawa K, Kawada N, et al. Diagnostic accuracy of endoscopic ultrasound-guided fine needle aspiration for suspected pancreatic malignancy in relation to the size of lesions. J Gastroenterol Hepatol 2011�G26�F1256-1261.
21�j ���ؒ��V�C���V�Ďu�C�V�ؖ��C���D10mm�ȉ��̏��X���̐f�f�ɂ�����EUS-FNA�̗L�p���D�_���X 2009�G30�F361-367.
22�j �ԓc�h�m�C�ѐ��m���C���싐�ʁC��. �X�������f�f�̎肪����ƂȂ�a�Ԃ���ѐf�f�E�V���Ȓm��. �̒_�X 2011�G62�F567-573.
23�j �g�c�_�i�C������O�C����N�N�C���D�X�������̐f�f�͉\���D�_���X 2009�G30�F317-323.
24�j Tanaka S, Nakao M, Ioka T, et al. Slight dilatation of the main pancreatic duct and presence of pancreatic cysts as predictive signs of pancreatic cancer�Fa prospective study. Radiology 2010�G254�F965-972.
25�j Tada M, Kawabe T, Arizumi M, et al. Pancreatic cancer in patients with pancreatic cystic lesions�Fa prospective study in 197 patients.Clin Gastroenterol Hepatol 2006�G4�F1265-1270.
26�j Maguchi H, Tanno S, Mizuno N, et al. Natural history of branch duct intraductal papillary mucinous neoplasms of the pancreas�Fa multicenter study in Japan. Pancreas 2011�G40�F364-370.
27�j Uehara H, Nakaizumi A, Ishikawa O, et al. Development of ductal carcinoma of the pancreas during follow-up of branch duct intraductal papillary mucinous neoplasm of the pancreas. Gut 2008�G57�F1561-1565.
28�j Hanada K, Amano H, Hino F, et al. Management strategies for branch duct intraductal papillary-mucinous neoplasms. Dig Endosc 2006�G18�iSuppl 1�j�FS68-S72.
29�j Tanno S, Nakano Y, Sugiyama Y, et al. Incidence of synchronous and metachronous pancreatic carcinoma in 168 patients with branch duct intraductal papillary mucinous neoplasm. Pancreatology 2010�G10�F173-178.
30�j Yamaguchi K, Kanemitsu S, Hatori T, et al. Pancreatic ductal adenocarcinoma derived from IPMN and pancreatic ductal adenocarcinoma concomitant with IPMN. Pancreas 2011�G40�F571-580.
31�j Poley JW, Kluijt I, Gouma DJ, et al. The yield of first-time endoscopic ultrasonography in screening individuals at a high risk of developing pancreatic cancer. Am J Gastroenteol 2009�G104�F2175-2181.
32�j Vasen HF, Wasser M, van Mil A, et al. Magnetic resonance imaging surveillance detects early-stage pancreatic cancer in carriers of a p16-Leiden mutation. Gastroenterology 2011�G140�F850-856.
33�j �ԓc�h�m�C�ѐ��m���C���싐�ʁC���D�\����P��ڎw�������X���f�f�̍őO���`�댯���q�̗����ƒn��A�g�`�i�����s��t���X�������f�f�v���W�F�N�g�j�D�����A���������a�@��� 2010�G20�F21-26.
http://ja-onomichi-hospital.jp/archives/index.php?sel=3&kid=4
2 �O�ȓI���Ö@
CQ 2-1�@Stage Ⅳa �X���ɑ����p�I�؏��Ö@�̈Ӌ`�͂��邩�H
| ����
|
Stage Ⅳa �܂ł��X���i���j�ɂ͍�����ڎw������p�؏��Ö@���s�����Ƃ����������i�O���[�hB�j�B �i���j�w�X���戵���K��x�i��6 �Łj��Stage Ⅳa �ŏ㒰�Ԗ������iSMA�j�������͕��o�������iCA�j�ɐZ���̂Ȃ����̂��ΏہB |
|---|
�� �G�r�f���X
��p�K�����ق��̎��Õ��@�Ɣ�r�����Տ�������1 �҂̂ݑ��݂���B��p���̏��������ƂɊO�Ȑ؏���p�Ɖ��w���ː��Ö@�ɖ���ׂɊ���t���������ʁC�O�Ȑ؏��Q�����w���ː��Ö@�Q�ɔ�r����3 �N�������i20��vs 0���j�C���ϐ������ԁi22.6 �J�� vs 11.8 �J���j�Ƃ��Ƀn�U�[�h��0.46 �ŗL�ӂɗǍD�ł������B5 �N�������͊O�Ȑ؏��Q10���ɑ��ĉ��w���ː��Ö@�Q�ł�0���ł������B������@���̍݉@���ԂƃR�X�g�̖ʂł��O�Ȑ؏��Q������66 ���i���ρ�17,500�j�ɑ��C ���w���ː��Ö@�Q�ł͕���101 ���i���ρ�28,200�j�ƗL�ӂɑ��������BStage Ⅳa �̂Ȃ��ł�A�i�{�j��͑ΏۂƂ��Ă��Ȃ��B�㒰�Ԗ������iSMA�j�������͕��o�������iCA�j�ɐZ���̂Ȃ�Stage Ⅳa �X����ΏۂɊO�Ȑ؏����s�����Ƃ͊��҂̗��v�ɂȂ�B�܂��C�J����������݂��p�OCT �̐��f���͑O���Z���iS�j65���C����Z���iRP�j84���C�喬�Z���iPV�j86���ł���C���Ö@�̌���͊J���f�f����ɍs���ׂ��ł���Əq�ׂĂ��� 1�j�i���x��Ⅱ�j�B
���m�Ȑi�W�x�f�f�����Õ��j�̌���ɂ͏d�v�ł��邪�C�J���Ɋ�Â����i�W�x�f�f�̏d�v���͌����Ă��Ȃ��B�Ǐ��i�s�؏��s�\�X���̐f�f�ŏp�O���Â��s�����Q�ł́C���ǐZ�����ߏ�]������Đ؏��\�����Ⴍ���ς�����X���ɂ���C�摜�f�f�݂̂ŊO�Ȏ�p��ے肷�邱�Ƃ͍ŏ����ɂ��ׂ��ł���Ƃ��Ă��� 2�j�i���x��Ⅲ�j�B�p�O�̐؏��ېf�f�́CMDCT �Ŋ��x90�`100���C���ٓx65�`71��3-5, 8�j�i���x��Ⅴ�j 6, 7�j�i���x��Ⅳb�j�CMRI �Ŋ��x90�`100���C���ٓx41�`89�� 9�j�i���x��Ⅲ�j 10�j�i���x��Ⅴ�j�CEUS�Ŋ��x100���C���ٓx75��5, 11-13�j�i���x��Ⅴ�j�ł������BEUS ���X��ᇂ̐؏��̉ۂɂ��Ă̐f�f���؏��Ǘ�̊J���������Ӗ���CT �̐f�f�⏕�ɏd�v�ł���B�������C�����̕��@�Őf�f���Ă��p�O�ɂ͌��o�ł��Ȃ������d��E�̓]�ڂȂǂ̉��u�]�ڂ�؏��ł��Ȃ����ǐZ����20�`50���߂��Ǘ�ő��݂��� 3-5, 8, 10-14�j�i���x��Ⅴ�j�Ƃ�����_���܂��c�����Ă���C�f�f�I���o�� 15�j�i���x��Ⅳb�j�̏d�v�����������Ă���B
�� �����ւ̒�
�{CQ �ɑ��鐄���̃G�r�f���X�ƂȂ��Ă���Տ����� 1�j�i���x��Ⅱ�j�őΏۂƂȂ����a�����X���ł�R0 ��p���\�ł���C�ꕔ�̊��҂ł͎������܂ޒ���������������B���������āC�����̉\�������҂������Õ��j��I������ꍇ�ɂ́C�؏���p�����{���邱�Ƃ����ɂ��Ȃ��Ă���B����ɁC���@���ԁC��p�C�����������ɂ����Ă��O�Ȑ؏��Q�����w���ː��Ö@�Q�ɔ�r���ė��v������B����C���w�Ö@�̃G�r�f���X���ςݏd�˂��Ă���C�Q���V�^�r�����_���CS-1 ���邢�̓Q���V�^�r�����_���{S-1 �ɂ�鎡�ÂƊO�Ȑ؏��p��O�����ɔ�r���鎎�����s����K�v���o�Ă���B�����ɐڂ��Ă���悤�ȏꍇ�ɁCdown-staging ��ڎw�������Â��s���邱�Ƃ������Ȃ��Ă��Ă���BBorderline resectable �X�����܂ނ̂��킪���́w�X���戵���K��x�i��6 �Łj�ɂ�����Stage Ⅳa �ł��邱�Ƃ���C �p�O�̕a���f�f�̐��x��������ƂƂ��ɁCborderline resectable �X���ɑ��āC�p�O���Â̈Ӌ`���O�����Ɏ��������ׂ��ł���BStage Ⅳa �X���͏p�O�̉摜�f�f�Ő��m�ɔ��f�ł��Ȃ����Ƃ�����C�p�O���Â��Ȃ��ꂽ�ꍇ�ɂ́C�f�f�I���o�����邢�͊J����p���s���������ł̎��Õ��j���肪�d�v�Ȃ��Ƃ�F�����ׂ��ł���B
�� ���p����
1�j Doi R, Imamura M, Hosotani R, et al. Surgery versus radiochemotherapy for resectable locally invasive pancreatic cancer�Ffinal results of a randomized multi-institutional trial. Surg Today 2008�G38�F1021-1028.
2�j Morgan DE, Waggoner CN, Canon CL, et al. Resectability of pancreatic adenocarcinoma in patients with locally advanced disease downstaged by preoperative therapy�Fa challenge for MDCT. AJR Am J Roentgenol 2010�G194�F615-622.
3�j Kaneko OF, Lee DM, Wong J, et al. Performance of multidetector computed tomographic angiography in determining surgical resectability of pancreatic head adenocarcinoma. J Comput Assist Tomogr 2010�G34�F732-738.
4�j Lee JK, Kim AY, Kim PN, et al. Prediction of vascular involvement and resectability by multidetector-row CT versus MR imaging with MR angiography in patients who underwent surgery for resection of pancreatic ductal adenocarcinoma. Eur J Radiol 2010�G73�F310-316.
5�j Bao PQ, Johnson JC, Lindsey EH, et al. Endoscopic ultrasound and computed tomography predictors of pancreatic cancer resectability. J Gastrointest Surg 2008�G12�F10-16�Gdiscussion 16.
6�j Grieser C, Steffen IG, Grajewski L, et al. Preoperative multidetector row computed tomography for evaluation and assessment of resection criteria in patients with pancreatic masses. Acta Radiol 2010�G51�F1067-1077.
7�j Kent TS, Raptopoulos V, Callery MP, et al. Escalating computed tomography angiogram�iCTA�jgrade predicts unresectability and margin status for pancreaticobiliary neoplasms. HPB�iOxford�j2010�G12�F115-122.
8�j Klauss M, Mohr A, von Tengg-Kobligk H, et al. A new invasion score for determining the resectability of pancreatic carcinomas with contrast-enhanced multidetector computed tomography. Pancreatology 2008�G8�F204-210.
9�j Park HS, Lee JM, Choi HK, et al. Preoperative evaluation of pancreatic cancer�Fcomparison of gadolinium-enhanced dynamic MRI with MR cholangiopancreatography versus MDCT. J Magn Reson Imaging 2009�G30�F586-595.
10�j Tapper EB, Martin D, Adsay NV, et al. An MRI-driven practice�Fa new perspective on MRI for the evaluation of adenocarcinoma of the head of the pancreas. J Gastrointest Surg 2010�G14�F1292-1297.
11�j Seicean A, Badea R, Mocan T, et al. Radial endoscopic ultrasonography in the preoperative staging of pancreatic cancer. J Gastrointestin Liver Dis 2008�G17�F273-278.
12�j Virtue MA, Mallery S, Li R, et al. Clinical utility of endoscopic ultrasound in solid pancreatic mass lesions deemed resectable by computer tomography. JOP 2008�G9�F167-171.
13�j Kala Z, Válek V, Hlavsa J, et al. The role of CT and endoscopic ultrasound in pre��operative staging of pancreatic cancer. Eur J Radiol 2007�G62�F166��169.
14�j Croome KP, Jayaraman S, Schlachta CM. Preoperative staging of cancer of the pancreatic head�Fis there room for improvement �H Can J Surg 2010�G53�F171��174.
15�j Mayo SC, Austin DF, Sheppard BC, et al. Evolving preoperative evaluation of patients with pancreatic cancer�Fdoes laparoscopy have a role in the current era�H J Am Coll Surg 2009�G208�F87��95.
CQ 2-2�@���o���זE�f�z���Ǘ�̐؏��̈Ӌ`�͂��邩�H
| ����
|
���o���זE�f�z�����X���ɑ��Ă��X�؏����s���ׂ����ۂ��͖��炩�ł͂Ȃ��B����C�Տ������⌤���̒~�ςɂ���Ė��炩�ɂ����ׂ��ł���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�w�X���戵���K��x�i��6 �Łj�ɂ����āC�X����p�ɂ����镠�o�זE�f�̎��{���@�����߂Ē�`���ꂽ���C���̌��ʂ͐i�s�x���ނɂ͔��f����Ă��Ȃ��B
���o���זE�f�z�����\��̈����Ɋ֗^����Ƃ����Ƃ��āC�ȉ�5 �҂���������B1 �߂́C32 ��̕��o���זE�f�z����̂����C17 ��̓���I�����d��z����̐������Ԓ����l��8.6 �J���C15 ��̓���I�����d��A�����7.8 �J���ō���F�߂��C�ΏƌQ�Ƃ��Ă̕��o���זE�f�A�����13.5 �J���ƗL�ӂɉ��������Ƃ����ł��� 1�j�i���x��Ⅳb�j�B2 �߂́C50 �ᒆ13 ��i26���j�ŕ��o���זE�f�z���ŁC13 �ᒆ9 ��œ���I�����d��A���ł��������̂̍זE�f�A����̂ق����z������S�������Ԃ̉�����F�߂��Ƃ����ł��� 2�j�i���x��Ⅳb�j�B3 �߂́C40 ���ΏۂƂ��āC�זE�f�̌��ʂ͉��u�]�ڂƂ̑��ւ�F�߂Ȃ��������̂́C�זE�f�z����͉A������L�ӂɗ\��s�ǂł������Ƃ���ł��� 3�j�i���x��Ⅳb�j�B4 �߂́C202 ��̋Ǐ��i�s�؏��s�\�X����ΏۂƂ��āC�זE�f�z����̐������Ԓ����l��11 �J���ŁC�A�����15 �J�������L�ӂɕs�ǂł���C���ϗʉ�͂ł��L�ӂȗ\��s�Ǘ\�����q�ł������Ƃ����ł��� 4�j�i���x��Ⅳb�j�B�܂�5 �߂Ƃ��āC36 ��̂����זE�f�z����3 ��͂��ׂē���I�����d��z���ł������Ƃ������݂�ꂽ 5�j�i���x��Ⅳb�j�B�ȏ��5 �҂́C�S��������͂��̑�������؏���ł��������C133 ��̐؏����ΏۂƂ��āC���o���זE�f�z�����T�哮�������p�ߓ]�ڂƂƂ��ɁC�Ɨ����������Ĕ��\�����q�ł������Ƃ����� 6�j�i���x��Ⅳb�j���݂�ꂽ�B
����C���o���זE�f�z���ł����Ă��\��ɉe�����Ȃ��Ƃ����͈ȉ���3 �҂���������B1 �߂́C157 �̐؏����76 �̔�؏���̂�����ɂ����Ă��C�זE�f�z����ƉA����Ő������Ԓ����l�̍��͔F�߂Ȃ������i�؏���F13.6 �J�� vs 13.5 �J���C��؏���F5.9 �J�� vs 6.1 �J���j�Ƃ����ł��� 7�j�i���x��Ⅳb�j�B2 �߂́C135 �̐؏����ΏۂƂ��āC���Ĕ��������ԁE�S�������ԂƂ��ɍזE�f�z����C�A����ԂɗL�Ӎ��͔F�߂��C�זE�f�z���ł��؏��������ꍇ������������݂�ꂽ�Ƃ����ł��� 8�j�i���x��Ⅳb�j�B3 �߂́C134 �̐؏����ΏۂƂ��āC����I�����d���F�߂Ȃ��זE�f�z���Q�́C�זE�f�A���Q�Ɣ�r���ėL�ӂɎ�ᇌa���傫���C�O���E����Z����F�߂�i�s�Ǘ�ł��������C�p�㐶�����Ԃɍ��͔F�߂��Ȃ������Ƃ���ł��� 9�j�i���x��Ⅳb�j�B���̕��ł��C�����d��̂Ȃ��זE�f�z����̂Ȃ��ɂ͔�r�I�����������F�߂��Ƃ���Ă���C�܂��Ӊ��s���ȍזE�W��ƌǗ��������זE�́C�����Ĕ��̊댯���q�ł������Ƃ����זE�f�����̓������L�q����Ă��� 9�j�B
��L�̕Ƃ͂��قȂ��������Ƃ��āC65 �̐؏���ł͍זE�f�z���Q���S�������ԁE���Ĕ��������Ԃ̒Z�k��F�߂��̂ɑ��C86 �̔�؏���ł͍זE�f�z����C�A����̊ԂŐ������Ԃɍ��͔F�߂�ꂸ�C����I�����d��̂Ȃ��זE�f�z����ł͐؏��Q�����ː����w�Ö@���{�s���ꂽ�Q�̂ق����������Ԃ̉�����F�߂��Ƃ�����݂�ꂽ 10�j�i���x��Ⅳb�j�B
�܂��C�������CEA ��RT-PCR �z���ł��������̂͗L�ӂɍĔ������㏸����Ƃ����� 11, 12�j�i���x��Ⅳa�j�C�؏��p�����O�̑�ʕ��o���ɂ�蕠���Ĕ������ቺ�����Ƃ����� 13�j�i���x��Ⅳa�j���݂�ꂽ�B
����CQ �ɑ���O���������CRCT �͊F���ł��邽�߁C���o���זE�f�z���X���ɑ����X�؏����s���ׂ����ۂ��͌����_�ł͖��炩�ł͂Ȃ��B����̂���Ȃ�Տ����������҂����B
�� �����ւ̒�
�X���͈����x���ɂ߂č������߁C�̓]�ڂ���p�ߓ]�ڂȂǂ̗\��ɗ^����e�����C���o���V�����זE����̉e���𔖂߂Ă��܂��\���͂���B������ɂ���C�؏���p�̐���ɂ��Ă͍��㌟�����d�˂Ė��炩�ɂ����ׂ��ł���B
�� ���p����
1�j Makary MA, Warshaw AL, Centeno BA, et al. Implications of peritoneal cytology for pancreatic cancer management. Arch Surg 1998�G133�F361-365.
2�j Nakatsuka A, Yamaguchi K, Shimizu S, et al. Positive washing cytology in patients with pancreatic cancer indicates a contraindication of pancreatectomy. Int J Surg Investig 1999�G1�F311-317.
3�j Warshaw AL. Implications of peritoneal cytology for staging of early pancreatic cancer. Am J Surg 1991�G161�F26-29.
4�j Clark CJ, Traverso LW. Positive peritoneal lavage cytology is a predictor of worse survival in locally advanced pancreatic cancer. Am J Surg 2010�G199�F657-662.
5�j Lei S, Kini J, Kim K, et al. Pancreatic cancer. Cytologic study of peritoneal washings. Arch Surg 1994�G129�F639-642.
6�j Shimada K, Sakamoto Y, Sano T, et al. The role of paraaortic lymph node involvement on early recurrence and survival after macroscopic curative resection with extended lymphadenectomy for pancreatic carcinoma. J Am Coll Surg 2006�G203�F345-352.
7�j Yamada S, Takeda S, Fujii T, et al. Clinical implications of peritoneal cytology in potentially resectable pancreatic cancer�Fpositive peritoneal cytology may not confer an adverse prognosis. Ann Surg 2007�G246�F254-258.
8�j Meszoely IM, Lee JS, Watson JC, et al. Peritoneal cytology in patients with potentially resectable adenocarcinoma of the pancreas. Am Surg 2004�G70�F208-213.
9�j Yachida S, Fukushima N, Sakamoto M, et al. Implications of peritoneal washing cytology in patients with potentially resectable pancreatic cancer.Br J Surg 2002�G89�F573-578.
10�j Konishi M, Kinoshita T, Nakagohri T, et al. Prognostic value of cytologic examination of peritoneal washings in pancreatic cancer. Arch Surg 2002�G137�F475-480.
11�j Eguchi H, Ohigashi H, Takahashi H, et al. Presence of minute cancer cell dissemination in peritoneal lavage fluid detected by reverse transcription PCR is an independent prognostic factor in patients with resectable pancreatic cancer. Surgery 2009�G146�F888-895.
12�j Kelly KJ, Wong J, Gladdy R, et al. Prognostic impact of RT-PCR-based detection of peritoneal micrometastases in patients with pancreatic cancer undergoing curative resection. Ann Surg Oncol 2009�G16�F3333-3339.
13�j Yamamoto K, Shimada S, Hirota M, et al. EIPL�iextensive intraoperative peritoneal lavage�jtherapy significantly reduces peritoneal recurrence after pancreatectomy in patients with pancreatic cancer. Int J Oncol 2005�G27�F1321-1328.
- CQ 2-3
- �X�������ɑ��Ă��X���\��w���؏��ɂ����āC�݁i�S�݂��邢�͈��S�݁j����������Ӌ`�͂��邩�H
| ����
|
�X�������ɑ����X���\��w���؏��ɂ����āC�݁i�S�݂��邢�͈��S�݁j�����ɂ���Ď�p���Ԃ͒Z�k����C�o���ʂ͏��Ȃ��C�܂��������ቺ�͂Ȃ��i�O���[�hC1�j�B ����ŁC�݁i�S�݂��邢�͈��S�݁j�����ɂ��p�㍇���ǂ̒ቺ�CQOL�C�p���X�@�\�C�h�{��Ԃ̉��P�ɂ��Ă͖��炩�ł͂Ȃ��i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�X�������ɑ��Ă͏]���C2/3 �̈ݐ؏����X���\��w���؏��ipancreato duodenectomy�GPD�j���L���s���Ă����B����@�\�����̍l���̕��y�ɂ��������C�H��ւƂƂ��Ɉ݂���������H��։����X���\��w���؏��ipylorus preserving pancreatoduodenectomy�GPPPD�j���s���{�݂������Ȃ��Ă��Ă���B
PPPD ��PD ���r����RCT ��4 �́i�p���j������݂̂ł���C���ꂼ��ᐔ��16 vs 15�C37 vs 40�C87 vs 83�C64 vs 66 �Ə��Ȃ� 1-4�j�i���x��Ⅱ�j�BPPPD ��PD ���r�������^�A�i���V�X��2007 �N�ȍ~��4 �Ҕ��\���ꂽ 5-8�j�i���x��Ⅰ�j�B�����͂�����RCT�𒆐S�ɍs���Ă��� 1-4�j�i���x��Ⅱ�j�B4 �҂̃��^�A�i���V�X�͑Ώۂ������Ɉ���Ă���C���^�A�i���V�X�̕��@�C��͂������q���قȂ�B�������C��p���Ԃ�PPPD ��PD ���Z���C�o���ʂ�PPPD ��PD ��菭�Ȃ��Ƃ�����̂������B�����ǁC��p���S�͕ς��Ȃ��Ƃ�����̂������B1 �҂ł�PPPD ��PD ���\��ǍD�ł���ƕ��Ă��� 7�j�BDiener ���RCT �Ԃł̔�r�̕��@�_�̈Ⴂ�C���ʂ̃p�����[�^�̈Ⴂ���傫�����Ƃ��w�E���Ă��� 5�j�BKaranicolas ��͗��Q�̍�����������ɂ͂���ɕ��@�_�I�ɋ��͂ȁC�傫�ȃg���C�A�����K�v���Əq�ׂĂ��� 6�j�B
PPPD��PD �̔�r�ł͍L���X���\��w���̈���i�X�������C���_�NJ��C���������Ȃǂ��܂ށj�̌����������C�X�������Ɍ����������͏��Ȃ��B�g���p�ƒʏ��p�̔�r�̂Ȃ��ŁC�ЂƂ̌������ڂƂ��Ĉݐ؏��̗L�����������Ă�����̂��CRCT 9�j�i���x��Ⅱ�j�ɂ����Ă��C�������̕��� 10-12�j�i���x��Ⅴ�j�ɂ����Ă������B���̍ہC�ق��̈��q�i�����p�߂�㕠���s���̒��x�Ȃǁj�̉e�������O�ł��Ȃ��B�p���QOL�iquality of life�j�C�X�@�\�C�h�{��ԂȂǂ̕]���@�����܂��܂ł���B�ȏ�̂悤�Ȗ��_���܂�ł���B
�� �����ւ̒�
PPPD ��PD �̌������X������������������L���܂���ΏۂƂ������̂������C�X�������Ɍ��������̂͏��Ȃ��B��͂ł̑����Ⓑ���̍����ǁCQOL �̌��������̒�`���_���ňقȂ�C�������̌����ɂ����Ē����ώ@�������̂͏��Ȃ��B�ŋ߂̃��^�A�i���V�X�ł́CPPPD ��PD ����p���Ԃ��Z���C�o���ʂ����Ȃ����C�\��͕ς��Ȃ��Ƃ̕�����B�X�������݂̂ɍi��C�p�㑁���Ⓑ���̍����ǁC�h�{��ԁC�X�@�\�CQOL �Ȃǂɂ��Ă̏ڍׂ�RCT �̌������]�܂��B
�� ���p����
1�j Lin PW, Lin YJ. Prospective randomized comparison between pylorus-preserving and standard pancreaticoduodenectomy. Br J Surg 1999�G86�F603-607.
2�j Wenger FA, Jacobi CA, Haubold K, et al. Gastrointestinal quality of life after duodenopancreatectomy in pancreatic carcinoma. Preliminary results of a prospective randomized study�Fpancreatoduodenectomy or pylorus-preserving pancreatoduodenectomy. �mArticle in German�n Chirurg 1999�G70�F1454-1459.
3�j Tran KT, Smeenk HG, van Eijck CH, et al. Pylorus preserving pancreaticoduodenectomy versus standard Whipple procedure�Fa prospective, randomized, multicenter analysis of 170 patients with pancreatic and periampullary tumors. Ann Surg 2004�G240�F738-745.
4�j Seiler CA, Wagner M, Bachmann T, et al. Randomized clinical trial of pylorus-preserving duodenopancreatectomy versus classical Whipple resection-long term results. Br J Surg 2005�G92�F547-556.
5�j Diener MK, Knaebel HP, Heukaufer C, et al. A systematic review and meta-analysis of pylorus-preserving versus classical pancreaticoduodenectomy for surgical treatment of periampullary and pancreatic carcinoma. Ann Surg 2007�G245�F187-200.
6�j Karanicolas PJ, Davies E, Kunz R, et al. The pylorus�Ftake it or leave it�H Systematic review and meta-analysis of pylorus-preserving versus standard whipple pancreaticoduodenectomy for pancreatic or periampullary cancer. Ann Surg Oncol 2007�G14�F1825-1834.
7�j Iqbal N, Lovegrove RE, Tilney HS, et al. A comparison of pancreaticoduodenectomy with pylorus preserving pancreaticoduodenectomy�Fa meta-analysis of 2822 patients. Eur J Surg Oncol 2008�G34�F1237-1245.
8�j Fitzmaurice C, Seiler CM, Büchler MW, et al. Survival, mortality and quality of life after pylorus-preserving or classical Whipple operation. A systematic review with meta-analysis.�mArticle inGerman�n Chirurg 2010�G81�F454-471.
9�j Yeo CJ, Cameron JL, Lillemoe KD, et al. Pancreaticoduodenectomy with or without distal gastrectomy and extended retroperitoneal lymphadenectomy for periampullary adenocarcinoma, part 2�Frandomized controlled trial evaluating survival, morbidity, and mortality. Ann Surg 2002�G236�F355-366�Gdiscussion 66-68.
10�j Iacono C, Accordini S, Bortolasi L, et al. Results of pancreaticoduodenectomy for pancreatic cancer�Fextended versus standard procedure. World J Surg 2002�G26�F1309-1314.
11�j Yamaguchi K, Shimizu S, Yokohata K, et al. Pancreatic carcinoma�Freappraisal of surgical experiences in one Japanese university hospital. Hepatogastroenterology 1999�G46�F3257-3262.
12�j Yeo CJ, Cameron JL, Lillemoe KD, et al. Pancreaticoduodenectomy for cancer of the head of the pancreas. 201 patients. Ann Surg 1995�G221�F721-731�Gdiscussion 731-733.
CQ 2-4�@�X���ɑ���喬�����؏��͗\������P���邩�H
| ����
|
�X���ɑ��č����������ړI�Ƃ����\�h�I�喬�����؏��ɂ��\�オ���P���邩�ۂ��͖��炩�ł͂Ȃ��B�喬�����؏��ɂ��؏��f�[����є����ʂɂ�������Z�����A���ɂł���Ǘ�Ɍ���K���ƂȂ�i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�喬�����؏��͏p�O���邢�͏p�������Ŗ喬�Z�����^�����C���邢�͖喬�Z���z����ɑ��čs���ꍇ���������C�喬���X���̈ꕔ�ƍl���č����������ړI�Ƃ��ė\�h�I�ɍs���ꍇ������B
���{�X���w���X���o�^20 �N�Ԃ̑����ɂ��ƁC�X�����ʏ�^�X���؏���ɂ�����喬�����؏��Ɨ\��ɂ����āC�喬�Z������̂Ȃ��ŁC761 ��̖喬�����؏���{�s���1,219 ��̖喬�����؏���̐������Ԓ����l�C5 �N�����������ꂼ��9.7 �J���C5.9����10.2 �J���C7.4���ŗL�Ӎ��Ȃ��C���l���X�̔������ɂ����āC�喬�Z������̂Ȃ��ŁC388��̖喬�����؏���{�s���148 ��̖喬�����؏���̐������Ԓ����l�C5�N�����������ꂼ��9.1�J���C9.2����8.7�J���C8.3���ŗL�Ӎ��Ȃ��ƕ��Ă���B
�喬�����؏���Ɩ喬�����؏���{�s����r����13 �҂̂̕���1 �� 1�j�i���x��Ⅳb�j�������Ă��ׂĂ��C�����̐��������]�߂�Ƃ��Ă��� 2-13�j�i���x��Ⅳb�j 14�j�i���x��Ⅰ�j�B���̂Ȃ��ŁC�喬�����؏����Ȃ���Ȃ�Ȃ��Ǘ�͍L�͈͂Ɍ㕠���Z�����i�s�Ⴊ�������ߓK�������i�ɂ���K�v������Ƃ����� 1�j�i���x��Ⅳb�j�C39 ��C160 ��̐؏����ΏۂƂ��āC�喬�����؏���͏o���ʂ������Ȃ���@���Ԃ������Ȃ�Ƃ���� 2, 3�j�i���x��Ⅳb�j�C34 ��̐؏����ΏۂƂ��āC�喬�����؏���͐؏��f�[�̊��̉A������\��̌���Ɋ�^���Ȃ������Ƃ����� 4�j�i���x��Ⅳb�j�̂悤�ɔے�I�Ȍ������݂�ꂽ�B����������ŁC1,212 ��̖L�x�ȏǗᐔ��ΏۂƂ��āC�����؏����ł���Ζ喬�����؏����̊g���p�ł������\�オ������ꍇ������Ƃ����� 5�j�i���x��Ⅳb�j�C194 ��C220 ��C482 ��C593 ��̐؏���̌����ŁC�������C�����ǔ������͖喬�����؏���{�s��Ɠ����ŁC�喬�����؏��͈��S�Ɏ{�s������Ƃ����� 6-9�j�i���x��Ⅳb�j�C81 ��C32 ��C110 ��̐؏����ΏۂƂ��āC�؏��f�[����є����ʂɂ�������Z�����A���ł��邱�Ƃ��������Ɋ֗^���Ă���Ƃ����� 10-12�j�i���x��Ⅳb�j�̂悤�ɍm��I�Ȍ������݂�ꂽ�B�܂��C110 ����X���͌��Ǎ����؏���ɂ����āC�������̏Ǐ�ɘa��p����\��͗ǍD�ŁC�������̖喬�����؏���{�s��Ɠ����̗\��ł������Ƃ������݂�ꂽ 13�j�i���x��Ⅳb�j�B����ɁC2010 �N��Chua ��ɂ��1,458 ��̌n���I���r���[�ł́Chigh volume center �ɂ����錌�Ǎ����؏����{�X���\��w���؏��p�{�s��̏p�㍇���ǁC���S���C�������́C�W���X���\��w���؏��p�{�s��Ɠ����ł���ƕ��ꂽ 14�j�i���x��Ⅰ�j�B
�O�q�̂悤�Ȗ喬�����؏���{�s��Ƃ̔�r���Ȃ�7 �҂̕ł́C�喬�����؏��̈Ӌ`�͂��܂��܂ł���BR0 �؏�121 ��̕a���w�I�����Ŗ喬�ǐZ���i�B�x�ʂŒ������Z�����Ă���Ǘ�͔�؏��ƕς��Ȃ��\��ł���C�O���܂ł̐Z����Ŗ喬�����؏�����C�喬�Z�����Ȃ��喬��؏��Ǘ�ƑS�������̗\��ƕ�����̂����� 15�j�i���x��Ⅳb�j�B�܂��C212 ��̐؏����ΏۂƂ��āC�p�O���Ǒ��e�����Ŗ喬�Z���̒��x�ނ��C�喬�Z�����y�x�ł���قǐ؏��f�[����є����ʂɂ�������Z���̉A�����������C�\�オ�ǍD�ł������Ƃ�������� 16�j�i���x��Ⅳb�j�B176 ����X�������؏��Ǘ��ΏۂƂ��āCR2 �؏��̓����p�ߓ]�ځC�喬�n�ւ̐Z���C�X�O�_�o�p�Z���ƂƂ��ɓƗ������\��s�Lj��q�ł������Ƃ�����̂����� 17�j�i���x��Ⅳb�j�B����C282 ��̊g���p���ΏۂƂ��āC�����xB �ȏ�Ȃ�Ίg���p�̈Ӌ`������Ƃ������ 18�j�i���x��Ⅳb�j�̂悤�ɁC�喬�Z���̒��x�⍪���x�ɂ��喬�����؏��̈Ӌ`���ς���Ă���Ƃ����C�喬�o�C�p�X�J�e�[�e���@��p����114 ��̐؏����ΏۂƂ��āC�����Z����ł͖喬�����؏��̓K�����Ȃ��Ȃ�Ƃ���� 19�j�i���x��Ⅳb�j���������B����ɁC�喬�������؏����邱�ƂŐ؏��f�[����є����ʂɂ�������Z�����A�����ł���Ǘ�Ɍ���C�喬�����؏��̓K���ƂȂ�Ƃ̕������� 20�j�i���x��Ⅳb�j�B����ɂ���250 ��̐؏���̂����C171 ��i68.4���j�̖喬�����؏��ᒆ�C�p��2 �N���邢��3 �N������̂قƂ�ǂ��喬�Z���iPV�j�z���ł������ɂ�������炸�C�؏��f�[����є����ʂɂ�������Z���iDPM�j���A���ł������ƕ��Ă��� 21�j�B���Ȃ킿�CPV�|DPM�|��PV�{DPM�|��DPM�{�̏��ɗ\�オ�����Ȃ邽�ߔ����ʂ��d�v�ł���ƕ��Ă��� 21�j�i���x��Ⅳb�j�B
���܂ł̂Ƃ���C����CQ �ɑ���O���������CRCT �͊F���ł���C�n���I���r���[���������p����20 �҂͂̕��ׂĎ�����̌������̌����ł���B���̂��߁C���Ȃ��Ƃ������_�ł͗\�h�I�喬�����؏��ɂ��\�オ���P����Ƃ������m�ȃG�r�f���X�́C�\���ł͂Ȃ��Ƃ��킴��Ȃ��B
�� �����ւ̒�
�喬�Z���̋^�����C���邢�͖喬�Z���z����ɑ���ꍇ�́C���Ȃ��Ƃ���v�����Z���킸�C�؏��f�[����є����ʂɂ�������Z�����A���ɂł���C�喬�����؏��ɂ�蒷�������Ⴊ�����邱�Ƃ�����ƍl������B
�� ���p����
1�j Shimada K, Sano T, Sakamoto Y, et al. Clinical implications of combined portal vein resection as a palliative procedure in patients undergoing pancreaticoduodenectomy for pancreatic head carcinoma. Ann Surg Oncol 2006�G13�F1569-1578.
2�j Howard TJ, Villanustre N, Moore SA, et al. Efficacy of venous reconstruction in patients with adenocarcinoma of the pancreatic head. J Gastrointest Surg 2003�G7�F1089-1095.
3�j Hristov B, Reddy S, Lin SH, et al. Outcomes of adjuvant chemoradiation after pancreaticoduodenectomy with mesenterico-portal vein resection for adenocarcinoma of the pancreas. Int J Radiat Oncol Biol Phys 2010�G76�F176-180.
4�j van Geenen RC, ten Kate FJ, de Wit LT, et al. Segmental resection and wedge excision of the portal or superior mesenteric vein during pancreatoduodenectomy. Surgery 2001�G129�F158-163.
5�j Imaizumi T, Hanyu F, Harada N, et al. Extended radical Whipple resection for cancer of the pancreatic head�Foperative procedure and results. Dig Surg 1998�G15�F299-307.
6�j Hartel M, Niedergethmann M, Farag-Soliman M, et al. Benefit of venous resection for ductal adenocarcinoma of the pancreatic head. Eur J Surg 2002�G168�F707-712.
7�j Toomey P, Hernandez J, Morton C, et al. Resection of portovenous structures to obtain microscopically negative margins during pancreaticoduodenectomy for pancreatic adenocarcinoma is worthwhile. Am Surg 2009�G75�F804-809.
8�j Yekebas EF, Bogoevski D, Cataldegirmen G, et al. En bloc vascular resection for locally advanced pancreatic malignancies infiltrating major blood vessels�Fperioperative outcome and long-term survival in 136 patients. Ann Surg 2008�G247�F300-309.
9�j Martin RC 2nd, Scoggins CR, Egnatashvili V, et al. Arterial and venous resection for pancreatic adenocarcinoma�Foperative and long-term outcomes. Arch Surg 2009�G144�F154-159.
10�j Nakagohri T, Kinoshita T, Konishi M, et al. Survival benefits of portal vein resection for pancreatic cancer. Am J Surg 2003�G186�F149-153.
11�j Zhou GW, Wu WD, Xiao WD, et al. Pancreatectomy combined with superior mesenteric-portal vein resection�Freport of 32 cases. Hepatobiliary Pancreat Dis Int 2005�G4�F130-134.
12�j Riediger H, Makowiec F, Fischer E, et al. Postoperative morbidity and long-term survival after pancreaticoduodenectomy with superior mesenterico-portal vein resection. J Gastrointest Surg 2006�G10�F1106-1115.
13�j Boggi U, Del Chiaro M, Croce C, et al. Prognostic implications of tumor invasion or adhesion to peripancreatic vessels in resected pancreatic cancer. Surgery 2009�G146�F869-881.
14�j Chua TC, Saxena A. Extended pancreaticoduodenectomy with vascular resection for pancreatic cancer�Fa systematic review. J Gastrointest Surg 2010�G14�F1442-1452.
15�j Fukuda S, Oussoultzoglou E, Bachellier P, et al. Significance of the depth of portal vein wall invasionafter curative resection for pancreatic adenocarcinoma. Arch Surg 2007�G142�F172-179�Gdiscussion 180.
16�j Nakao A, Harada A, Nonami T, et al. Regional vascular resection using catheter bypass procedure for pancreatic cancer. Hepatogastroenterology 1995�G42�F734-739.
17�j Kato K, Yamada S, Sugimoto H, et al. Prognostic factors for survival after extended pancreatectomy for pancreatic head cancer�Finfluence of resection margin status on survival. Pancreas 2009�G38�F605-612.
18�j ����r�G�C�H�����C���c�M��ÁC���D�X���ɑ���g���p�͗\��ɍv���������D������O��2000�G30�F120-126.
19�j Nakao A, Takagi H. Isolated pancreatectomy for pancreatic head carcinoma using catheter bypass of the portal vein. Hepatogastroenterology 1993�G40�F426-429.
20�j Nakao A, Takeda S, Sakai M, et al. Extended radical resection versus standard resection for pancreatic cancer�Fthe rationale for extended radical resection. Pancreas 2004�G28�F289-292.
21�j Nakao A, Takeda S, Inoue S, et al. Indications and techniques of extended resection for pancreatic cancer. World J Surg 2006�G30�F976-982�Gdiscussion 983-984.
CQ 2-5�@�X���ɑ��Ċg�僊���p�߁E�_�o�p�s���̈Ӌ`�͂��邩�H
| ����
|
�X���ɑ���g�僊���p�߁E�_�o�p�s��������������Ɋ�^���邩�ۂ��͖��炩�łȂ��C�s���悤���߂邾���̍��������m�ł͂Ȃ��i�O���[�hC2�j�B |
|---|
�� �G�r�f���X
�X���͐����w�I�����x�������C�ق��̏�������ɔ�ׂ��̊O�Ȏ��Ð��т͋ɂ߂ĕs�ǂł���B�������C���܂��܂ȏW�w�I���Â����B�������݂ɂ����Ă��O�ȓI�؏��݂̂��B��̍����I���Âł���B�킪���ł͉��u�]�ڂ�F�߂Ȃ��X���ɑ��C��ᇋߖT�����p�ߓ]�ڂ̗L���ɂ�����炸�ϋɓI�Ƀ����p�߂�_�o�p�̊g��s�����s����p�i������g���p�j��1980 �N�ォ��1990 �N��ɂ����čs���Ă��� 1-10�j�i���x��Ⅳb�j�B���ď����ł��X���ɑ��ϋɓI�Ȋg��؏����s�����͂��邪�C�����ǔ�������݉@���S�����������u���т��s�ǂł������Ƃ̕��������� 11-17�j�i���x��Ⅳb�j�B���̂��߉��ď����ł́C�����p�߂�_�o�p�s�����邢�͌��Ǎ����؏����s��Ȃ���p�i������W����p�j���s����̂���ʓI�ƂȂ�C��p�P�Ǝ��Â̌��E���F������Ă��� 18, 19�j�i���x��Ⅱ�j�B���̂悤���X���ɂ����郊���p�߂�_�o�p�s���̈Ӌ`�ɂ��ẮC�킪���Ɖ��ď����̊Ԃł͍l�����ɑ傫�ȍ��ق��������B
�X���ɑ���W���s���Ɗg��s���̗��҂��r����RCT ��1990 �N�ォ��2000 �N��ɂ����ĉ��Ă��3 ���ꂽ 20-24�j�i���x��Ⅱ�j�i�\2�j�B�����͂̕��ׂďp�㐶�����Ԃɍ��͂Ȃ��C�p�㍇���Ǘ����g��s���Q�ŗL�ӂɑ����Ƃ̌��ʂł������B�������C���ď���������ꂽRCT �ɂ�����g��s���̒��x�́C���{���̓O�ꂵ�������p�߁E�_�o�p�s�����K�������s���Ă���킯�ł͂Ȃ������B�����ŁC�킪���ɂ����Ă����Ď��̂�����W����p�Ɠ��{���̓O�ꂵ���g���p���r����RCT�i�����J���Ȃ����������nj����j���s��ꂽ 25, 26�j�i���x��Ⅱ�j�i�\2�j�B�킪����RCT �ɂ����Ă��C�W���s���Q�Ɗg��s���Q�̊ԂŐ������ɗL�Ӎ��͂Ȃ��i1 �N�C3 �N�������͕W����p�Q��78���C28���C�g���p�Q��54���C18���Ɗg���p�Q�̂ق�����s�ǁj�C�p���QOL �͊g���p�Q���L�ӂɕs�ǂł������B2007 �N�ɂ��X���ɑ���W���s���Ɗg��s���̈Ӌ`�ɂ��ăV�X�e�}�e�B�b�N�E���r���[����у��^�A�i���V�X���s�������ʂ�����C�X���ɑ���g��s���͐���������Ɋ�^���邱�Ƃ͂Ȃ��C�ނ���p�㍇���ǔ�������������X���ɂ���ƌ��_�Â����Ă��� 27�j�i���x��Ⅰ�j�B���������āC�����_�ł��X���ɑ���g��s������p��ϋɓI�ɐ������鍪���͂Ȃ��C�ނ���p�㍇���ǔ�����\�h���邤���ł͍s���ׂ��ł͂Ȃ��ƍl������B
| Italian | American | Japanese | ||||||
|---|---|---|---|---|---|---|---|---|
| Johns Hopkins* | Mayo Clinic | |||||||
| �W�� | �g�� | �W�� | �g�� | �W�� | �g�� | �W�� | �g�� | |
�Ǘᐔ |
40 | 41 | 146 | 148 | 40 | 39 | 51 | 50 |
��p���ԁi���j |
372 | 397 | 354 | 384 | 378 | 450 | 426 | 547 |
�p���A���ʁiU�j |
1.95 | 2.07 | 0.5 | 0.5 | — | — | 2.1 | 2.4 |
PD/PPPD/SSPPD |
20/20/0 | 18/23/0 | 21/125/0 | 148/0/0 | 40/0/0 | 39/0/0 | 13/19/19 | 11/23/16 |
�喬�؏� |
— | — | 4�i3���j | 4�i3���j | 9�i23���j | 8�i21���j | 24�i47���j | 24�i48���j |
�����p�ߊs���� |
13.3 | 19.8 | 17 | 28.5 | 15 | 36 | 13.3 | 40.1 |
�p��݉@���� |
22.7 | 19.3 | 11.3 | 14.3 | 13 | 16 | 43.8 | 42.4 |
�����Ǘ� |
18�i45���j | 14�i34���j | 42�i29���j | 64�i43���j | ����8�� | ����42�� | ����0 | ����48�� |
���S�� |
2�i5���j | 2�i5���j | 6�i4���j | 3�i2���j | 0 | 1�i3���j | 0 | 1�i2���j |
�\�� |
���Q�ō��Ȃ� | ���Q�ō��Ȃ� | ���Q�ō��Ȃ� | ���Q�ō��Ȃ� | ||||
*�Fperiampullary carcinomas ���܂ށB
�� �����ւ̒�
�{CQ �ŏЉ��RCT �͖ړI�������ł��e�X�̍��̈�Î���f���Ĕ����Ƀv���g�R�[�����قȂ邽�߂��̌��ʂ̉��߂ɂ͒��ӂ�v����B�������������RCT �ł��g��s����p�ɗ\������P������ʂ͂Ȃ��C�ނ���p��̍����ǂ������X���ɂ���C�g��s����p�̈Ӌ`�͂قڔے肳�ꂽ�ƌ����Ă悢�B�X���̎�p�ł͐؏��f�[�����A���ɂ��邱�Ƃ��܂��匴���ł���C���̂��߂̓w�͂�ɂ���ł͂����Ȃ��B�������C���x�ȋǏ��Z������p�ߓ]�ڂ�����悤�ȏǗ�́C���Ƃ��g��s����p���s�����Ƃ��Ă��\��͋ɂ߂ĕs�ǂł���B���������āC���̂悤�ȏǗ�͂ł��邾�������ǂ��N����Ȃ��悤�ɒ��ӂ��Ď�p���s���C���̌�̕⏕�Ö@�ɗ\����P���ʂ����҂����ق����悢�B
�����ŋ߂ł͐f�f���x�̐i���ɂ��C��葁���̒i�K�Ō������X���������Ă����B���̂悤�ȏǗ�ɂǂ��܂Ŋs�����s���ׂ��Ȃ̂��͍���̌�����v����B�g���p����T�ɔے肷��̂ł͂Ȃ��C����͐ϋɓI�Ȋs����p���K�v�ȏǗ�Ƃ����łȂ��Ǘ�����ɂ߂邽�߂̌������K�v�Ȃ̂�������Ȃ��B
�� ���p����
1�j Nagakawa T, Nagamori M, Futakami F, et al. Results of extensive surgery for pancreatic carcinoma. Cancer 1996�G77�F640-645.
2�j Takahashi S, Ogata Y, Miyazaki H, et al. Aggressive surgery for pancreatic duct cell cancer�Ffeasibility, validity, limitations. World J Surg 1995�G19�F653-659�Gdiscussion 660.
3�j Ozaki H, Kinoshita T, Kosuge T, et al. An aggressive therapeutic approach to carcinoma of the body and tail of the pancreas. Cancer 1996�G77�F2240-2245.
4�j Hirata K, Sato T, Mukaiya M, et al. Hirata K, Sato T, Mukaiya M,et al. Results of 1001 pancreatic resections for invasive ductal adenocarcinoma of the pancreas. Arch Surg 1997�G132�F771-776�Gdiscussion 777.
5�j Onoue S, Katoh T, Chigira H, et al. Carcinoma of the head of the pancreas. Hepatogastroenterology 2002�G49�F549-552.
6�j Hiraoka T, Uchino R, Kanemitsu K, et al. Combination of intraoperative radiation with resection of cancer of the pancreas. Int J Pancreatol 1990�G7�F201-207.
7�j Tsuchiya R, Tsunoda T, Yamaguchi T. Operation of choice for resectable carcinoma of the head of the pancreas. Int J Pancreatol 1990�G6�F295-306.
8�j MaNabe T, Ohshio G, Baba N, et al. Radical pancreatectomy for ductal cell carcinoma of the head of the pancreas. Cancer 1989�G64�F1132-1137.
9�j Ishikawa O, Ohhigashi H, Sasaki Y, et al. Practical usefulness of lymphatic and connective tissue clearance for the carcinoma of the pancreas head. Ann Surg 1988�G208�F215-220.
10�j Ishikawa O, Ohigashi H, Imaoka S, et al. Preoperative indications for extended pancreatectomy for locally advanced pancreas cancer involving the portal vein. Ann Surg 1992�G215�F231-236.
11�j Fortner JG. Regional pancreatectomy for cancer of the pancreas, ampulla, and other related sites. Tumor staging and results. Ann Surg 1984�G199�F418-425.
12�j Kremer B, Vogel I, Lüttges J, et al. Surgical possibilities for pancreatic cancer�Fextended resection. Ann Oncol 1999�G10 Suppl 4�F252-256.
13�j Gazzaniga GM, Cappato S, Papadia F, et al. D1 versus D2 pancreatoduodenectomy in surgical therapy of pancreatic head cancer. Hepatogastroenterology 2001�G48�F1471-1478.
14�j Henne-Bruns D, Vogel I, Lüttges J, et al. Surgery for ductal adenocarcinoma of the pancreatic head�Fstaging, complications, and survival after regional versus extended lymphadenectomy. World J Surg 2000�G24�F595-601�Gdiscussion 601-602.
15�j Capussotti L, Massucco P, Ribero D, et al. Extended lymphadenectomy and vein resection for pancreatic head cancer�Foutcomes and implications for therapy.�@Arch Surg 2003�G138�F1316-1322.
16�j Gebhardt C, Meyer W, Reichel M, et al. Prognostic factors in the operative treatment of ductal pancreatic carcinoma. Langenbecks Arch Surg 2000�G385�F14-20.
17�j Benassai G, Mastrorilli M, Mosella F, et al. Significance of lymph node metastases in the surgical management of pancreatic head carcinoma. J Exp Clin Cancer Res 1999�G18�F23-28.
18�j Lygidakis NJ, Sgourakis G, Georgia D, et al. Regional targeting chemoimmunotherapy in patients undergoing pancreatic resection in an advanced stage of their disease�Fa prospective randomized study. Ann Surg 2002�G236�F806-813.
19�j Lygidakis NJ, Stringaris K. Adjuvant therapy following pancreatic resection for pancreatic duct carcinoma�Fa prospective randomized study. Hepatogastroenterology 1996�G43�F671-680.
20�j Pedrazzoli S, DiCarlo V, Dionigi R, et al. Standard versus extended lymphadenectomy associated with pancreatoduodenectomy in the surgical treatment of adenocarcinoma of the head of the pancreas�Fa multicenter, prospective, randomized study. Lymphadenectomy Study Group. Ann Surg 1998�G228�F508-517.
21�j Yeo CJ, Cameron JL, Lillemoe KD, et al. Pancreaticoduodenectomy with or without distal gastrectomy and extended retroperitoneal lymphadenectomy for periampullary adenocarcinoma, part 2�Frandomized controlled trial evaluating survival, morbidity, and mortality. Ann Surg 2002�G236�F355-366�Gdiscussion 366-368.
22�j Nguyen TC, Sohn TA, Cameron JL, et al. Standard vs. radical pancreaticoduodenectomy for periampullary adenocarcinoma�Fa prospective, randomized trial evaluating quality of life in pancreaticoduodenectomy survivors. J Gastrointest Surg 2003�G7�F1-9�Gdiscussion 9-11.
23�j Stojadinovic A, Hoos A, Brennan MF, et al. Randomized clinical trials in pancreatic cancer. Surg Oncol Clin N Am 2002�G11�F207-229.
24�j Farnell MB, Pearson RK, Sarr MG, et al. A prospective randomized trial comparing standard pancreatoduodenectomy with pancreatoduodenectomy with extended lymphadenectomy in resectable pancreatic head adenocarcinoma. Surgery 2005�G138�F618-628�Gdiscussion 628-630.
25�j Nimura Y, Nagino M, Takao S, et al. Standard versus extended lymphadenectomy in radical pancreatoduodenectomy for ductal adenocarcinoma of the head of the pancreas�Flong-term results of a Japanese multicenter randomized controlled trial. J Hepatobiliary Pancreat Sci 2012�G19�F230-241.
26�j ���쐳�l�D���ʃv���g�R�[���Ɋ�Â��X����̊O�ȓI�Ö@�̕]���Ɋւ��錤���D�����J���Ȃ����������ɂ�錤���W-����15�N�x��-�C288-292.
27�j Michalski CW, Kleeff J, Wente MN, et al. Systematic review and meta-analysis of standard and extended lymphadenectomy in pancreaticoduodenectomy for pancreatic cancer. Br J Surg 2007�G94�F265-273.
CQ 2-6�@�i�J����j��؏���ł̗\�h�I�o�C�p�X�͐�������邩�H
| ����
|
�O�Ȑ؏���ړI�ɊJ������؏��ƂȂ������t���X���ɑ��āC�_�Nj����p�ɂ�錸���p�C�\�h�I�����p�����������i�O���[�hB�j�B |
|---|
�� �G�r�f���X
�X���̕ۑ��I���Â̑ΏۂƂȂ�̂́C�ǐ����t�C�\��w������ɂ��ʉߏ�Q�C�����u�ɂȂǂł���BCQ4-6�ł́C�O�Ȑ؏���ړI�ɊJ�����C��؏��ƂȂ������t���X���ɑ���_�Nj����p�ɂ�錸���p�C�\�h�I�����p�C���o�_�o�p�u���b�N�ɂ��Ă̂ݐG���B�ɘa��ÂɊւ��Ă͓��{�ɘa��È�Êw��̃z�[���y�[�W<http://www.jspm.ne.jp/guidelines/index.html>�G1, 2�j�i���x��Ⅵ�j���Q�Ƃ��ꂽ���B
�X���̊O�ȓI�⏕�Ö@�ɑ���RCT���܂Ƃ߂�������3���\����Ă��� 3-5�j�i���x��Ⅵ�j�B�ǐ����t�C�\��w������ɂ��ʉߏ�Q�C�����u�ɂ̏����ŋL�ڂ���B
- �ǐ����t�̌���
�����p�Ɋւ���ERC ���[�g���̃`���[�u�X�e���g�ƊO�ȓI�����p���r����RCT ��3 ���� 6-8�j�i���x��Ⅱ�j�C���^�A�i���V�X��2 ���� 9, 10�j�i���x��Ⅰ�j�BTaylor �� 9�j�̂����3 ��RCT 6-8�j�Ɋւ��郁�^�A�i���V�X�ł́C①�������s�C�d�Ǎ����ǂ͂��܂��܂Ŗ��炩�ȍ��͂Ȃ������C②�������`���[�u�X�e���g�ł͊O�ȓI�����p��������Ȃ鎡�Â�v�����C③30 �����S���ɗL�Ӎ��͂Ȃ������C④�O�Ȏ��Â͈��������̎��Â�v���Ȃ������C⑤�������I�`���[�u�X�e���g�ƊO�ȓI�����p�Ƃ̊Ԃɖ��炩�ȍ��͂Ȃ������Ƃ��C���傫��RCT �ŐV���ȃ��^���b�N�X�e���g�ƊO�ȓI�����p�Ƃ̔�r���K�v�ł���C�K��QOL �̕]�����K�v�ł���Əq�ׂĂ���BMoss �� 10�j�̈��������_�Ǖǂɑ���������I�`���[�u�X�e���g�ƊO�ȓI�����p��3 ��RCT 6-8�j���g�������^�A�i���V�X�ł́C�Z�p�I�����C���ÓI�����ɗ��Q�Ԃɍ��͂Ȃ������B�S�����ǂ̓X�e���g�ŗL�ӂɏ��Ȃ��C30 ���ȓ����S�̓X�e���g�̂ق����悢�X���ł������B���t�Ĕ��͗L�ӂɊO�ȓI�����p�ŏ��Ȃ������B��������QOL �͗��Q�Ԃɍ��͂Ȃ������B3 ��RCT �̂����C2 �̃V���[�Y�ł̓X�e���g�Q�ő����@�������Z�������B
���^���b�N�X�e���g�ƊO�ȓI�����p��RCT ��1 ����C���^���b�N�X�e���g�ƊO�ȓI�����p��RCT �ł͓������I���^���b�N�X�e���g�͊O�ȓI�����p�������CQOL �����悢�Ƃ̌��ʂł����� 11�j�i���x��Ⅱ�j�B
�o��o�̃��[�g�iPTE�j�ɂ��X�e���g���O�ȓI�����p���̔�r�ɂ��ẮC1986 �N��Bornman ��ɂ��RCT ������Ă��� 12�j�i���x��Ⅱ�j�BPTE �͍ŏ��̓��@�͒Z�����C�����@������PTE �ƊO�ȓI�����p�ƂňႢ�͂Ȃ��C�X�e���g�̕ǁC�����Ǖǂ��l����Ɨ��ҊԂɍ��͂Ȃ��Ƃ��Ă���B
�O�ȓI�����p�̏p���ɂ͒_嚢�����p�ƒ_�Nj����p�����邪�C�������r����Sarfeh ���RCT �ł́C�_嚢�����p�ł͍ċ���������ŁC�_�Nj����p�ł͊J�������悭�C�����_�Nj���ɂ͒_�Nj����p�̂ق����悢�Ƃ��Ă��� 13�j�i���x��Ⅱ�j�B
- �\�h�I����
�\�h�I�����ɂ��Ă�2 ��RCT �����\����Ă��� 14, 15�j�i���x��Ⅱ�j�B�X���̊O�ȓI�؏���ړI�ɊJ�����Ă���؏��ƂȂ邱�Ƃ���������C���̍ہC�\�h�I���������ƂȂ�B�J�����C�����ǂ̒ʉߏ�Q���Ȃ������Ǘ�ł�10�`20���ɂ͏����I�ɏ����ǂ̒ʉߏ�Q�����������Ƃ��m���Ă���CLillemoe �� 14�j��Van Heek �� 15�j��RCT �ł́C�������s�����Ƃɂ��C�����ǁC�p���C�p����@�����CQOL�C�\��ɕω��͂Ȃ��C�����I�Ɉ����Ȃǂ���K�v���Ȃ��Ȃ邽�߁C�\�h�I�����͈Ӌ`������Ƃ���Ă��� 14, 15�j�B����ɁC�����ł̏�従��Ƌt従��̕������r����Yilmaz ���RCT �ł́C���ҊԂɏp�㍇���ǁC�o���J�n�܂ł̊��ԁC�ĊJ�����C�㕔�����Ǐo���C�p���C���@�����Ɛ������ԂɗL�Ӎ��͂Ȃ����� 16�j�i���x��Ⅱ�j�B��従��̂ق����t従����L�ӂɎ�p���Ԃ������C�t従��Ɉݔr���x�������Ȃ��X���ɂ������B��従����t従����p��݂̈̔r�����Ԃ�L�ӂɉ��������B��従��̂ق����Տ��I�ɂ悢���ʂƂȂ�X���ɂ������B
�\�h�I�����ɂ��Ă�2 �̃��^�A�i���V�X��2009 �N�C2010 �N�ɕ���Ă��� 17, 18�j�i���x��Ⅰ�j�B�ǂ�����\�h�I�����͒Z���̌��ʂ������������C�����Ɉݏ\��w������������p�x���Ⴍ�C�J�����Ĕ�؏��ƂȂ����X���ɂ����Ă͈������s���Ă����ق����悢�Ƃ̌��ʂł������B
- �����u�ɂɑ���O�ȓI����
�����u�ɂɑ���O�ȓI���ÂɊւ��ẮC�J���� 19�j�i���x��Ⅱ�j�⋹�o���� 20�j�i���x��Ⅱ�j�̐_�o�u���b�N�ɂ��Ă�RCT ������Ă���B�J������50���G�^�m�[���ɂ��_�o�u���b�N�����Q�ƁC�v���Z�{�Ƃ��Đ����H�����𗘗p�����Q���r��������RCT �ł́C�ɂ݂̃X�R�A�̕��ς͗L�ӂɌy���������C���@�����S�C�����ǁC�o���ێ�J�n�C���@�����ɍ��͂Ȃ����� 19�j�B�܂��C�ɂ݂̂Ȃ��������҂ւ̐_�o�u���b�N�͒ɂ݂̃X�R�A���y�����C�ɂ݂̔�����L�ӂɒx�点���B����ɗ\��̉��P���L�ӂɔF�߂�ꂽ�B�ʂ̎�p�I�A�v���[�`�ł��闼�����o�����_�o�u���b�N�́C�ǐ��C�������X���u�ɂɑ��ėL���Ȏ��Ö@�ł��邱�Ƃ�������Ă��� 20�j�B
�� �����ւ̒�
�Տ��̏�ł͔�؏��X�����命�����߂錻�����l����ƌ����p�C�����ǃo�C�p�X�C�����u�ɏ����Ȃǂ͏d�v�ł��邪�C�킪���ł͂��u������ɂ���Ă������ł�����B��������p�ł̃o�C�p�X��V�K�X�e���g�̊J���E���P�Ȃǂ��i��ł��邽�߁C�M���x�̍���RCT ���s���C�������Ă����K�v������B
�� ���p����
1�j ��Ɋɘa�̂��߂̒��ÂɊւ���K�C�h���C��2010 �N�ŁD���{�ɘa��Êw��ɘa��ÃK�C�h���C�� �쐬�ψ���ҁC�����o�ŁC2010.
2�j �I�������҂̗A�t�Ö@�Ɋւ���K�C�h���C��2013 �N�ŁD���{�ɘa��Êw��ɘa��ÃK�C�h�� �C���ψ���ҁC�����o�ŁC2013.
3�j Kaido T. Randomized controlled trials on hepato-biliary-pancreatic surgery. J Hepatobiliary Pancreat Surg 2004�G11�F381-389.
4�j Andtbacka RH, Evans DB, Pisters PW. Surgical and endoscopic palliation for pancreatic cancer. Minerva Chir 2004�G59�F123-136.
5�j Kuhlmann KF, De Castro SM, Gouma DJ. Surgical palliation in pancreatic cancer. Minerva Chir 2004�G59�F137-149.
6�j Shepherd HA, Royle G, Ross AP, et al. Endoscopic biliary endoprosthesis in the palliation of malignant obstruction of the distal common bile duct�Fa randomized trial. Br J Surg 1988�G75�F1166-1168.
7�j Andersen JR, Sørensen SM, Kruse A, et al. Randomised trial of endoscopic endoprosthesis versus operative bypass in malignant obstructive jaundice. Gut 1989�G30�F1132-1135.
8�j Smith AC, Dowsett JF, Russell RC, et al. Randomised trial of endoscopic stenting versus surgical bypass in malignant low bileduct obstruction. Lancet 1994�G344�F1655-1660.
9�j Taylor MC, McLeod RS, Langer B. Biliary stenting versus bypass surgery for the palliation of malignant distal bile duct obstruction�Fa meta-analysis. Liver Transpl 2000�G6�F302-308.
10�j Moss AC, Morris E, Leyden J, et al. Malignant distal biliary obstruction�Fa systematic review and meta-analysis of endoscopic and surgical bypass results. Cancer Treat Rev 2007�G33�F213-221.
11�j Artifon EL, Sakai P, Cunha JE, et al. Surgery or endoscopy for palliation of biliary obstruction due to metastatic pancreatic cancer. Am J Gastroenterol 2006�G101�F2031-2037.
12�j Bornman PC, Harries-Jones EP, Tobias R, et al. Prospective controlled trial of transhepatic biliary endoprosthesis versus bypass surgery for incurable carcinoma of head of pancreas. Lancet 1986�G1�F69-71.
13�j Sarfeh IJ, Rypins EB, Jakowatz JG, et al. A prospective, randomized clinical investigation of cholecystoenterostomy and choledochoenterostomy. Am J Surg 1988�G155�F411-414.
14�j Lillemoe KD, Cameron JL, Hardacre JM, et al. Is prophylactic gastrojejunostomy indicated for unresectable periampullary cancer? A prospective randomized trial. Ann Surg 1999�G230�F322-328.
15�j Van Heek NT, De Castro SM, van Eijck CH, et al. The need for a prophylactic gastrojejunostomy for unresectable periampullary cancer�Fa prospective randomized multicenter trial with special focus on assessment of quality of life. Ann Surg 2003�G238�F894-902�Gdiscussion 902-905.
16�j Yilmaz S, Kirimlioglu V, Katz DA, et al. Randomised clinical trial of two bypass operations for unresectable cancer of the pancreatic head. Eur J Surg 2001�G167�F770-776.
17�j Hüser N, Michalski CW, Schuster T, et al. Systematic review and meta-analysis of prophylactic gastroenterostomy for unresectable advanced pancreatic cancer. Br J Surg 2009�G96�F711-719.
18�j Gurusamy KS, Kumar S, Davidson BR. Prophylactic gastrojejunostomy for unresectable periampullary carcinoma. Cochrane Database Syst Rev 2010�FCD008533.
19�j Lillemoe KD, Cameron JL, Kaufman HS, et al. Chemical splanchnicectomy in patients with unresectable pancreatic cancer. A prospective randomized trial. Ann Surg 1993�G217�F447-455�Gdiscussion 456-457.
20�j Ihse I, Zoucas E, Gyllstedt E, et al. Bilateral thoracoscopic splanchnicectomy�Feffects on pancreatic pain and function. Ann Surg 1999�G230�F785-790�Gdiscussion 90-91.
CQ 2-7�@�X���ɑ���������I��p�̈Ӌ`�́H
| ����
|
�X���ɑ���������I��p�͏Ǘ��I�ׂΈ��S�Ɏ{�s�\�ł���B�������u���т����コ���邩�ۂ��ɂ��Ă�high volume center �ł̏Ǘ�̒~�ςɂ�薾�炩�ɂ����ׂ��ł���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
1992 �N��Gagner �炪�����X���ɑ��镠�o�����X���\��w���؏�����Ĉȗ� 1�j�i���x��Ⅴ�j�C���X�ɕ��o�����X�؏��{�s�Ǘᐔ�͑���������B���������̑����͗ǐ��������邢�͒ራ���x�̎�ᇂɑ��čs���Ă����B�Z�����X�NJ��ɑ���������I�X�؏��͂悤�₭�ŋ߂ɂȂ���high volume center �ɂ����Ď{�s���������̂�����ł���B���B��25 �{�݂ŏW�v���ꂽ2005 �N��Mabrut ��̕ł́C�Z�����X�NJ���127 �ᒆ4 ��ɉ߂��� 2�j�i���x��Ⅳb�j�C2008 �N��Kooby ��ɂɂ��č�8 �{�݂̏W�v�ł�159 ��̕��o�����X�̔����؏��iLapDP�j�̂����B����10���i16/159 ��j�ɂƂǂ܂��Ă��� 3�j�i���x��Ⅳb�j�B2009 �N��Gagner ��ɂ�镠�o�����X���\��w���؏��p�iLapPD�j�̕������r���[�ł́C���W���ꂽ146�ᒆ�X����45 ��i30.8���j�� 4�j�i���x��Ⅵ�j�C2011 �N��Ammori ��̃V�X�e�}�e�B�b�N�E���r���[�ł́C���W���ꂽ987 ���LapDP �̂���139 �Ⴊ������ᇁC126 ���LapPD �̂���104 �Ⴊ������ᇂƕ���Ă��� 5�j�i���x��Ⅰ�j�B���̂悤�ɏ��X�ɏǗᐔ�͑�����������̂́C2011 �N���݂ł��Z�����X�NJ��̕��o������p��́C�T�d�ɓK����I��ōs���Ă���̂�����ł��낤�B�X���݂̂�ΏۂƂ���Տ������͂��܂����Ȃ����߁C���ł̖{CQ �ł́C�Z�����тɂ��Ă͗ǐ������𑽂��܂ޕ��̗p������Ȃ������B
LapDP �ɂ��āC2011 �N�ɔ��\���ꂽ���o�����X�؏��̃V�X�e�}�e�B�b�N�E���r���[��Ammori ���46 �_������987 ������W�����BLapDP �̂���83.9���̏ǗႪ�ǐ������Ɏ{�s����Ă����B��p����221 ���C�o����227mL�C�݉@����7.7 ���C�X�t�16.4���C�J���ڍs11.5���C��p���S��0.4���ł������B�ȏ�̌��ʂ���LapDP �͏Ǘ��I�ׂΈ��S�Ɏ{�s�\�ł���ƌ��_�Â����Ă��� 5�j�i���x��Ⅰ�j�B�P��{�݂�LapDP �ƊJ���X�̔����؏��p�iODP�j���r���������ł́C�Z�����т�ODP �Ɣ�r���āC�p�㍇���ǔ������͓����ł���C�o���ʂ����Ȃ��݉@�������Z�����Ƃ�����Ă��� 6�j�i���x��Ⅳb�j 7�j�i���x��Ⅳa�j�B�č���8 �{�݂���W�v����142 ���LapDP ��200 ���ODP ��case-match ������r���������ł́C��p����230 �� vs 216 ���ip �� 0.28�j�C�o����357mL vs 588mL�ip �� 0.001�j�C�d�升���� 10��vs 17���ip �� 0.08�j�C�X�t� 11��vs 18���ip ��0.10�j�C�݉@����5.9 �� vs 9.0 ���ip �� 0.001�j�ƁCLapDP �͒�N�P�ł���Ǘ�I���ɂ��ǍD�ȒZ�����т��������Ƃ��ł���Ƃ��Ă��� 3�j�i���x��Ⅳb�j�B�ߔN�C���{�b�g��p�̕����������� 8, 9�j�i���x��Ⅳb�j�BWaters ����X�̔����؏��ɂ����āC���{�b�g��p�͎�p���Ԃ��������o���ʂ͏��Ȃ��C�B�����������������Ƃ��Ă���B�݉@������4 ���ł���C�J����p��8 ���C���o������p��6���Ɣ�ׂĂ�����ɒZ�k����Ă��� 8�j�i���x��Ⅳb�j�B
LapPD �Ɋւ��āCAmmori ��̃V�X�e�}�e�B�b�N�E���r���[�ł́CLapDP �Ƃ͈قȂ�C89�������������Ɏ{�s����Ă����BLapPD ��14 �_���i126 ��j�����r���[����C��p����448 ���C�o����324mL�C�X�t�11.6���C�J���ڍs15���ł����� 5�j�i���x��Ⅰ�j�B���݂܂ł̒P��{�݂̕ł͍ő�K�͂ł���Kendrick ��̕ł́C���S������PD���{�s����62 �ᒆ�X����30 ��ł������B��p���Ԃ�368 ���C�o����240mL�C�݉@���������l7 ���C�X�t�18���C�݉@���S��1.6���i1/62�j�ł������B���ڂ̔�r�͂ł��Ȃ����C�J����p�Ɣ�r���đ��F�Ȃ��Z�����тƍl����ꂽ 10�j�i���x��Ⅳb�j�B������LapPD �ɂ����Ă͊J��PD �Ɠ�Q�Ԕ�r�����O���������͌��݂܂ł݂��Ȃ����߁C����Ȃ�Ǘ�̒~�ς��K�v�Ǝv����B
���̎����x�Ɋւ��āCKooby ��́C�J���p�ƕ��o�����ł̓����p�ߊs�����C�f�[�z�����͓����ł������ƕ��Ă��� 11�j�i���x��Ⅳb�j�BDulucq ��͒f�[�z������0��12�j�i���x��Ⅳa�j�CPalanivelu ��2.4���i2/82�j 13�j�i���x��Ⅳb�j�ƕ��Ă���C�f�[�z�����͒ᗦ�Ƃ̕������B����CBaker ���LapDP ��ODP �̔�r�ŁC�����p�ߊs������5.2 �� vs 9.4 �ip��0.04�j�ƗL�ӂɏ��Ȃ��������߁CLapDP �͈��������ɂ͕s�K�ł���ƌ��_���Ă��� 7�j�i���x��Ⅳa�j�B���̂悤�ɁC���܂����̕]���ɂ͂�������邽�߁C����̏Ǘ�W�ς�҂��˂Ȃ�Ȃ��B
�������тɊւ���͏Ǘᐔ�����Ȃ������C�ώ@���Ԃ��Z�����߁C���܂�����ꂽ�{�݂���̕ɂƂǂ܂��Ă���BPalanivelu ���9 ��̐Z�����X�NJ���5 �N��������19.1���ƕ��Ă��� 14�j�i���x��Ⅴ�j�BPugliese ���11 ����X���̕��ϐ������Ԃ�18 �J���ł��������Ă��� 15�j�i���x��Ⅳb�j�BKooby ���LDP ��ODP �̕��ϐ������Ԃ͂Ƃ���16 �J���ł���L�Ӎ���F�߂Ȃ������Ƃ��Ă��� 11�j�B��������p�̒�N�P���Ƃ������_������C�p�㑁���ɕ⏕���w�Ö@���J�n����Ƃ������_��C��N�P�̂��ߐ��݊��̑��B���}�������Ȃǒ������тɂ��D�e�����y�ڂ��\���ɂ��Ă�����̌�����҂������B
��������p�ɂ��Ƒ���p�Ɋւ��Ă����������݂���BRöthlin ����X�������ŏ\��w������Ǘ�ɑ��ĕ��o���������C�_�Nj������{�s���C�݉@������9 ���ԂƁC�J���p��21 ���ԂƔ�r���ĒZ�������Ƃ������т���Ă��� 16�j�i���x��Ⅳb�j�B����C�������I�X�e���g���u�Ƃ̗D��ɂ��ĕ��o�Ă�����̂Ǝv����B
�� �����ւ̒�
1990 �N��Ɏn�܂������o�����X�؏��p��20 �N�o�߂������݂ł����܂��X���ɑ�����{��͏����ɂƂǂ܂��Ă���B�Z�����т͊J���p�Ɣ�r���đ��F�Ȃ����߁C���҂̊�]������Γ������I��p��I�����邱�Ƃ͉\�Ǝv����B�����������p�ߊs���������Ȃ��Ƃ��������邱�ƂⒷ�����т̕����Ȃ����Ƃ���C�X���ւ̖{�p���̓K���̈Ӌ`�͍���high volume center�ł̏Ǘ�̒~�ςɂ�薾�炩�ɂ����ׂ��ł��낤�B
�� ���p����
1�j Gagner M, Pomp A. Laparoscopic pylorus-preserving pancreatoduodenectomy. SurgEndosc 1994�G8�F408-410.
2�j Mabrut JY, Fernandez-Cruz L, Azagra JS,et al. Laparoscopic pancreatic resection�Fresults of a multicenter European study of 127 patients. Surgery 2005�G137�F597-605.
3�j Kooby DA, Gillespie T, Bentrem D, et al. Left-sided pancreatectomy�Fa multicenter comparison of laparoscopic and open approaches. Ann Surg. 2008�G248�F438-446.
4�j Gagner M, Palermo M. Laparoscopic Whipple procedure�Freview of the literature. J Hepatobiliary Pancreat Surg 2009�G16�F726-730.
5�j Ammori BJ, Ayiomamitis GD. Laparoscopic pancreaticoduodenectomy and distal pancreatectomy�Fa UK experience and a systematic review of the literature. Surg Endosc 2011�G25�F2084-2099.
6�j Velanovich V. Case-control comparison of laparoscopic versus open distal pancreatectomy. J Gastrointest Surg 2006�G10�F95-98.
7�j Baker MS, Bentrem DJ, Ujiki MB, et al. A prospective single institution comparison of peri-operative outcomes for laparoscopic and open distal pancreatectomy. Surgery 2009�G146�F635-645.
8�j Waters JA, Canal DF, Wiebke EA, et al. Robotic distal pancreatectomy�Fcost effective�H Surgery 2010�G148�F814-823.
9�j Narula VK, Mikami DJ, Melvin WS. Robotic and laparoscopic pancreaticoduodenectomy�Fa hybrid approach. Pancreas 2010�G39�F160-164.
10�j Kendrick ML, Cusati D. Total laparoscopic pancreaticoduodenectomy�Ffeasibility and outcome in an early experience. Arch Surg 2010�G145�F19-23.
11�j Kooby DA, Hawkins WG, Schmidt CM, et al. A multicenter analysis of distal pancreatectomy for adenocarcinoma�Fis laparoscopic resection appropriate �H J Am Coll Surg 2010�G210�F779-785, 786-787.
12�j Dulucq JL, Wintringer P, Mahajna A. Laparoscopic pancreaticoduodenectomy for benign and malignant diseases. SurgEndosc 2006�G20�F1045-1050.
13�j Palanivelu C, Rajan PS, Rangarajan M, et al. Evolution in techniques of laparoscopic pancreaticoduodenectomy�Fa decade long experience from a tertiary center. J Hepatobiliary Pancreat Surg 2009�G16�F731-740.
14�j Palanivelu C, Jani K, Senthilnathan P, et al. Laparoscopic pancreaticoduodenectomy�Ftechnique and outcomes. J Am Coll Surg 2007�G205�F222-230.
15�j Pugliese R, Scandroglio I, Sansonna F, et al. Laparoscopic pancreaticoduodenectomy�Fa retrospective review of 19 cases. Surg Laparosc Endosc Percutan Tech 2008�G18�F13-18.
16�j Röthlin MA, Schöb O, Weber M. Laparoscopic gastro- and hepaticojejunostomy for palliation of pancreatic cancer�Fa case controlled study. Surg Endosc 1999�G13�F1065-1069.
CQ 2-8�@�X���ł͎�p�ᐔ�̑����{�݂Ŏ��Â���̂��悢���H
| ����
|
�X���\��w���؏��Ȃ��X���ɑ���O�Ȑ؏��p�ł́C��p�Ǘᐔ�����ȏ゠�����̂���{�݂ł͍����ǂ����Ȃ��X��������C�����ǔ�����̊Ǘ����D��Ă���i�O���[�hB�j�B |
|---|
�� �G�r�f���X
���x�ȋZ�p�ƗD�ꂽ���p���Ǘ���v���錌�Ǎ����؏����X�؏��p�ɂ����āC�V�X�e�}�e�B�b�N�E���r���[���s��ꂽ 1�j�i���x��Ⅰ�j�B1995�`2009 �N��14 �N�Ԃɕ��ꂽ28 �_������̃T���v������10 �ȏ��1,458 �Ǘ�ɂ����āC��p�֘A���S���̒����l��4���i0�`17���j�C�������Ԓ����l�imedian survival time�GMST�j�͖喬�����؏���ł�13 �J���C�喬�E���������؏���ł�18 �J���ł������BHigh volume center�iHVC�j16 �{�݂ɂ����錌�Ǎ����؏���MST ��15 �J���ŁC�e�{�݂ɂ����錌�Ǎ����؏���Ȃ��ꍇ�Ƃ̗L�Ӎ��͂Ȃ��CHVC �ł�����e�����Ƃ��Ă���B�������C62���̘_���Ŗ喬�ǐ��͎�p�̋֊��Ƃ���C71���̘_���œ����Z���͎�p�̋֊��Ƃ���Ă���B�܂��C����n��ɂ������K�͂ȑS�������̃f�[�^�x�[�X�Ɋ�Â������Ȃ���Ă���B�č��ł́C�X�؏��p��̍݉@����1998 �N����2003 �N�̊Ԃ�7.8������4.6���ւƗL�ӂȌ�����F�߂Ă��� 2�j�i���x��Ⅳa�j�BLow volume center�iLVC�j�i�N4��ȉ��j�Cmedium volume center�iMVC�j�i�N��5�`18 ��j�CHVC�i19 ��ȏ�j�ł̎��S���́CHVC ��1 �Ƃ����Ƃ��ɁC�I�b�Y�䂪MVC ��2.1�CLVC ��3.3 �ł������B6 �N�Ԃ�HVC �Ŏ�p���ꂽ�Ǘ�̊�����30������39���ɗL�ӂɑ������Ă����B�܂��C�č��ŁCNationwide Inpatient Sample�iNIS�j�ɓo�^����C�X�؏��p��̍݉@���ɉe�����郊�X�N���q�͉���E�j���E���������늳�E�؏��Ǘᐔ�ł����� 3�j�i���x��Ⅳa�j�B�݉@���͉���ɂ�葝�����邪�C�X�؏���p�����̑����{�݂Ə��Ȃ��{�݂Ŕ�ׂ��PD 4.78 �{, DP 3.84 �{, TP 2.6 �{�̍����������B���l�ɐ؏��Ǘᐔ�����Ȃ����Ƃ͗L�ӂȍ݉@���̃��X�N�ɂȂ��Ă��� 4�j�i���x��Ⅳa�j�B�N��C�����ǁC���C�X�؏��p���C�؏��Ǘᐔ����Ȃ�X�R�A�ɂ�����LVC ��5 �_�CMVC ��2 �_�CHVC ��0 �_�Ƃ���C�X�R�A�̍��v�_��5 �_�ȉ��ł���Η\���݉@���S����2.0���C6�`9 �_�̏ꍇ��6.2���C10 �_�ȏ�̏ꍇ��13.9���Ə㏸����B�܂��C�C�^���A�ł́C�p�㎀�S���̃n�U�[�h���LVC ��1�CMVC ��0.601�CHVC ��0.448�Cvery high volume center ��0.189 �ŁC�p��݉@������very high volume center �ŗL�ӂɒZ���C�Ǘ�W�̕��j�͓K�ł���Ƃ��Ă��� 5�j�i���x��Ⅳa�j�B
HVC �̒�`�ɂ��ẮC�G�r�f���X�ƂȂ�_���̂Ȃ��ł��\3 �̂��Ƃ��C���������B
�č���HVC �Ƃ���œK�ȃJ�b�g�I�t�l�͔N��19 ��ȏ�ł��������C�{�݂��Ƃ̔N�Ԑ؏����͏p�㎀�S���̂����2���ȉ��������������Ȃ��Ƃ��Ă��� 6�j�i���x��Ⅲ�j�B
�؏��Ǘᐔ�C��Î����C���G�ȏ����ǐf�Âɂ�����i���]���C��ʊO�ȃ��W�f���g�C��������ȃt�F���[�CIVR�iinterventional radiology�j�̂�������C�P�Ƃł͎��p�����S�Ƒ��ւ��Ȃ����C6 �̈�Î������ׂĂ������istrong support�j�{�݂ł́C�L�ӂɎ��p�����S�����Ȃ������iHR�F0.32�j 7�j�i���x��Ⅳb�j�B
| ���� | �G�r�f���X ���x�� |
�Ώۊ���/Database | LVC | MVC | HVC |
|---|---|---|---|---|---|
| 1�j | �T | �V�X�e�}�e�B�b�N�E���r���[ |
19�ȉ� |
20�ȏ� |
|
| 2�j | �Wa | NIS |
4�ȉ� |
5�`18 |
19�ȏ� |
| 3�j | �Wa | NIS |
��3�C3�`5�C6�`11�C12�`23�C24�`35�C |
||
| 4�j | �Wa | NIS |
8�ȉ� |
9�`32 |
33�ȏ� |
| 5�j | �Wa | �C�^���A�n��DB |
5�ȉ� |
6�`13 |
14�`51 |
| 100�ȏ��very high volume | |||||
| 6�j | Ⅲ | NIS |
Cut off�����肷�郂�f���쐬 |
||
| 7�j | �Wb | LeapfrogGroup database, |
10�ȉ� |
11�ȏ� |
|
| 8�j | �Wa | NCDB |
���Ґ����������Ȃ�悤5���� |
||
| 9�j | �Wa | �m���E�F�[DB |
6.7�ȉ� |
6.7�`15 |
18.8 |
| 10�j | �Wa | NSQIP |
���Ґ����������Ȃ�悤5���� |
||
| 11�j | Ⅲ | �t�����_���o�^ |
����1/3 |
���1/3 |
|
| 12�j | �Wa | NCDB |
���Ґ����������Ȃ�悤4���� |
||
| 13�j | �Wa | SEER |
2.3�ȉ� |
2�`7.3 |
8.3�`135.5 |
| 14�j | �X | ���{�� |
���{�݂�HVC�ƒ�` |
||
| 15�j | �Wb | NIS�i�O�Ȉ�̌o�����j |
4�ȉ� |
5�ȏ� |
|
| 16�j | �Wb | ���{�݁i�O�Ȉ�̌o�����j |
49�ȉ� |
50�ȏ� |
|
| 17�j | �Wb | �J���t�H���j�A�މ@�f�[�^�x�[�X |
��6�C6�`10�C11�`20�C21�`30�C31�`50, |
||
| 18�j | �Wa | ���{�� |
���{�݂�HVC�ƒ�` |
||
| 19�j | �Wa | �J�i�_�n���DB |
��10 |
10�ȏ� |
|
| 20�j | �Wa | �e�L�T�XPUDF |
10�ȉ� |
11�ȏ� |
|
| 21�j | �Wa | �j���[���[�N�C�j���[�W���[�W�[�C |
���Ґ����������Ȃ�悤5���� |
||
| 22�j | �Wa | NIS, ARF |
��20 |
20�ȏ� |
|
�� �����ւ̒�
�����̏Ǘ�Ɋ�Â���HVC �ł̍����ǔ������C�����������ł̗D�ʐ���������Ă��邪�CHVC ���`����Ǘᐔ�͂���Ă���B�܂��C�Ǘᐔ�����ł͍���x���X�؏��p�����S�E�m���Ɏ{�s�ł���\�������ɂ͂Ȃ�Ȃ��B�ǂ̒n��ɏZ�ފ��҂��A�N�Z�X���悭�C�����f�f���x�E�Z�p�������C�����ǂ̏��Ȃ��W���I�Ȏ�p�Əp�㑁������̕⏕�Ö@���C���S�̂̈�ÃR�X�g���Ó��Ȉ�Ë����̐������߂���BNCD�iNational Clinical Database�j�C�n�悪��o�^�Ȃǂ̑�K�͑S�������f�[�^�x�[�X���킪���ɂ����Ă��[��������B�X���o�^�̃f�[�^�͒��N�̒~�ς����邪�C��������HVC �ɂ�����f�Ð��т̐ςݏd�˂ł�����B�X���o�^�́C����NCD �ɑg�ݍ��܂�邱�Ƃ��m�肵�Ă���C�킪�����X���ɑ���f�Ñ̐��̌���c���E���P�ɑ傫����^������̂Ǝv����B
�� ���p����
1�j Chua TC, Saxena A. Extended pancreaticoduodenectomy with vascular resection for pancreatic cancer�Fa systematic review. J Gastrointest Surg 2010�G14�F1442-1452.
2�j McPhee JT, Hill JS, Whalen GF, et al. Perioperative mortality for pancreatectomy�Fa national perspective. Perioperative mortality for pancreatectomy�Fa national perspective. Ann Surg 2007�G246�F246-253.
3�j Teh SH, Diggs BS, Deveney CW, et al. Patient and hospital characteristics on the variance of perioperative outcomes for pancreatic resection in the United States�Fa plea for outcome-based and not volume-based referral guidelines. Arch Surg 2009�G144�F713-721.
4�j Hill JS, Zhou Z, Simons JP, et al. A simple risk score to predict in-hospital mortality after pancreatic resection for cancer. Ann Surg Oncol 2010�G17�F1802-1807.
5�j Balzano G, Zerbi A, Capretti G, et al. Effect of hospital volume on outcome of pancreaticoduodenectomy in Italy. Br J Surg 2008�G95�F357-362.
6�j Meguid RA, Ahuja N, Chang DC. What constitutes a �ghigh-volume�h hospital for pancreatic resection�H J Am Coll Surg 2008�G206�F622. e1-9.
7�j Joseph B, Morton JM, Hernandez-Boussard T, et al. Relationship between hospital volume, system clinical resources, and mortality in pancreatic resection. J Am Coll Surg 2009�G208�F520-527.
8�j Bilimoria KY, Talamonti MS, Sener SF, et al. Effect of hospital volume on margin status after pancreaticoduodenectomy for cancer. J Am Coll Surg 2008�G207�F510-519.
9�j Westgaard A, Larønningen S, Mellem C, et al. Are survival predictions reliable�H Hospital volume versus standardisation of histopathologic reporting for accuracy of survival estimates after pancreatoduodenectomy for adenocarcinoma. Eur J Cancer 2009�G45�F2850-2859.
10�j Bilimoria KY, Talamonti MS, Wayne JD, et al. Effect of hospital type and volume on lymph node evaluation for gastric and pancreatic cancer. Arch Surg 2008�G143�F671-678�Gdiscussion 678.
11�j Yang R, Cheung MC, Byrne MM, et al. Survival effects of adjuvant chemoradiotherapy after resection for pancreatic carcinoma. Arch Surg 2010�G145�F49-56.
12�j Bilimoria KY, Bentrem DJ, Ko CY, et al. Multimodality therapy for pancreatic cancer in the U.S.�Futilization, outcomes, and the effect of hospital volume. Cancer 2007�G110�F1227-1234.
13�j Birkmeyer JD, Sun Y, Wong SL, et al. Hospital volume and late survival after cancer surgery. Ann Surg 2007�G245�F777-783.
14�j Michalski CW, Kleeff J, Bachmann J, et al. Second-look operation for unresectable pancreatic ductal adenocarcinoma at a high-volume center. Ann Surg Oncol 2008�G15�F186-192.
15�j Eppsteiner RW, Csikesz NG, McPhee JT, et al. Surgeon volume impacts hospital mortality for pancreatic resection. Ann Surg 2009�G249�F635-640.
16�j Schmidt CM, Turrini O, Parikh P, et al. Effect of hospital volume, surgeon experience, and surgeon volume on patient outcomes after pancreaticoduodenectomy�Fa single-institution experience. Arch Surg 2010�G145�F634-640.
17�j Gasper WJ, Glidden DV, Jin C, et al. Has recognition of the relationship between mortality rates and hospital volume for major cancer surgery in California made a difference�H�FA follow-up analysis of another decade. Ann Surg 2009�G250�F472-483.
18�j Mukherjee S, Kocher HM, Hutchins RR, et al. Impact of hospital volume on outcomes for pancreaticoduodenectomy�Fa single UK HPB centre experience. Eur J Surg Oncol 2009�G35�F734-738.
19�j Simunovic M, Urbach D, Major D, et al. Assessing the volume-outcome hypothesis and region-level quality improvement interventions�Fpancreas cancer surgery in two Canadian Provinces. Ann Surg Oncol 2010�G17�F2537-2544.
20�j Riall TS, Eschbach KA, Townsend CM Jr, et al. Trends and disparities in regionalization of pancreatic resection. J Gastrointest Surg 2007�G11�F1242-1251�Gdiscussion 1251-1252.
21�j Stitzenberg KB, Sigurdson ER, Egleston BL, et al. Centralization of cancer surgery�Fimplications for patient access to optimal care. J Clin Oncol 2009�G27�F4671-4678.
22�j Chang DC, Zhang Y, Mukherjee D, et al. Variations in referral patterns to high-volume centers for pancreatic cancer. J Am Coll Surg 2009�G209�F720-726.
CQ 2-9�@Borderline resectable �X���̎��ÁF�킪���ɂ�����O�ȓI�؏��̈Ӌ`�́H
| ����
|
Borderline resectable �X���ɑ��ĕ⏕�i�p�O�j���Â��s�����ƂŁC�O�ȓI�؏��̎��Ð��т����P���邩�ɂ��Ă͍���̗Տ������⌤���Ŗ��炩�ɂ����ׂ��ł���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
Borderline resectable �Ǘ�Ƃ́C�Z�p�I�ɊO�ȓI�؏�������Ȃ��Ƃɉ����C�X���̋Ǐ��̐Z���ɂ��O�ȓI�؏����{�s���Ă������Ɋ�����c���iR1,2�j�C��p�ɂ�萶�����Ԃ��������Ȃ��\����������̂ƍl������ 1, 2�j�i���x��Ⅵ�j�B���������āCborderline resectable�Ǘ�ɑ����p�P�Ǝ��Â���������邩�ۂ��͍���̉ۑ�ł���B����ɁC�p�O���Âɂ��down-staging �ɂ��R0 �؏��������シ�邱�ƂŁC���Ð��т����P����\��������B
Borderline resectable �Ǘ�ɑ��C�p�O���w���ː��Ö@����Q�̂ق����Ȃ��Q���R0 ���������Łi���� 59��vs �Ȃ� 11���Cp �� 0.0001�j�C�����p�ߓ]�ډA�������p�O���w���ː��Ö@����Q�̂ق��������i���� 73��vs �Ȃ� 14���Cp��0.0001�j�C��ᇂ��L�ӂɏ����������i���� 2.5cm vs �Ȃ� 3.5cm�Cp��0.009�j�B�܂��C�p�O���w���ː��Ö@�{�s�Q�Ń����p�ߓ]�ڗz�������L�ӂɒႩ���� 3�j�i���x��Ⅳb�j�BBorderline resectable �X����喬�n�Ö��ǁC���̓����܂��͏㒰�Ԗ������ւ̗אڂƂ����ꍇ�C���w���ː��Ö@���s�����Q�͍s��Ȃ������Q�Ɣ�r���Ď�p���Ԃ�1 ���Ԓ����ip �� 0.01�j�C���@���Ԃ�5 �������Ȃ������ip��0.02�j�C�A���Cmorbidity�Cmortality �ɗL�Ӎ��͂Ȃ������B�����2 �N��disease-free survival ��B���ł����̂�R0 �؏�������ꂽ�Ǘ�ł����� 4�j�i���x��Ⅳb�j�BBorderline resectable �Ǘ�ɑ��C�J�y�V�^�r���ƕ��ː��ɂ��p�O���w���ː��Ö@���s������ɐ؏��ł����Ǘ�̂����C75����R0 ��p���\�ł����� 5�j�i���x��Ⅳb�j�B�������ώ@�����ŏp�O�Ö@�ɂ��؏��ł����Ǘ��67����R0 �؏��ł���C�������Ԓ����l��23.3 �J���i��؏�15.5 �J���j�ł���C���{�݂�initially resectable �Ǘ��R0 ���E�������Ɠ����ł����� 6�j�i���x��Ⅳa�j�B�p�O���w���ː��Ö@��ɐ؏����\�ł�����borderline resectable �Ǘ��94����margin-negative �ƂȂ�C���̗\��K����q�͏p�O���w���ː��Ö@�ɂ��g�D�w�I���ʂ�Ⅱb �ȏ�ł��邱�ƁCCA19-9 ��50���ȏ�̌�����2 ���ڂ����o���ꂽ���Ƃ���C���w���ː��Ö@��̎�p���Ì��ʂ�����Ǘ��I���ł��邱�Ƃ��������ꂽ 7�j�i���x��Ⅳa�j�B�܂�borderline resectable �X��13 ��̏�����̌����ł͂��邪�C�p�O���Âɂ��84.6���̏Ǘ��R0 �؏����\�ł���C�g�D�w�I�Ɏ�ᇂ̐��ۉ���60���ȏ�F�߂�ꂽ�Ǘ�͐������Ԃ��������� 8�j�i���x��Ⅳb�j�B�Ĕ��`�������������͏��Ȃ����C�p�O���w���ː��Ö@�͋Ǐ��̍Ĕ���}�����Ă��� 9�j�i���x��Ⅳb�j�BBorderline resectable �X���ɑ���p�O���w�Ö@�P�Ƃł̕͏��Ȃ����C�p�O���w�Ö@�P�Ƃł�borderline resectable �Ǘ�̗\�オ���P����\��������BBorderline resectable �Ǘ�33 �ᒆ13 ��Ɏ�p���{�s���CR0 ����69���C�������Ԓ����l��22�J���ł����� 10�j�i���x��Ⅳa�j�B
�喬�E�㒰�Ԗ��Ö��Z���Ǘ�109 ��̂���74 ��ɏp�O���w���ː��Ö@���{�s�����Ƃ���C�S�����ɋ��Ă���Ǘ�ł͏p�O���w���ː��Ö@�ɂ��\�オ���P���Ȃ��������C�Б����̋���Ǘ�ł͏p�O���w���ː��Ö@�ɂ�萶�����Ԃ͉��P�����iOS �����l�FCRT ���� 26 �J�� vs �Ȃ� 10 �J���Cp��0.0001�j 3�j�i���x��Ⅳb�j�B
���o�����Z�����X���́wNCCN �K�C�h���C���x�i2012 �N�Łj�ł͐؏��s�\�X���Ƃ��Ĉ����邪�C���o�������͂ւ̊��Z�����X�̕����ł͕��o�������������؏������X�����؏��p���s���邱�Ƃ�����B����c�̂Ȃ�R0 �؏�����37�`91��11-14�j�C�p��̐������Ԓ����l��10�`21 �J�� 11-17�j�ł����� 14�j�i���x��Ⅳa�j 11-13, 15-17�j�i���x��Ⅵ�j�B����ɏp�O���w���ː��Ö@�{�s��ɕ��o���������؏����X�̔����؏����{�s���邱�Ƃ�R0 ����91���C�������Ԓ����l��26 �J���Ƃ��������� 18�j�i���x��Ⅵ�j�C���o���������؏����邱�ƂŋǏ�������ʂ�������Ǘ�����邱�Ƃ���C���o���������؏��ɂĐ؏��\���X����borderline resectable �X���Ƃ݂Ȃ����Ƃ��\���͂���Ȃ�Ǘ�̒~�ςƌ������K�v�ł���B
�� �����ւ̒�
�L���ȏp�O���Â̊J���ɂ��p��̕⏕�Ö@���܂߂��W�w�I���Â��{�s���邱�ƂŁCborderline resectable �X���̗\��͉��P����\��������B����ɏp�O���Ì�ɐ؏�����Ɛ����\�㉄�����ʂ����҂ł���Ǘ��I�ʂ��邱�ƂŁCborderline resectable �X���̐V���Ȏ��Õ��j���m���ł���\��������B
�� ���p����
1�j Adams RB, Allen PJ. Surgical treatment of resectable and borderline resectable pancreatic cancer�Fexpert consensus statement by Evans et al. Ann Surg Oncol 2009�G16�F1745-1750.
2�j Berlin J, Hoffman JP, Regine WF. Editorial�FCombined modality treatment of resectable and borderline resectable pancreas cancer�Fexpert consensus conference. Ann Surg Oncol 2009�G16�F1757-1759.
3�j Chun YS, Milestone BN, Watson JC, et al. Defining venous involvement in borderline resectable pancreatic cancer. Ann Surg Oncol 2010�G17�F2832-2838.
4�j Massucco P, Capussotti L, Magnino A, et al. Pancreatic resections after chemoradiotherapy for locally advanced ductal adenocarcinoma�Fanalysis of perioperative outcome and survival. Ann Surg Oncol 2006�G13�F1201-1208.
5�j Stokes JB, Nolan NJ, Stelow EB, et al. Preoperative capecitabine and concurrent radiation for borderline resectable pancreatic cancer. Ann Surg Oncol 2011�G18�F619-627.
6�j McClaine RJ, Lowy AM, Sussman JJ, et al. Neoadjuvant therapy may lead to successful surgical resection and improved survival in patients with borderline resectable pancreatic cancer. HPB�iOxford�j2010�G12�F73-79.
7�j Katz MH, Pisters PW, Evans DB, et al. Borderline resectable pancreatic cancer�Fthe importance of this emerging stage of disease. J Am Coll Surg 2008�G206�F833-846�Gdiscussion 846-848.
8�j Brown KM, Siripurapu V, Davidson M, et al. Chemoradiation followed by chemotherapy before resection for borderline pancreatic adenocarcinoma. Am J Surg 2008�G195�F318-321.
9�j Greer SE, Pipas JM, Sutton JE, et al. Effect of neoadjuvant therapy on local recurrence after resection of pancreatic adenocarcinoma. J Am Coll Surg 2008�G206�F451-457.
10�j Sahora K, Kuehrer I, Eisenhut A, et al. NeoGemOx�FGemcitabine and oxaliplatin as neoadjuvant treatment for locally advanced, nonmetastasized pancreatic cancer. Surgery 2011�G149�F311-320.
11�j Hishinuma S, Ogata Y, Tomikawa M, et al. Stomach-preserving distal pancreatectomy with combined resection of the celiac artery�Fradical procedure for locally advanced cancer of the pancreatic body. J Gastrointest Surg 2007�G11�F743-749.
12�j Hirano S, Kondo S, Hara T, et al. Distal pancreatectomy with en bloc celiac axis resection for locally advanced pancreatic body cancer�Flong-term results. Ann Surg 2007�G246�F46-51.
13�j Sperti C, Berselli M, Pedrazzoli S. Distal pancreatectomy for body-tail pancreatic cancer�Fis there a role for celiac axis resection�H Pancreatology 2010�G10�F491-498.
14�j Okada K, Kawai M, Tani M, et al. Surgical strategy for patients with pancreatic body/tail carcinoma�Fwho should undergo distal pancreatectomy with en-bloc celiac axis resection�H Surgery 2013�G153�F365-372.
15�j Miyakawa S, Horiguchi A, Hanai T, et al. Monitoring hepatic venous hemoglobin oxygen saturation during Appleby operation for pancreatic cancer. Hepatogastroenterology 2002�G49�F817-821.
16�j Shimada K, Sakamoto Y, Sano T, et al. Prognostic factors after distal pancreatectomy with extended lymphadenectomy for invasive pancreatic adenocarcinoma of the body and tail. Surgery 2006�G139�F288-295.
17�j Wu X, Tao R, Lei R, et al. Distal pancreatectomy combined with celiac axis resection in treatment of carcinoma of the body/tail of the pancreas�Fa single-center experience. Ann Surg Oncol 2010�G17�F1359-1366.
18�j Baumgartner JM, Krasinskas A, Daouadi M, et al. Distal pancreatectomy with en bloc celiac axis resection for locally advanced pancreatic adenocarcinoma following neoadjuvant therapy. J Gastrointest Surg 2012�G16�F1152-1159.
3 �⏕�Ö@
CQ 3-1�@�X���ɑ���p�O���Ái①���w���ː��Ö@�C②���w�Ö@�j�͐�������邩�H
| ����
|
�p�O���Ái①���w���ː��Ö@�C②���w�Ö@�j�̗L�p�����x������_���������X���ɂ���B���������ꂪ�������u���т����コ���邩�ۂ��ɂ��ẮC����̗Տ������⌤���̒~�ςɂ���Ė��炩�ɂ����ׂ��ł���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�X���ɑ����p�P�Ǝ��Â̐��т��ɂ߂ĕs�ǂł��邱�Ƃ���C�p�O�ɉ��w���ː��Ö@�܂��͉��w�Ö@���{�s���C���̌���X����؏�������@������Ă���B�摜��؏��\�ƍl������Ǘ�ɂ����āC�p�O���Âɂ���Ċ��̐i�s�x��������idown-staging�j���Ƃ��ł���C�؏������グ�C���זE���p���Ɉ�c�E�T�z����@���������������B����C�p�O���Ò��ɉ��u�]�ڂ�f�f�������ꍇ��C�����ÂɑS���t�����Ȃ��ꍇ�ɂ́C�J���p������ł���\��������B
����܂��X���ɑ���p�O���w���ː��Ö@�̕�1980 �N���Pilpich ��Ishikawa �Ɏn�܂�ŋ߂ł͋}�����Ă��� 1�j�i���x��Ⅲ�j�B�������O���������_������r�����Œ����������Ȃǂ��r�E���������̂͂Ȃ��B�p�O���w�Ö@�Ɋւ���\���Ȓm���͒~�ς���Ă��Ȃ��B
- �p�O���w���ː��Ö@
�p�O���w���ː��Ö@����X���؏����s���Ă��p�㍇���ǂ̕p�x�͑������Ȃ��i���S���̊m�F�j�Ƃ����͑������C������������_������r�����̌��ʂł͂Ȃ� 2, 3�j�i���x��Ⅳa�j�BSpitz ����X���؏���̍����ǔ����p�x�͒Ⴍ�Ȃ��̂ŁC��p��s��̖�1/4 ���p�㉻�w���ː��Ö@�̋@����킵���i�p�O���Â̂ق����p�㎡�Â������p���Â̊������������j�ƕ��Ă��� 4�j�i���x��Ⅳa�j�B
���w���ː��Ö@�ɂ��down-staging ������CHoffman ��͖�1/3 �̏Ǘ�Ɏ�ᇏk�����ʂ�F�� 2�j�i���x��Ⅳa�j�CEvans��͖�40���̏ǗႪ�g�D�w��50���ȏ�̎��Ŋ��זE�Œu������Ă����ƕ��Ă��� 3�j�i���x��Ⅳa�j�B�p�O���w���ː��Ö@�ɂ���Đ؏��s�\�X������؏��\�ɂȂ����Ǘ�ł�R0 �؏�����90���ƍ����ł������Ƃ�����݂��� 5�j�i���x��Ⅳb�j�B
Borderine resectable ��ɂ�����Sa Cunha ��͏p�O���w���ː��Ö@�ɂ���Ė�20���̏Ǘ�œ����Z���i�g�D�w��j���������C�؏��������ƕ��Ă��� 6�j�i���x��Ⅳa�j�BStokes ��͏p�O���Âɂ���Đ؏��\�ƂȂ�Ύ�p�P�Ƃ̐؏��\��Ɠ����̐��т� 7�j�i���x��Ⅳb�j�BGreer ��͏p�O���×�ł͋Ǐ��Ĕ���4���ŏp�O�����×��44���ɔ�גᗦ�ł������ƕ��Ă��� 8�j�i���x��Ⅳb�j�BGillen �炪�W�v����111 �̕ɂ����郁�^�A�i���V�X�ł́Cborderline resectable ��ɂ�����p�O���Â̗L�p���������ꂽ���C����Ȃ錟���K�v�ł��� 1�j�i���x��Ⅲ�j�B
Snady ��͉��w���ː��Ö@���s����68 �Ǘ�i�S��T3�C����20 �Ⴊ���̌�ɐ؏��\�j�̐������Ԓ����l��24 �J���ŁC���̂����؏�20 ��̐������Ԓ����l��32 �J���ł������ƕ����B����ɑ��Đ؏��p���s����91 ��iTl�`2��73���C63 �Ⴊ�p�㕹�p���Áj�̐������Ԓ����l��14 �J���ɉ߂����C�p�O���w���ː��Ö@�̈Ӌ`��]�����Ă��� 9�j�i���x��Ⅳb�j�B�܂��CStessin ��̃f�[�^�x�[�X��p����������̉�͂ɂ��C�p�O�Ǝ˂��؏��\��̐��������P�Ɋ�^���Ă��� 10�j�i���x��Ⅳb�j�B���Ȃ݂ɁC�ŋ߂̐؏��\��ɂ����鉻�w���ː��Ö@��؏����5 �N�������ɂ��āCEvans�� 11�j��36���CTurrini �� 12�j��41���COhigashi �� 13�j��53���ƕ��Ă��� 11-13�j�i���x��Ⅳa�j�B
�Q���V�^�r�����_�����X�����Âɂ�������I���ƂȂ�C�Q���V�^�r�����_�����p�̕��������Cfull-dose �ł̓��^ 13-15�j�C���邢�̓h�Z�^�L�Z��* 12�j��J�y�V�^�r��* 7�j���̎g�p�����݂��Ă��邪�C�����̂��ׂĂ������_������r�����ł͂Ȃ� 7�j�i���x��Ⅳb�j 12-15�j�i���x��Ⅳa�j�B
��ʂɉ��w���ː��Ö@��̐؏���ł́C�Ǐ��Ĕ��͌����������ʁC���u�Ĕ��C���Ɋ̓]�ڍĔ������� 4, 12, 16�j�i���x��Ⅳa�j 8, 17�j�i���x��Ⅳb�j�BOhigashi ��́C�p�O���w���ː��Ö@��̐؏���Ɋ̓]�ڗ\�h�̂��߂̟̊��w�Ö@���p��ɒlj����C�������̉��P��F�߂� 13�j�i���x��Ⅳa�j�B
- �p�O���w�Ö@
Palmer ��͐؏��\�Əp�O�f�f�����X���ɑ��C�p�O���w�Ö@�̔�r�������{�s�����B����̓Q���V�^�r�����_���Q�i24 ��j�ƃQ���V�^�r�����_���{�V�X�v���`��* �Q�i26 ��j�Ԃł̃����_������r�����ł���C�؏����͊e�X38��vs 70���C��؏�����܂ޑS���1 �N��������42��vs 62���Ɓi�L�Ӎ�����Ȃ��j�C���������҂̐��т��D��Ă��� 18�j�i���x��Ⅱ�j�B����ɃQ���V�^�r�����_���ɃV�X�v���`��* �p������ 19�j��C���w���ː��Ö@�ɐ旧�������w�Ö@ 20, 21�j�≻�w���ː��Ö@��̏p�O���� 22�j�Ƃ��Ă̎��g�݂��s���Ă��邪�C������������_������r�����ł͂Ȃ� 19-21�j�i���x��Ⅳa�j 22�j�i���x��Ⅳb�j�B
- �킪���ɂ�����p�O���ÂɊւ��郉���_������r����
�p�O���ÂƂ��Ă�S-1 ���p���ː��Ö@�ƃQ���V�^�r�����_���{S-1 ���p�Ö@�̃����_������r�����iJASPAC-04�j��C�؏��{�⏕�Ö@��ɑ���p�O���ÂƂ��ẴQ���V�^�r�����_���{S-1 ���p�Ö@�̗L�����E���S���Ɋւ��郉���_������r�����iPrep-02/JSAP-05�j�Ȃǂ�RCT ���킪���ōs���悤�Ƃ��Ă���C���̌��ʂ��҂����B
* �ی������ڂ̌����E����
�� �����ւ̒�
����C�����_������r�����̒~�ςȂǂɂ���āC�X���ɑ���p�O���w���ː��Ö@��p�O���w�Ö@���������ԁi���j�̌���Ɋ�^���邩�ۂ��𖾂炩�ɂ��Ă����K�v������B�p�O���w���ː��Ö@�ł́C�̓]�ڗ\�h�d�v�ۑ�ł���B
�� ���p����
1�j Gillen S, Schuster T, Meyer Zum Büschenfelde C, et al. Preoperative/neoadjuvant therapy in pancreatic cancer�Fa systematic review and meta-analysis of response and resection percentages. PLoS Med 2010�G7�Fe1000267
2�j Hoffman JP, Weese JL, Solin LJ, et al. A pilot study of preoperative chemoradiation for patients with localized adenocarcinoma of the pancreas. Am J Surg. 1995�G169�F71-77�Gdiscussion 77-78.
3�j Evans DB, Rich TA, Byrd DR, et al. Preoperative chemoradiation and pancreaticoduodenectomy for adenocarcinoma of the pancreas. Arch Surg 1992�G127�F1335-1339.
4�j Spitz FR, Abbruzzese JL, Lee JE, et al. Preoperative and postoperative chemoradiation strategies in patients treated with pancreaticoduodenectomy for adenocarcinoma of the pancreas. J Clin Oncol 1997�G15�F928-937.
5�j Golcher H, Brunner T, Grabenbauer G, et al. Preoperative chemoradiation in adenocarcinoma of the pancreas. A single centre experience advocating a new treatment strategy. Eur J Surg Oncol 2008�G34�F756-764.
6�j Sa Cunha A, Rault A, Laurent C, et al. Surgical resection after radiochemotherapy in patients with unresectable adenocarcinoma of the pancreas. J Am Coll Surg 2005�G201�F359-365.
7�j Stokes JB, Nolan NJ, Stelow EB, et al. Preoperative capecitabine and concurrent radiation for borderline resectable pancreatic cancer. Ann Surg Oncol 2011�G18�F619-627.
8�j Greer SE, Pipas JM, Sutton JE, et al. Effect of neoadjuvant therapy on local recurrence after resection of pancreatic adenocarcinoma. J Am Coll Surg 2008�G206�F451-457.
9�j Snady H, Bruckner H, Cooperman A, et al. Survival advantage of combined chemoradiotherapy compared with resection as the initial treatment of patients with regional pancreatic carcinoma. An outcomes trial. Cancer 2000�G89�F314-327.
10�j Stessin AM, Meyer JE, Sherr DL. Neoadjuvant radiation is associated with improved survival in patients with resectable pancreatic cancer�Fan analysis of data from the surveillance, epidemiology, and end results�iSEER�jregistry. Int J Radiat Oncol Biol Phys 2008�G72�F1128-1133.
11�j Evans DB, Varadhachary GR, Crane CH, et al. Preoperative gemcitabine-based chemoradiation for patients with resectable adenocarcinoma of the pancreatic head. J Clin Oncol 2008�G26�F3496-3502.
12�j Turrini O, Ychou M, Moureau-Zabotto L, et al. Neoadjuvant docetaxel-based chemoradiation for resectable adenocarcinoma of the pancreas�FNew neoadjuvant regimen was safe and provided an interesting pathologic response. Eur J Surg Oncol 2010�G36�F987-992.
13�j Ohigashi H, Ishikawa O, Eguchi H, et al. Feasibility and efficacy of combination therapy with preoperative full-dose gemcitabine, concurrent three-dimensional conformal radiation, surgery, and postoperative liver perfusion chemotherapy for T3-pancreatic cancer. Ann Surg 2009�G250�F88-95.
14�j Talamonti MS, Small W Jr, Mulcahy MF, et al. A multi-institutional Phase Ⅱ�Gtrial of preoperative full-dose gemcitabine and concurrent radiation for patients with potentially resectable pancreatic carcinoma. Ann Surg Oncol 2006�G13�F150-158.
15�j Small W Jr, Berlin J, Freedman GM, et al. Full-dose gemcitabine with concurrent radiation therapy in patients with nonmetastatic pancreatic cancer�Fa multicenter Phase Ⅱ�Gtrial. J Clin Oncol 2008�G26�F942-947.
16�j Le Scodan R, Mornex F, Girard N, et al. Preoperative chemoradiation in potentially resectable pancreatic adenocarcinoma�Ffeasibility, treatment effect evaluation and prognostic factors, analysis of the SFRO-FFCD 9704 trial and literature review. Ann Oncol 2009�G20�F1387-1396.
17�j Ishikawa O, Ohigashi H, Imaoka S, et al. Is the long-term survival rate improved by preoperative irradiation prior to Whipple�fs procedure for adenocarcinoma of the pancreatic head �H Arch Surg 1994�G129�F1075-1080.
18�j Palmer DH, Stocken DD, Hewitt H, et al. A randomized phase 2 trial of neoadjuvant chemotherapy in resectable pancreatic cancer�Fgemcitabine alone versus gemcitabine combined with cisplatin. Ann Surg Oncol 2007�G14�F2088-2096.
19�j Heinrich S, Pestalozzi BC, Schäfer M, et al. Prospective phaseⅡtrial of neoadjuvant chemotherapy with gemcitabine and cisplatin for resectable adenocarcinoma of the pancreatic head. J Clin Oncol 2008�G26�F2526-2531.
20�j Marti JL, Hochster HS, Hiotis SP, et al. Phase�T/Ⅱtrial of induction chemotherapy followed by concurrent chemoradiotherapy and surgery for locoregionally advanced pancreatic cancer. Ann Surg Oncol 2008�G15�F3521-3531.
21�j Varadhachary GR, Wolff RA, Crane CH, et al. Preoperative gemcitabine and cisplatin followed by gemcitabine-based chemoradiation for resectable adenocarcinoma of the pancreatic head. J Clin Oncol 2008�G26�F3487-3495.
22�j Brown KM, Siripurapu V, Davidson M, et al. Chemoradiation followed by chemotherapy before resection for borderline pancreatic adenocarcinoma. Am J Surg 2008�G195�F318-321.
CQ 3-2�@�X���̏p�㉻�w���ː��Ö@�͐�������邩�H
| ����
|
�X���ɑ���p�����ː��Ö@�̗L�p���͖��炩�ł͂Ȃ��B���{�ōs��ꂽ�����_������r�����ł́C�p�����ː��Ö@�P�Ƃ̌��ʂ͔F�߂��Ȃ������i�O���[�hC2�j�B |
|---|
�� �G�r�f���X
�X���ɑ���⏕�Ö@�Ƃ��Ă̏p�����ː��Ö@�iintraoperative radiotherapy�GIORT�j�̗L�p���͖��炩�ł͂Ȃ��B�Ȃ��Ȃ�C�����_������r�����iRCT�j�܂��̓��^�A�i���V�X�ɂ����IORT �̗L�p���m�Ɏ������G�r�f���X���x���̍����_�����Ȃ�����ł���B
�X���⏕�Ö@�Ƃ��Ă�IORT �̗L�p���ɂ��ẮC�����J���Ȃ��������������ǁi�؉��ǁj�ɂ��RCT�Ō����� 1, 2�j�i���x��Ⅱ�j�C�X���؏����IORT �͑S�������ԁiOS�j����ыǏ�����ɉe�����y�ڂ��Ȃ������ƕ���Ă���B�]���\�ł�����144 ��̐؏��\�X������p�P�ƌQ�Ǝ�p�{IORT �Q��2 �Q�ɕ����Ĕ�r�����Ƃ���COS �Ɩ��Ĕ��������ԁiPFS�j�͗��Q�ԂɗL�Ӎ���F�߂Ȃ������B�܂�2 �N�Ǐ����䗦�́C���Q�ԂɗL�Ӎ���F�߂Ȃ��������CIORT �Q�ŗǍD�ȌX���ł������B�Ȃ��C���̎����ł͌��݂̕W�����Âł���p��⏕���w�Ö@�͕��p����Ă��Ȃ��B
���̑����X���ɑ���IORT �Ɋւ���� 3-14�j�i���x��Ⅳb�j�̑����͌������̌����ł���C�p�O�E�p��Ǝ˂��X�̕⏕���w�Ö@�����p����Ă���ȂǏ��������܂��܂ł���B
�����̑̕唼�ł́CIORT �ɂ���X���̐����������ʂ͎�����Ă��Ȃ��B����ɏڂ����݂�ƁC�⏕�Ö@�Ƃ��Ă�IORT �̗L�p���͔F�߂��Ȃ������Ƃ���� 8, 11�j�i���x��Ⅳb�j�CIORT �ɂ�鐶���������ʂ͔F�߂��Ȃ����̂̋Ǐ��Ĕ��͌��������Ƃ���� 3, 10, 13, 14�j�i���x��Ⅳb�j�C�����ĕ⏕�Ö@�Ƃ��Ă�IORT �̌��ʂ��]������Ă��Ȃ��� 5-7, 12�j�i���x��Ⅳb�j�Ȃǂɕ����邱�Ƃ��ł���B
����CReni ��͋Ǐ��Ɍ��ǂ����ilocally limited disease�jStage Ⅰ�`Ⅱ�X���ɂ����āCIORT ��{�s�Q�̐������Ԓ����l13 �J���ɑ��āCIORT �Q��18.5 �J���Ɛ������Ԃ������������Ƃ���Ă��� 4�j�i���x��Ⅳb�j�B�������C����IORT ��{�s�Q�̐������Ԓ����l��13 �J���ƒZ������_�ɂ͂���肪����B����Ŕނ�́C�L�͈͂ɐi�W�����ilocally advanced disease�jStage Ⅲ�`Ⅳ�X���̐������Ԓ����l�́CIORT ��{�s�Q14.5 �J���CIORT �Q12 �J���ł���CIORT �̌��ʂ͔F�߂��Ȃ������ƕ��Ă���B
�܂��CIORT �ɂق��̎��Ö@�p���邱�Ƃɂ���Đ������Ԃ����P�����Ƃ��������BValentini ��́C�p�O�Ǝ˂�IORT �p�����Q�̐������Ԓ����l��30 �J���ŁCIORT�{�p��Ǝ˂�22 �J���CIORT �P�Ƃ�13 �J�������L�ӂɗ\��ǍD�ł������ƕ��Ă��� 12�j�i���x��Ⅳb�j�B�܂��COgawa ��́CIORT ���s�����X��210 ��̐������Ԓ����l��19.1�J���ł���C���ɉ��w�Ö@�p�����Q��2 �N��������48.0���ŁC���w�Ö@�p���Ă��Ȃ��Q��2 �N������34.8�������L�ӂɗǍD�ł������ƕ��Ă��� 14�j�i���x��Ⅳb�j�B
�� �����ւ̒�
�킪������̑��{����RCT �ɂ��C�X���ɑ���⏕�Ö@�Ƃ���IORT �P�Ǝ��Âɂ͐����������ʂ��Ȃ����Ƃ��G�r�f���X�Ƃ��Ď����ꂽ�B�������C�⏕���w�Ö@�܂��͏p�O�E�p��Ǝ˂ȂǂƂ̕��p�ɂ��IORT �̗L�p��������F�߂���\���͔ے�ł��Ȃ��B��������IORT �Ƃق��̎��Ö@�̕��p���ʂɊւ��Ă͍���̌����ۑ�ł��낤�B
�� ���p����
1�j Kinoshita T, Uesaka K, Shimizu Y, et al. Effects of adjuvant intra-operative radiation therapy after curative resection in pancreatic cancer patients�FResults of a randomized study by 11 institutions in Japan. J Clin Oncol 2009�F27�F15s�isuppl�Gabstr 4622�j.
2�j �؉����C���S���v�C��⍎�F�C���D�X�������؏���̕⏕�Ö@�Ƃ��Ă̏p�����ː����ÁiIORT�j�̈Ӌ`��₤RCT�D���{�O�Ȋw��G�� 2010�G111�F161�D
3�j Hiraoka T, Kanemitsu K. Value of extended resection and intraoperative radiotherapy for resectable pancreatic cancer. World J Surg 1999�G23�F930-936.
4�j Reni M, Panucci MG, Ferreri AJ, et al. Effect on local control and survival of electron beam intraoperative irradiation for resectable pancreatic adenocarcinoma. Int J Radiat Oncol Biol Phys 2001�G50�F651-658.
5�j Okamoto A, Matsumoto G, Tsuruta K, et al. Intraoperative radiation therapy for pancreatic adenocarcinoma�Fthe Komagome hospital experience. Pancreas 2004�G28�F296-300.
6�j O�fConnor JK, Sause WT, Hazard LJ, et al. Survival after attempted surgical resection and intraoperative radiation therapy for pancreatic and periampullary adenocarcinoma. Int J Radiat Oncol Biol Phys 2005�G63�F1060-1066.
7�j Yamaguchi K, Nakamura K, Kobayashi K, et al. ERT following IORT improves survival of patients with resectable pancreatic cancer. Hepatogastroenterology 2005�G52�F1244-1249.
8�j Messick C, Hardacre JM, McGee MF, et al. Early experience with intraoperative radiotherapy in patients with resected pancreatic adenocarcinoma. Am J Surg 2008�G195�F308-311�Gdiscussion 312.
9�j Ruano-Ravina A, Almazán Ortega R, Guedea F. Intraoperative radiotherapy in pancreatic cancer�Fa systematic review. Radiother Oncol 2008�G87�F318-325.
10�j Valentini V, Morganti AG, Macchia G, et al. Intraoperative radiation therapy in resected pancreatic carcinoma�Flong-term analysis. Int J Radiat Oncol Biol Phys 2008�G70�F1094-1099.
11�j Showalter TN, Rao AS, Rani Anne P, et al. Does intraoperative radiation therapy improve local tumor control in patients undergoing pancreaticoduodenectomy for pancreatic adenocarcinoma�H A propensity score analysis. Ann Surg Oncol 2009�G16�F2116-2122.
12�j Valentini V, Calvo F, Reni M, et al. Intra-operative radiotherapy�iIORT�jin pancreatic cancer�Fjoint analysis of the ISIORT-Europe experience. Radiother Oncol 2009�G91�F54-59.
13�j Bachireddy P, Tseng D, Horoschak M, et al. Orthovoltage intraoperative radiation therapy for pancreatic adenocarcinoma. Radiat Oncol 2010�G5�F105.
14�j Ogawa K, Karasawa K, Ito Y, et al�GJROSG Working Subgroup of Gastrointestinal Cancers. Intraoperative radiotherapy for resected pancreatic cancer�Fa multi-institutional retrospective analysis of 210 patients. Int J Radiat Oncol Biol Phys 2010�G77�F734-742.
CQ 3-3�@�X���̏p�㉻�w���ː��Ö@�͐�������邩�H�H
| ����
|
�X���ɑ���p�㉻�w���ː��Ö@�̗L�p���͖��炩�ł͂Ȃ��C�����I�Ȉʒu�Â��Ƃ��čs����ׂ��ł���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�t���I���E���V�����x�[�X�ɂ����p�㉻�w���ː��Ö@�Ɋւ��郁�^�A�i���V�X��2 �� 1, 2�j�i���x��Ⅰ�j����Ă���BKhanna ��́C�����_������r�����iRCT�j4 �҂Ɣ��_������r����1�҂�p���āC�����\����������� 1�j�BRCT�́CGITSG�in��49�j 3�j�i���x��Ⅱ�j 4�j�i���x��Ⅳa�j�CNPST�in��61�j 5�j�i���x��Ⅱ�j�CEORTC�in��207�j 6�j�i���x��Ⅱ�j�CESPAC�in �� 217�j 7�j�i���x��Ⅱ�j��4 �҂ł���C���_������r������Hopkins Group �̘_���in �� 174�j 8�j�i���x��Ⅲ�j�ł������B���ʂ́C��p�P�Ƃɔ�ׂďp��̉��w���ː��Ö@�iCRT�j��2 �N��������12���i95��CI�F2�`22���j���P�����C�L�Ӎ���F�߂��ip ��0.022�j�B�������C�Ǘᐔ������3 �҂̎����iHopkins Group�CEORTC�CESPAC�j�Ɍ����Č�������ƁC���P����10���i95��CI�F�|1�`21���j�ɒቺ���C�L�Ӎ��͏��������ip ��0.084�j�B�ȏ�̌��ʂ���C�t���I���E���V�����x�[�X�Ƃ����p�㉻�w���ː��Ö@�̗L�p�����x�����鍪���͕s�\���ƌ��_���ꂽ�B
Stocken ��́CNorway �O���[�v 9�j�i���x��Ⅱ�j�C ESPAC 7�j�CEORTC 6�j�CGITSG 4�j�C���{����̕� 10�j�i���x��Ⅱ�j�C�ȏ�5 ��875 ���RCT �̂����C�t���I���E���V�����x�[�X�Ƃ����ގ��̃��W������p����EORTC ��ESPAC ��478 ��ɂ��ă��^�A�i���V�X�̌������s���� 2�j�B�������C���҂����n�U�[�h���1.09�i95��CI�F0.89�`1.32, p �� 0.43�j�ł���C�L�Ӎ���F�߂Ȃ������B�܂��C�������Ԓ����l��CRT �Q��15.8 �J�� �i95��CI�F13.9�`18.1�j�CCRT ���s��Ȃ������Q��15.2 �J���i95��CI�F13.1�`18.2�j�C2 �N�����5 �N�������͂��ꂼ��CRT �Q��30����12���CCRT ��{�s�Q��34����17���ł�������L�ӂȍ����Ȃ������B�\����q�ʂɔ�r�����Ƃ���CCRT ��R0 ���R1 �ł��L���ip �� 0.04�j�ł������B�ȏ���CR0 �؏��ł͏p��⏕�Ö@�Ƃ��ĉ��w���ː��Ö@�͐�������Ȃ����C�؏��f�[�z����R1 �؏��̉��w���ː��Ö@�̗L�p���ɂ��Ă͂���Ȃ錟�����K�v�Ƃ��ꂽ�B
���̌�C�I�����_����2 �҂̕⏕�������w���ː��Ö@�Ɋւ���RCT 11, 12�j�i���x��Ⅱ�j�����ꂽ�B�؏�����X������ѓ�����������120 ���⏕�������w���ː��Ö@�Q59��Ɗώ@�Q61 ��ɕ����C�O�����Ɍ��������Ƃ���C�⏕�������w���ː��Ö@�Q�Ŗ��������Ԃ͉����������C�S�������Ԃ͉������Ȃ����� 11�j�B�܂��C�A���P�[�g��QOL �������_���ł́C�⏕�������w���ː��Ö@�Q�ŗL�ӂ��u�Ɂip �� 0.02�j�ƚq�C�E�q�f�ip ��0.01�j�̏Ǐ������C�S�̂�QOL�͉��P����X�����������ip��0. 08�j 12�j�B
�܂��C�����������ł͂��邪�C��K�͂ȏǗ���W�ς��p����ː����w�Ö@������������5 �� 13-17�j�i���x��Ⅳb�j����B�����̕ł́C�⏕���w���ː��Ö@�͗\������P�������Ƃ��Ă���B
���݁C�X���ɑ��鉻�w�Ö@�̒��S�̓Q���V�^�r�����_���ł��邱�Ƃ���C�Q���V�^�r�����_���𒆐S�Ƃ����⏕���w���ː��Ö@�̃��W��������������Ă��邪�C3 �҂̕ɂƂǂ܂� 18, 19�j�i���x��Ⅳb�j 20�j�i���x��Ⅱ�j�B�����͂���������K�͂ȗՏ������ł���C���܂��L�p���������Ɏ����Ă��Ȃ��B
�p�㉻�w���ː��Ö@�k������50.4Gy/5.5 �T�̑̊O�Ǝˁ{�t���I���E���V���i250mg/m2/���C�Ò��j�l�̑O��ɁC�t���I���E���V���ƃQ���V�^�r�����_���̂����ꂩ��Ò����郌�W�������L�����ۂ���ׂɔ�r��������������iRTOG 9704�j 21�j�i���x��Ⅱ�j�B�X���������҂ł̓Q���V�^�r�����_���Q�̂ق����t���I���E���V���Q�����C�������Ԓ����l�i20.5 �J�� vs 16.9 �J���j��3 �N�������i31��vs 22���j�̓_�ŗD��Ă������C�L�ӂȍ��ł͂Ȃ������BRTOG 9704 �̒����\����݂��_�� 22�j�i���x��Ⅱ�j�����ꂽ���C5 �N�����������l�ɗL�Ӎ��͂Ȃ������B
�� �����ւ̒�
RCT �̌��ʂ���̓t���I���E���V�����x�[�X�Ƃ����X���ɑ���⏕���w���ː��Ö@�̗L�p���͏ؖ�����Ȃ������B�������CR1 �؏��Ǘ�ɑ��L�p�ł���\���������ꂽ���ƁC�����������ł͂��邪������̕���\�������������\����������Ă��邱�ƁC�Q���V�^�r�����_���ɂ��⏕���w���ː��Ö@�̉�͂����܂��ɕs�\���ł��邱�Ƃ���C���コ��Ȃ錟�����K�v�ł���B
�� ���p����
1�j Khanna A, Walker GR, Livingstone AS, et al. Is adjuvant 5-FU-based chemoradiotherapy for resectable pancreatic adenocarcinoma beneficial�H A meta-analysis of an unanswered question. J Gastrointest Surg 2006�G10�F689-697.
2�j Stocken DD, Büchler MW, Dervenis C, et al�GPancreatic Cancer Meta-analysis Group. Meta-analysis of randomised adjuvant therapy trials for pancreatic cancer. Br J Cancer 2005�G92�F1372-1381.
3�j The Gastrointestinal Tumor Study Group. A multi-institutional comparative trial of radiation therapy alone and in combination with 5-fluorouracil for locally unresectable pancreatic carcinoma. Ann Surg 1979�G189�F205-208.
4�j Gastrointestinal Tumor Study Group. Further evidence of effective adjuvant combined radiation and chemotherapy following curative resection of pancreatic cancer. Cancer 1987�G59�F2006-2010.
5�j Kalser MH, Ellenberg SS. Pancreatic cancer. Adjuvant combined radiation and chemotherapy following curative resection. Arch Surg 1985�G120�F899-903.
6�j Klinkenbijl JH, Jeekel J, Sahmoud T, et al. Adjuvant radiotherapy and 5-fluorouracil after curative resection of cancer of the pancreas and periampullary region�FphaseⅢtrial of the EORTC gastrointestinal tract cancer cooperative group. Ann Surg 1999�G230�F776-782.
7�j Neoptolemos JP, Stocken DD, Friess H et al�GEuropean Study Group for Pancreatic Cancer. A randomized trial of chemoradiotherapy and chemotherapy after resection of pancreatic cancer. N Engl J Med 2004�G350�F1200-1210.
8�j Yeo CJ, Abrams RA, Grochow LB, et al. Pancreaticoduodenectomy for pancreatic adenocarcinoma�Fpostoperative adjuvant chemoradiation improves survival. A prospective, single-institution experience. Ann Surg 1997�G225�F621-633�Gdiscussion 633-636.
9�j Bakkevold KE, Arnesjø�GB, Dahl O, et al. Adjuvant combination chemotherapy�iAMF�jfollowing radical resection of carcinoma of the pancreas and papilla of Vater--results of a controlled, prospective, randomised multicentre study. Eur J Cancer 1993�G29A�F698-703.
10�j Takada T, Amano H, Yasuda H, et al�GStudy Group of Surgical Adjuvant Therapy for Carcinomas of the Pancreas and Biliary Tract. Is postoperative adjuvant chemotherapy useful for gallbladder carcinoma�H A phaseⅢmulticenter prospective randomized controlled trial in patients with resected pancreaticobiliary carcinoma. Cancer 2002�G95�F1685-1695.
11�j Morak MJ, van der Gaast A, Incrocci L, et al. Adjuvant intra-arterial chemotherapy and radiotherapy versus surgery alone in resectable pancreatic and periampullary cancer�Fa prospective randomized controlled trial. Ann Surgery 2008�G248�F1031-1041.
12�j Morak MJ, Pek CJ, Kompanje EJ, et al. Quality of life after adjuvant intra-arterial chemotherapy and radiotherapy versus surgery alone in resectable pancreatic and periampullary cancer�Fa prospective randomized controlled study. Cancer 2010�G15�F830-836.
13�j Hsu CC, Herman JM, Corsini MM, et al. Adjuvant chemoradiation for pancreatic adenocarcinoma�Fthe Johns Hopkins Hospital-Mayo Clinic collaborative study. Ann Surg Oncol 2010�G17�F981-990.
14�j Corsini MM, Miller RC, Haddock MG, et al. Adjuvant radiotherapy and chemotherapy for pancreatic carcinoma�Fthe Mayo Clinic experience�i1975-2005�j. J Clin Oncol 2008�G26�F3511-3516.
15�j You DD, Lee HG, Heo JS, et al. Prognostic factors and adjuvant chemoradiation therapy after pancreaticoduodenectomy for pancreatic adenocarcinoma. J Gastointest Surg 2009�G13�F1699-1706.
16�j Merchant NB, Rymer J, Koehler EA, et al. Adjuvant chemoradiation therapy for pancreatic adenocarcinoma�Fwho really benefits�H J Am Coll Surg 2009�G208�F829-838.
17�j Yang R, Cheung MC, Byrne MM, et al. Survival effects of adjuvant chemoradiotherapy after resection for pancreatic carcinoma. Arch Surg 2010�G145�F49-56.
18�j Abrams RA, Winter KA, Regine WF, et al. Failure to adhere to protocol specified radiation therapy guidelines was associated with decreased survival in RTOG 9704--a Phase Ⅲ�Gtrial of adjuvant chemotherapy and chemoradiotherapy for patients with resected adenocarcinoma of the pancreas. Int J Radiat Oncol Biol Phys 2012�G82�F809-816.
19�j Ozkok S, Demirci S, Yalman D, et al. Postoperative gemcitabine alone and concurrent with radiation therapy in locally advanced pancreatic carcinoma. Tumori 2010�G96�F560-567.
20�j Van Laethem JL, Hammel P, Mornex F, et al. Adjuvant gemcitabine alone versus gemcitabine-based chemoradiotherapy after curative resection for pancreatic cancer�Fa randomized EORTC-40013-22012/FFCD-9203/GERCOR phaseⅡstudy. J Clin Oncol 2010�G28�F4450-4456.
21�j Regine WF, Winter KA, Abrams RA, et al. Fluorouracil vs gemcitabine chemotherapy before and after fluorouracil-based chemoradiation following resection of pancreatic adenocarcinoma�Fa randomized controlled trial. JAMA 2008�G299�F1019-1026.
22�j Regine WF, Winter KA, Abrams R, et al. Fluorouracil-based chemoradiation with either gemcitabine or fluorouracil chemotherapy after resection of pancreatic adenocarcinoma�F5-year analysis of the U.S. Intergroup/RTOG 9704 Phase Ⅲ�Gtrial. Ann Surg Oncol 2011�G18�F1319-1326.
CQ 3-4�@�p��⏕���w�Ö@���s�����Ƃ͐�������邩�H
| ����
|
�p��⏕���w�Ö@�͐؏��P�Ƃɔ�חǍD�Ȏ��Ð��т������Ă���C���{���邱�Ƃ����߂���i�O���[�hA�j�B�p��⏕�Ö@�̃��W������S-1 �P�ƗÖ@����������i�O���[�hA�j�CS-1 �ɑ���E�e�����Ⴂ�Ǘ�Ȃǂł̓Q���V�^�r�����_���P�ƗÖ@�����߂���i�O���[�hB�j�B |
|---|
�� �G�r�f���X
- �p��⏕���w�Ö@�Ɛ؏��P�ƂƂ̔�r����
�p��⏕���w�Ö@�Ɛ؏��P�Ƃ��r���������_������r�����́C���B����т킪���𒆐S�ɍs���Ă����B�m���E�F�[�ōs��ꂽ�����ł́C61 ���̍����؏���̊��҂��t���I���E���V���{�h�L�\���r�V�����_���{�}�C�g�}�C�V��C�iAMF�j�Ö@�{�s�Q�Ɛ؏��P�ƌQ�ɖ���ׂɊ���t���CAMF �Ö@�{�s�Q�̐������Ԓ����l���؏��P�ƌQ�����L�ӂɗǍD�ł��邱�Ƃ��������� 1�j�i���x��Ⅱ�j�C61 ���̒���14 ���̓����������҂��܂�ł����_�ŁC�����f�U�C���ɉۑ���܂�ł����B�킪���ōs��ꂽ�����ł́C508 ����X�E�_�����؏�����t���I���E���V���{�}�C�g�}�C�V��C �Ö@�Q�Ɛ؏��P�ƌQ�ɖ���ׂɊ���t�������C���̂����X��158 ��̃T�u�O���[�v�ɂ����ẮC�����ɑ���⏕���w�Ö@�̗L�����͎�����Ȃ����� 2�j�i���x��Ⅱ�j�B�܂��C89 ����X���؏�����t���I���E���V���{�V�X�v���`��* �Ö@�Q�Ɛ؏��P�ƌQ�ɖ���ׂɊ���t�����킪���̎����ɂ����Ă��C�⏕���w�Ö@�̐����ɑ���L�����͎�����Ȃ����� 3�j�i���x��Ⅱ�j�B
����h�C�c�𒆐S�ɁC�X���؏����354 ����Q���V�^�r�����_���P�܂ɂ��⏕���w�Ö@�Q�Ɛ؏��P�ƌQ�ɖ���ׂɊ���t����CONKO-001 �������s���C�⏕���w�Ö@�ɂ�閳�Ĕ��������Ԃ̗L�ӂȉ����������ꂽ 4�j�i���x��Ⅱ�j�B�����́C�⏕���w�Ö@���������Ԃ̗L�ӂȉ����������ɂ͎���Ȃ������ip �� 0.06�j���C���̌�̒����̒ǐՒ����ł́C���Ĕ��������Ԃ݂̂Ȃ炸�C�������Ԃ����L�ӂɉ��������邱�Ƃ����ꂽ 5�j�i���x��Ⅱ�j�B�܂��킪���ł́C118 ����X���؏���̊��҂��Q���V�^�r�����_���ɂ��⏕���w�Ö@�Q�Ɛ؏��P�ƌQ�ɖ���ׂɊ���t����JSAP-02 �������s���CCONKO-001 �����̓����̕Ɠ��l�C�Q���V�^�r�����_���ɂ��⏕���w�Ö@�����Ĕ��������Ԃ̗L�ӂȉ����������炷���Ƃ����ꂽ 6�j�i���x��Ⅱ�j�B
- �t���I���E���V���{�z���i�[�g�J���V�E��*���p�Ö@����уQ���V�^�r�����_���ɂ��p��⏕�Ö@
European Study Group of Pancreatic Cancer�iESPAC�j�ł́C�X���؏����289 ���two-by-two factorial design �ɂ���ĉ��w�Ö@�i�t���I���E���V���{�z���i�[�g�J���V�E��*�j�Q�C�t���I���E���V�����p���w���ː��Ö@�Q�C���w���ː��Ö@�{���w�Ö@�Q�C�؏��P�ƌQ��4 �Q�ɖ���ׂɊ���t���C���w���ː��Ö@���܂�2 �Q vs ���w���ː��Ö@���܂܂Ȃ�2 �Q�C���w�Ö@���܂�2 �Q vs ���w�Ö@���܂܂Ȃ�2�Q�ɂ����Đ������Ԃ��r�����iESPAC-1 �����j�B���̌��ʁC���w���ː��Ö@���܂�2 �Q�̐������Ԃ́C���w���ː��Ö@���܂܂Ȃ�2 �Q�̐������Ԃ���������ip �� 0.05�j���C�t���I���E���V�����x�[�X�Ƃ��鉻�w�Ö@���܂�2 �Q�́C���w�Ö@���܂܂Ȃ�2 �Q�����L�ӂɐ������Ԃ��ǍD�ł������ip��0.009�j���Ƃ������ꂽ 7�j�i���x��Ⅱ�j�B
�܂��C���̌�ESPAC �́C1,088 ����X���؏���̊��҂��t���I���E���V���{�z���i�[�g�J���V�E��* �ɂ��⏕���w�Ö@�Q�ƃQ���V�^�r�����_���ɂ��⏕���w�Ö@�Q�ɖ���ׂɊ���t����ESPAC-3 �������s���C�Q���V�^�r�����_���Q�ƃt���I���E���V���{�z���i�[�g�J���V�E��*�Q�̊Ԃɐ������Ԃ̗L�ӂȍ��͂Ȃ��������C�d�ĂȗL�Q���ۂ̓Q���V�^�r�����_���Q�̂ق����t���I���E���V���{�z���i�[�g�J���V�E��* �Q�����L�ӂɏ��Ȃ��������Ƃ���� 8�j�i���x��Ⅱ�j�B
�ȏ�̂��Ƃ��C�p��⏕���w�Ö@�C���ɃQ���V�^�r�����_����p�����p��⏕���w�Ö@�́C�؏��P�Ƃɔ�ׂāC���Ĕ��������Ԃ���ѐ������Ԃɂ����ėL�ӂɗǍD�Ȑ��т������C�܂��Q���V�^�r�����_���̓t���I���E���V���{�z���i�[�g�J���V�E��* �����d�ĂȗL�Q���ۂ����Ȃ��������Ƃ���C2012 �N�܂ł͏p��⏕���w�Ö@�̕W�����Â̓Q���V�^�r�����_���ł���ƈʒu�Â����Ă����B
- S-1 �ɂ��p��⏕�Ö@
�킪�����X���⏕���w�Ö@�����O���[�v�iJASPAC�j�́C�X���؏���̕⏕���w�Ö@�ɂ�����Q���V�^�r�����_���Ö@��S-1 �Ö@�̑�Ⅲ����r�����iJASPAC-01�j���s���CS-1 ���Q���V�^�r�����_���ɔ�ׂāC�X���؏���̑S��������і��Ĕ�������L�ӂɉ��������邱�Ƃ��C2013 �N��Gastrointestinal Cancers Symposium �Ŕ��\�����BJASPAC-01 �ł́C����I�ɍ����؏����{�s���ꂽ�X������385 �Ⴊ�o�^����C�p��̕⏕���w�Ö@�Ƃ��ăQ���V�^�r�����_���{�s�Q��S-1 �{�s�Q�ɖ���ׂɊ���t����ꂽ�B�ŏI�o�^����2 �N1 �J���ڂ̒ǐՃf�[�^�Œ��ԉ�͂��Ȃ���C�p��2 �N��������S-1 �Q�F70���C�Q���V�^�r�����_���Q�F53���CS-1 �̃Q���V�^�r�����_���Q�ɑ��鎀�S���C�x���g�Ƃ���n�U�[�h���0.56 �ł���CS-1 �̓Q���V�^�r�����_���ɔ�ׂėL�ӂɑS���������P����ip��0.001�j���Ƃ������ꂽ�B�܂��C2 �N���Ĕ�����������і��Ĕ��������Ԓ����l�́CS-1 �Q��49��, 23.2�J���C�Q���V�^�r�����_���Q��29���C11.2 �J���ł���CS-1 �̓Q���V�^�r�����_���ɔ�ׂĖ��Ĕ��������L�ӂɉ��P����ip��0.001�j���Ƃ������ꂽ 9�j�i���x��Ⅱ�j�B
�ȏ�̂��Ƃ���C2013 �N���݂ł́C�X���̏p��⏕���w�Ö@�Ƃ��Ă�S-1 �P�ƗÖ@���s�����Ƃ����������B���̍ۂ̃��W������JASPAC-01 �ɏ����āC�̕\�ʐςɉ�����1 ��40�`60mg�i�̕\�ʐ�1.25m2 �����F40mg�C1.25m2 �ȏ�1.5m2 �����F50mg�C1.5m2 �ȏ�F60mg�j��S-1 ��1 ��2 ��o�����^�i1 ����80�`120mg�j�C�����28 ���ԘA�����^���C���̌�14 ���Ԃ̋x����Ԃ�݂��C�ȏ�6 �T��1 �R�[�X�Ƃ�4 �R�[�X�J��Ԃ����Ƃ����������B
����C�p��R���g���[���s�ǂ̉�����o���ێ悪�s�\���ȏǗ�ȂǁCS-1 �̔E�e�����Ⴂ�ƍl������ꍇ�́C��r�I������Ő����Ⴂ�Q���V�^�r�����_����p�����p��⏕�Ö@�����߂���B
�� �����ւ̒�
�p��⏕���w�Ö@�̕W�����ẤC�]���̃Q���V�^�r�����_������V����S-1 �ɐ�ւ���ꂽ�B���㐔�N�̊ԂɁC�Q���V�^�r�����_���ƌo���t�b���s���~�W���Ƃ̕��p�Ö@�̗Տ������̌��ʂ����炩�ɂȂ�\��ł���B����C�����̗Տ������̌��ʂɂ����ڂ������B
�� ���p����
1�j Bakkevold KE, Arnesjø�GB, Dahl O, et al. Adjuvant combination chemotherapy�iAMF�jfollowing radical resection of carcinoma of the pancreas and papilla of Vater--results of a controlled, prospective, randomised multicentre study. Eur J Cancer 1993�G29A�F698-703.
2�j Takada T, Amano H, Yasuda H, et al�GStudy Group of Surgical Adjuvant Therapy for Carcinomas of the Pancreas and Biliary Tract. Is postoperative adjuvant chemotherapy useful for gallbladder carcinoma�H A phaseⅢmulticenter prospective randomized controlled trial in patients with resected pancreaticobiliary carcinoma. Cancer 2002�G95�F1685-1695.
3�j Kosuge T, Kiuchi T, Mukai K, et al�GJapanese Study Group of Adjuvant Therapy for Pancreatic Cancer�iJSAP�j. A multicenter randomized controlled trial to evaluate the effect of adjuvant cisplatin and 5-fluorouracil therapy after curative resection in cases of pancreatic cancer. Jpn J Clin Oncol 2006�G36�F159-165.
4�j Oettle H, Post S, Neuhaus P, et al. Adjuvant chemotherapy with gemcitabine vs observation in patients undergoing curative-intent resection of pancreatic cancer�Fa randomized controlled trial. JAMA 2007�G297�F267-277.
5�j Neuhaus P, Riess H, Post S, et al�GDeutsche Krebsgesellschaft�iCAO/AIO�j. CONKO-001�FFinal results of the randomized, prospective, multicenter phaseⅢtrial of adjuvant chemotherapy with gemcitabine versus observation in patients with resected pancreatic cancer�iPC�j. J Clin Oncol 2008�G26�Fabstr LBA4504.
6�j Ueno H, Kosuge T, Matsuyama Y, et al. A randomised phaseⅢtrial comparing gemcitabine with surgery-only in patients with resected pancreatic cancer�FJapanese Study Group of Adjuvant Therapy for Pancreatic Cancer. Br J Cancer 2009�G101�F908-915.
7�j Neoptolemos JP, Stocken DD, Friess H, et al�GEuropean Study Group for Pancreatic Cancer. A randomized trial of chemoradiotherapy and chemotherapy after resection of pancreatic cancer. N Engl J Med 2004�G350�F1200-1210.
8�j Neoptolemos JP, Stocken DD, Bassi C, et al�GEuropean Study Group for Pancreatic Cancer. Adjuvant chemotherapy with fluorouracil plus folinic acid vs gemcitabine following pancreatic cancer resection�Fa randomized controlled trial. JAMA 2010�G304�F1073-1081.
9�j Uesaka K, Fukutomi A, Boku N, et al. Randomized phaseⅢtrial of adjuvant chemotherapy with gemcitabine versus S-1 for patients with resected pancreatic cancer�iJASPAC-01 study�j. J Clin Oncol 2013�G31�isuppl�j�Fabstr 145.
4 ���ː��Ö@
CQ 4-1�@�Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���Â͉����H
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ���ꎟ���ÂƂ��ẮC���w���ː��Ö@�܂��͉��w�Ö@�P�Ƃɂ�鎡�Â����������i�O���[�hA�j�i���w���ː��Ö@�C���w�Ö@�̋�̓I�Ȏ��Ã��W�����́CCQ4-2�CCQ5-2�ɂ����Đ�������j�B |
|---|
�� �G�r�f���X
�؏��͍���ł��邪���u�]�ڂ�F�߂Ȃ��Ǐ��i�s�؏��s�\�X����ΏۂƂ������ː��Ö@�P�ƁC���w���ː��Ö@�C���w�Ö@�P�ƂɊւ��郉���_������r�����Ƃ��ẮC�Â���1988 �N�܂łɕ��ꂽ4 �̎��� 1-4�j�ƁC���ۂ̓o�^��1980 �N��i���\��2005 �N�j�ɍs��ꂽ1 �̎��� 5�j�́C�v5 �̎���������B���̌�14 �N�ԃ����_������r�����͂̕Ȃ��������C2002 �N�ȍ~�ɉ��w���ː��Ö@�C���w�Ö@�P�ƁC�x���Ö@�Ɋւ���4 �̃����_������r���������ꂽ 6-9�j�B�����̃����_������r�����̌��ʂ��܂Ƃ߁i�\4�j�C�Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���Âɂ��Č��������B
- ���w���ː��Ö@�ƕ��ː��Ö@�P�Ƃ̔�r�i3 �̃����_������r�����j
�č���Moertel ��́C�Ǐ��i�s�؏��s�\�������187 ��i�X��64 ��j�ɑ��ăt���I���E���V�����p���w���ː��Ö@�Q�ƕ��ː��Ö@�P�ƌQ�i�v���Z�{�Ƃ��Đ����H������_�H�j�Ƃɕ������d�ӌ��ɂ�郉���_������r�������{�s���C���w���ː��Ö@�Q�̐������Ԃ����ː��Ö@�P�ƌQ�ɔ䂵�L�ӂɗǍD�ł��邱�Ƃ�1969 �N�ɕ��Ă���i�������Ԓ����l�͉��w���ː��Ö@�Q��10.4 �J���C���ː��Ö@�P�ƌQ��6.3�J���j 1�j�i���x��Ⅱ�j�B���̌�C�č���Gastrointestinal Tumor Study Group�iGITSG�j�́C�Ǐ��i�s�؏��s�\�X���ɑ��ăt���I���E���V�����p���w���ː��Ö@�Q �i40Gy �Q�C60Gy �Q�j�ƕ��ː��Ö@�P�ƌQ�ƂɊ���t���郉���_������r�������{�s���C���w���ː��Ö@�Q�̐������Ԃ��L�ӂɗǍD�ł��邱�Ƃ�1981 �N�ɕ����i�������Ԓ����l��40Gy �̉��w���ː��Ö@�Q��10.6 �J���C60Gy �̉��w���ː��Ö@�Q��10.1 �J���C���ː��Ö@�P�ƌQ��5.7 �J���j 2�j�i���x��Ⅱ�j�B����C�č���Eastern Cooperative Oncology Group�iECOG�j�́C�Ǐ��i�s�؏��s�\�X��104 ��ɑ��ăt���I���E���V���ƃ}�C�g�}�C�V��C ���p���w���ː��Ö@�Q�ƕ��ː��Ö@�P�ƌQ�ƂɊ���t���郉���_������r���������{���i�o�^���Ԃ�1983 �N����1989 �N�j�C���Q�Ԃɂ͐������Ԃ̍����Ȃ��������Ƃ�2005 �N�ɕ����i�������Ԓ����l�͉��w���ː��Ö@�Q��8.4 �J���C���ː��Ö@�P�ƌQ��7.1 �J���j 5�j�i���x��Ⅱ�j�B���̎����̉��w���ː��Ö@�Q�ł̓t���I���E���V���ƃ}�C�g�}�C�V��C �ɂ��2 �܂̍R����p�̂��߂ɗL�Q���ۂ̔����������L�ӂɍ����ip��0.0002�j�C���ꂪ�������Ԃ̌���Ɍ��т��Ȃ������\��������B
�ȏ�̂��Ƃ���C���w���ː��Ö@�̐������Ԃ͕��ː��Ö@�P�Ƃɔ䂵�L�ӂɗǍD�ƍl������B
- ���w���ː��Ö@�Ǝx���Ö@�̔�r�i1 �̃����_������r�����j
���{��Shinchi ��́C�Ǐ��i�s�؏��s�\�X��31 ��ɑ��ăt���I���E���V�����p���w���ː��Ö@�Q�Ɩ����ÌQ�ƂɊ���t���郉���_������r�������{�s���C���w���ː��Ö@�Q�̐������Ԃ��L�ӂɗǍD�ł��邱�Ƃ�2002 �N�ɕ��Ă���i�������Ԓ����l�͉��w���ː��Ö@�Q��13.2 �J���C�����ÌQ��6.4 �J���j 6�j�i���x��Ⅱ�j�B�L�Q���ۂɊւ��āC���w���ː��Ö@�Q��grade 3 �̊�����6.3���ł������B
- ���w���ː��Ö@�Ɖ��w�Ö@�P�Ƃ̔�r�i4 �̃����_������r�����j
�č���ECOG �́C�Ǐ��i�s�؏��s�\�X��91 ��ɑ��ăt���I���E���V�����p���w���ː��Ö@�Q�ƃt���I���E���V���ɂ�鉻�w�Ö@�P�ƌQ�ƂɊ���t���郉���_������r�������{�s���C���Q�Ԃɂ͖��炩�ȍ����Ȃ����Ƃ�1985 �N�ɕ��Ă���i�������Ԓ����l�͉��w���ː��Ö@�Q��8.3 �J���C���w�Ö@�P�ƌQ��8.2 �J���j 3�j�i���x��Ⅱ�j�B���̎����ł͕��ː��̑����ʂ�40Gy �Ə��Ȃ��Ƃ����w�E������B����C�č���GITSG �́C�Ǐ��i�s�؏��s�\�X��43 ��ɑ��ăt���I���E���V�����p���w���ː��Ö@�Q�ƃX�g���v�g�]�V��* �{�}�C�g�}�C�V��C�{�t���I���E���V���ɂ�鉻�w�Ö@�P�ƌQ�ƂɊ���t���郉���_������r�������{�s���C���w���ː��Ö@�Q�̐������Ԃ��L�ӂɗǍD�ł��邱�Ƃ�1988 �N�ɕ����i�������Ԓ����l�͉��w���ː��Ö@�Q��10.5 �J���C���w�Ö@�P�ƌQ��8.0 �J���j 4�j�i���x��Ⅱ�j�B
�ߔN�C���w���ː��Ö@�ƃQ���V�^�r�����_���ɂ�鉻�w�Ö@�P�Ƃ�2 �̃����_������r����������Ă���B1 �̓t�����X��Fédération Francophone de Cancérologie Digestive/Société�GFrancophone de Radiotherapié�GOncologique�iFFCD/SFRO�j���C�Ǐ��i�s�؏��s�\�X��119 ��ɑ��ăt���I���E���V���{�V�X�v���`�����p���w���ː��Ö@�Q�ƁC�Q���V�^�r�����_���ɂ�鉻�w�Ö@�P�ƌQ�ƂɊ���t���郉���_�������������{�������̂ŁC���w�Ö@�P�ƌQ�̐������Ԃ��L�ӂɗǍD�ł��邱�Ƃ�2008 �N�ɕ��Ă���i�������Ԓ����l�͉��w���ː��Ö@�Q��8.6 �J���C���w�Ö@�P�ƌQ��13.0 �J���j 8�j�i���x��Ⅱ�j�B�L�Q���ۂɊւ��āCgrade 3�`4 �̊����͈ꎟ�Ö@���ƈێ��Ö@���̂ǂ�������w���ː��Ö@�Q�ŗL�ӂɍ��������i�ꎟ�Ö@���C�ێ����w�Ö@���Ŋe�X�C���w���ː��Ö@�Q��65.5���C78.1���C���w�Ö@�P�ƌQ��40.0���C40.0���j�B���̎����̉��w���ː��Ö@�Q�̐������Ԃ��]���̕����s�ǂȗ��R�Ƃ��āC�t���I���E���V���ƃV�X�v���`�����p�̂��߂ɗL�Q���ۂ������C�ێ����w�Ö@�̃Q���V�^�r�����_���̓��^�Ƒ����^�ʂ��L�ӂɒႩ�������Ƃ��W���Ă���ƍl�����Ă���B����C�č���ECOG �͋Ǐ��i�s�؏��s�\�X��71 ��ɑ��ăQ���V�^�r�����_�����p���w���ː��Ö@�Q�ƃQ���V�^�r�����_���ɂ�鉻�w�Ö@�P�ƌQ�ƂɊ���t���郉���_������r���������{���C���w���ː��Ö@�Q�̐������Ԃ��L�ӂɗǍD�ł��邱�Ƃ�2011 �N�ɕ��Ă���i�������Ԓ����l�͉��w���ː��Ö@�Q��11.1 �J���C���w�Ö@�P�ƌQ��9.2 �J���j 9�j�i���x��Ⅱ�j�B�L�Q���ۂɊւ��āCgrade 4�`5 �̊����͉��w���ː��Ö@�Q�ō����������i���w���ː��Ö@�Q��41���C���w�Ö@�P�ƌQ��9���j�Cgrade 3�`4 �̊����͗��Q�ō��͂Ȃ������i���w���ː��Ö@�Q��77���C���w�Ö@�P�ƌQ��79���j�B�����2 �̎����͓o�^�W�ς��x���C�r���Ŏ������I�����Ă��邽�߁C�����̎��ɑ���^�₪�悳��Ă���B
�ȏ�̂��Ƃ���C�����_�ʼn��w���ː��Ö@�Ɖ��w�Ö@�P�Ƃ̗D�ʐ������_�t���邱�Ƃ͂ł��Ȃ��B
- ���_
1�`3 ���Ǐ��i�s�؏��s�\�X���ɑ��ẮC1�C2 �ŏq�ׂ��悤�ɕ��ː��Ö@�P�Ƃ܂��͎x���Ö@�Ƃ̔�r����͉��w���ː��Ö@�����������B�܂��C3 �ŏq�ׂ��悤�ɉ��w���ː��Ö@�Ɖ��w�Ö@�P�Ƃ̃����_������r�����͑������錋�ʂł���C���̗D��ɂ��Ĉ��̃R���Z���T�X�͓����Ă��Ȃ��B���w���ː��Ö@�Ɖ��w�Ö@�P�Ǝ��Â͂��łɎ��n�f�ÂƂ��čL���Z�����Ă���C���S�����������Ƃ���ǂ�����ꎟ���ÂƂ��Đ������꓾��Ɣ��f�����B
* �ی������ڂ̌����E����
| �� �Տ������O���[�v |
�N | ���w���ː��Ö@ | ���ː� �Ö@ |
���w �Ö@ |
�ێ��� �w�Ö@ |
���Ґ� | �������� �����l�i���j |
p �l |
|---|---|---|---|---|---|---|---|---|
Moertel 1�j |
1969 | 35�`40Gy�{5-FU — |
— 40Gy |
— — |
— — |
32 32 |
10.4 6.3 |
<�G0.05 |
Moertel 2�j |
1981 | 40Gy�{5-FU 60Gy�{5-FU — |
— — 60Gy |
— — — |
5-FU 5-FU — |
28 31 25 |
10.6 10.1 5.7 |
<�G0.01 <�G0.01 |
Klaassen 3�j |
1985 | 40Gy�{5-FU — |
— — |
— 5-FU |
5-FU 5-FU |
47 44 |
8.3 8.2 |
n.s. |
GITSG 4�j |
1988 | 54Gy�{5-FU — |
— — |
— SMF |
SMF SMF |
22 21 |
10.5 8.0 |
0.02 |
Cohen 5�j |
2005 | 59.4Gy�{5-FU�{MMC — |
— 59.4Gy |
— — |
— — |
55 49 |
8.4 7.1 |
0.16 |
Shinchi 6�j |
2002 | 50.4Gy�{5-FU — |
— — |
— — |
5-FU — |
16 15 |
13.2 6.4 |
0.0009 |
Li 7�j |
2003 | 50. 4�`61. 2 Gy�{5-FU 50. 4�`61. 2 Gy�{GEM |
— — |
— — |
GEM GEM |
16 18 |
6.7 14.5 |
0.027 |
Chauffert 8�j |
2008 | 60 Gy�{5 -FU�{CDDP — |
— — |
— GEM |
GEM GEM |
59 60 |
8.6 13.0 |
0.03 |
Loehrer 9�j |
2011 | 50.4Gy�{GEM — |
— — |
— GEM |
GEM GEM |
34 37 |
11.1 9.2 |
0.017 |
5-FU�F�t���I���E���V��
MMC�F�}�C�g�}�C�V��C
GEM�F�Q���V�^�r�����_��
CDDP�F�V�X�v���`��
SMF�F�X�g���v�g�]�V��*�C�}�C�g�}�C�V��C�C�t���I���E���V��
n.s.�F�L�Ӎ��Ȃ�
�� �����ւ̒�
�Ǐ��i�s�؏��s�\�X���̎��Ð��т́C�Q���V�^�r�����_����S-1 �Ȃǂ̐V�K�R������p�������Âɂ�菭�������サ�Ă��Ă��邪�iCQ4-2�CCQ5-2�j�C�܂������������̂ł͂Ȃ��C�Տ������ł̎��ÊJ�����]�܂��ł���B���w���ː��Ö@�̗��_�Ƃ��ẮC���w�Ö@�P�Ƃɔ䂵�C2 �N���������Ȃǂ̒������I�Ȑ��������̌����}��邱�Ƃ�C�Ǐ�����ɂ���u�Ɋɘa�����҂ł��邱�ƂȂǂ�����iCQ4-6�j�B����C���w�Ö@�P�Ƃ̗��_�́C���w���ː��Ö@�ɔ䂵�L�Q���ۂ��y���C�O�����Â��\�Ȃ��Ƃ���������B���Õ��j����̍ۂɂ́C���ꂼ��̎��Â̗L�����ƂƂ��Ɏ��Õ��@�E���ÃX�P�W���[���C�L�Q���ۂȂǂ��܂߂����������邱�Ƃ��K�v�ł���B�܂�����̗Տ������ɂ���ė����Ö@�̗D���ʒu�Â��𖾂炩�ɂ��邱�Ƃ��d�v�ł���B
�� ���p����
1�jMoertel CG, Childs DS Jr, Reitemeier RJ, et al. Combined 5-fluorouracil and supervoltage radiation therapy of locally unresectable gastrointestinal cancer. Lancet 1969�G2�F865-867.
2�jMoertel CG, Frytak S, Hahn RG, et al. Therapy of locally unresectable pancreatic carcinoma�Fa randomized comparison of high dose�i6000 rads�jradiation alone, moderate dose radiation�i4000 rads�{5-fluorouracil�j, and high dose radiation�{5-fluorouracil�FThe Gastrointestinal Tumor Study Group. Cancer 1981�G48�F1705-1710.
3�jKlaassen DJ, MacIntyre JM, Catton GE, et al. Treatment of locally unresectable cancer of the stomach and pancreas�Fa randomized comparison of 5-fluorouracil alone with radiation plus concurrent and maintenance 5-fluorouracil--an Eastern Cooperative Oncology Group study. J Clin Oncol 1985�G3�F373-378.
4�jGastrointestinal Tumor Study Group. Treatment of locally unresectable carcinoma of the pancreas�Fcomparison of combined-modality therapy�ichemotherapy plus radiotherapy�jto chemotherapy alone. J Natl Cancer Inst 1988�G80�F751-755.
5�jCohen SJ, Dobelbower R Jr, Lipsitz S, et al. A randomized phaseⅢstudy of radiotherapy alone or with 5-fluorouracil and mitomycin-C in patients with locally advanced adenocarcinoma of the pancreas�FEastern Cooperative Oncology Group study E8282. Int J Radiat Oncol Biol Phys 2005�G62�F1345-1350.
6�jShinchi H, Takao S, Noma H, et al. Length and quality of survival after external-beam radiotherapy with concurrent continuous 5-fluorouracil infusion for locally unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 2002�G53�F146-150.
7�jLi CP, Chao Y, Chi KH, et al. Concurrent chemoradiotherapy treatment of locally advanced pancreatic cancer�Fgemcitabine versus 5-fluorouracil, a randomized controlled study. Int J Radiat Oncol Biol Phys 2003�G57�F98-104.
8�jChauffert B, Mornex F, Bonnetain F, et al. PhaseⅢtrial comparing intensive induction chemoradiotherapy�i60 Gy, infusional 5-FU and intermittent cisplatin�jfollowed by maintenance gemcitabine with gemcitabine alone for locally advanced unresectable pancreatic cancer. Definitive results of the 2000-01 FFCD/SFRO study. Ann Oncol 2008�G19�F1592-1599.
9�jLoehrer PJ Sr, Feng Y, Cardenes H, et al. Gemcitabine alone versus gemcitabine plus radiotherapy in patients with locally advanced pancreatic cancer�Fan Eastern Cooperative Oncology Group trial. J Clin Oncol 2011�G29�F4105-4112.
CQ 4-2�@�Ǐ��i�s�؏��s�\�X���ɑ��Đ�������鉻�w���ː��Ö@�͉����H
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ��āC���ː��Ö@���s���ꍇ�ɂ́C�t�b���s���~�W���n�R�����܂��̓Q���V�^�r�����_���Ƃ̕��p�����������i�O���[�hB�j�B ���ː��Ö@�ɂ��ẮC3 �������Ìv����s���C��ᇂɑ��鐳�m�ȏƎ˂Ɛ��푟��ւ̐��ʒጸ��}�邱�Ƃ����������B |
|---|
�� �G�r�f���X
�Ǐ��i�s�؏��s�\�X���ɑ��鉻�w���ː��Ö@�ɂ��āC����܂łɓ����Ă���G�r�f���X���������B
�t���I���E���V���͌Â������������̎��Ö�Ƃ��ėp�����Ă������C���ː��̑����܂Ƃ��Ă����̗L�������m���Ă���C�����̌Ō`���ɑ��ĕ��p�Ö@�����݂��Ă����B�؏��s�\�X���̕W�����ÂƂ��ĉ��w���ː��Ö@����������鍪���ƂȂ���3 �̃����_������r�����ɂ����Ă��C�t���I���E���V�����x�[�X�Ƃ������w�Ö@���p�����Ă��� 1-3�j�i���x��Ⅱ�j�C�܂��č��́wNCCN �K�C�h���C���x�i2012 �N�Łj�ɂ����ẮC������45�`54Gy�i1 ��1.8�`2.4Gy�j�̕��ː��Ö@�Ƀt���I���E���V�����x�[�X�Ƃ������w�Ö@�̓������p����������Ă���B
�������Ȃ���C���̋�̓I�ȃ��W�����ɂ��Ă͂��܂������i�K�ł���C���̃R���Z���T�X�͓����Ă��Ȃ��B�t���I���E���V���͂��̖\�I���Ԃ������قǁC���ː��ɑ��鑝����p���������邱�Ƃ��m���Ă���C���ː��Ƃ̕��p�Ö@�ɂ����āC�����Ò��iprotracted venous infusion�GPVI�j���{�[���X�Ò������ʂ̖ʂŗD��Ă��邱�Ƃ��C�������iⅡ�`Ⅲ���j�ɑ��郉���_������r�����ɂ����Ď�����Ă���B����Ɋ�Â��C�X���̎��Âɂ����Ă��C�t���I���E���V�������Ò��ƕ��ː��Ƃ̂��܂��܂ȕ��p�Ö@�����݂��Ă������C�����_������r�������s���ɂ͎����Ă��炸�C�������̔�r�����ɂ����ẮC���Ë��x�C�������Ԃɂ����āC�����Ò��̗D�ʐ����������Ƃ͂ł��Ȃ����� 4�j�i���x��Ⅲ�j�B
����C2006 �N�C�X���ɑ��ĐV�K�ɕی��K�����F���ꂽS-1 �́C�t���I���E���V�������Ò��Ɠ��l�C�����t���I���E���V���Z�x����荂�Z�x�ł������Ԏ����������p�������C�ق��̊���ɂ����Ă����ː��Ö@�Ƃ̕��p���ʂ����҂�����܂ł���B�X���ɑ�����ː��Ö@�Ƃ̕��p�ɂ��ẮC��Ⅰ�CⅡ�������̕�����C�S�������Ԃ�12.9�`16.8 �J���i�����l�j�ł����� 5-8�j�i���x��Ⅲ�j�B�����̎����ɂ�������ː��Ö@�̃��W�����ɂ́C�]���̃t���I���E���V�����p���W�����Ɠ��l��50Gy ���x�̐��ʁi1 ��1.8Gy �ɂ�1 ��1 ��܂���1 ��1.25Gy �ɂ�1 ��2 ��j���p�����Ă���B�t���I���E���V�����p���w���ː��Ö@�Ƃ̔�r�����͂���܂łɂȂ����C�o����ł��邱�Ƃ̗����ɂ��C�wNCCN �K�C�h���C���x�i2012 �N�Łj�ɂ����Ă͓������t�b���s���~�W���n�o���R�����ł���J�y�V�^�r��*���I�����Ƃ��ċ������Ă���B
�Ȃ��C�V�X�v���`���ɂ��Ă��C���ː�������p�����҂����p�����݂�ꂽ���C�V�X�v���`���P���ʘA�����^�ł̓������p�ɂ����Ă͓Ő��������C�L�����͎�����Ȃ����� 9�j�i���x��Ⅲ�j�B
�Q���V�^�r�����_���̓t���I���E���V���Ƃ̃����_������r�����̌��ʁC�؏��s�\�X���ɑ���ꎟ���w�Ö@�ƈʒu�Â����Ă��邪�C���ː��Ö@�Ƃ̕��p�ɂ��ẮC�܂Ƃ܂�����r�������Ȃ��B�������C�X���ւ̎g�p���J�n����Ă��猻�݂܂łɁC��Ⅰ�CⅡ�������𒆐S�Ƃ����������ʂ͐���������Ă��� 10, 11, 13, 15�j�i���x��Ⅲ�j 12�j�i���x��Ⅳb�j 14�j�i���x��Ⅱ�j�i���{�ł�2002 �N���ی��K�p�j�B���̎��Ð��т͑S�������Ԃ�8.2�`16.6 �J���i�����l�j�ƕ��͂�����̂́C2�`3 �N���钷����������U������邱�Ƃ������̂ЂƂł���B�������C�����ǂւ̓Ő��Ȃǂ̍����ǂ̊����������C���S�����m�F����Ă��Ȃ����W�����͕��p�Ö@�Ƃ��Ďg�p�����ׂ��ł͂Ȃ��B��܂̓��^�ʁC���ː��Ö@�̏Ǝː��ʂ�Ǝ˃X�P�W���[���Ȃǂɂ��Ă͂��܂��R���Z���T�X�͓����Ă��Ȃ����C����܂ł̕������Ƃ��Ă͑傫��2 �̕��@�ɕ����邱�Ƃ��ł���B�ЂƂ́C�ʏ핪���@��p����45�`54Gy�k1 ��1.8Gy�`2.0Gy�C�����w�I�������ʁibiologically effective dose�GBED�j60�`65Gy�l�̕��ː��Ö@�ɏ��ʂ̃Q���V�^�r�����_���i�ʏ퓊�^�ʂ�25�`60�����x�C������100mg/m2�ȉ��̒�p�ʂŏT2 �^�j�����p���郌�W���� 10, 11, 13-15�j�C��������́C�����ʁC�����i�Ǝˊ��ԁj�����������ː��Ö@�i��Ƃ��āC������36Gy�C1 ��2.4Gy�CBED 45Gy�j�ɍ��Z�x�̃Q���V�^�r�����_���i1,000mg/m2�j�p������@�ł��� 12�j�B�O�҂́C������x�L���͈͂̏Ǝ˖��ݒ肵�i�����͗\�h�I�����p�ߗ̈���܂ށj�C�L�Q���ۂ����e�ł���ő哊�^�ʂł̖�܂̑�����p�����҂������̂ł���C��҂́C�Տ��W�I�̐ςɗ\�h�I�����p�ߗ̈���܂������܂܂Ȃ����@�Ŏ��͑���ւ̗L�Q���ۂ��I�Ɍy�����C�Ǐ����ÂƓ����ɑS�g���Â��������邱�Ƃ�_���Ƃ������̂ł���B�����p�ߗ̈�̗\�h�Ǝ˂ɂ��Ă͋c�_�̕������Ƃ���ł��邪�C�ڍׂ�CQ4-3 ���Q�Ƃ��ꂽ���B�܂��C���w���ː��Ö@�̑O�ɓ������w�Ö@���s�����W�������ߔN���݂��Ă��� 16�j�i���x��Ⅲ�j�B���u�]�ڂ������Ɍ��݉�����Ǘ�i�Ǐ��Ö@�ł�����ː��Ö@�̏�悹���ʂ��������ƍl������Ǘ�j��I�ʂ��邱�Ƃ��ړI�̂ЂƂƍl�����Ă��邪�C���w�Ö@���s���邱�ƂŁC���ː��Ö@�̃R���v���C�A���X�⊴�����炩�̉e������\��������C�S�̓I�Ȏ��Ì��ʂƂ��ẮC����̌��،��ʂ�҂K�v������i�ڍׂ�CQ4-4 ���Q�Ɓj�B
�Ȃ��C�Ǝ˕��@�ɂ��ẮC���G�l���M�[��X����p���邱�Ƃ��]�܂����C���X�N����ւ̐��ʂ��l����3 �������Ìv����s�����Ƃ����������B�̊�����ʕ��ː����Áistereotactic body radiation therapy�GSBRT�j�⋭�x�ϒ����ː����Áiintensity modulated radiation therapy�GIMRT�j�Ȃǂ̍����x���Â◱�q�����Â̓������ߔN���݂��Ă���B����������͑���ւ̗L�Q���ۂ������邱�ƂȂ����ʑ������s�����Ƃ�ړI�Ƃ������̂ł��邪�C�����_�ł͂��܂��������x���ł���B
�ȏ���C�����_�ɂ����āC�Ǐ��i�s�؏��s�\�X���ɑ��ĉ��w���ː��Ö@���s���ꍇ�C�t�b���s���~�W���n�R�����܂��̓Q���V�^�r�����_���Ƃ̕��p�����������B���p���̋�̓I�ȃ��W�����ɂ��Ă͂��܂����̃R���Z���T�X�͓����Ă��Ȃ����C���ː��Ö@�Ɋւ��Ă͍��G�l���M�[��X ����p���C���X�N����ւ̐��ʂ��l����3 �������Ìv����s�����Ƃ��]�܂����B
�� �����ւ̒�
��ʓI�ɁC�X���͑����ɉ��u�]�ڂ����������������C�Ǐ��i�s�؏��s�\�X���ɑ��鎡�Âɂ����ẮC�Ǐ����ÂƑS�g�Ö@�Ƃ̃o�����X���d�v�ƍl������B���w���ː��Ö@�ɂ����郌�W�����̊������C�L�����ɂ��ẮC���ː��Ö@�̐��ʂ�Ǝ˖�̐ݒ�C���ʕ����C�Ǝ˕��@�ɂ���Ă��傫���e������邱�Ƃɒ��ӂ��ꂽ���B�܂��C���ݐi�s�����镪�q���x���ł̌������ʂɊ�Â��C�X�̐i�s�p�^�[������ʂ�\�������Ö@��I�����鎎�݂��i�߂��Ă���C����̔��W�����҂����B
������ɂ��Ă��C�ߋ�20 �N�Ԃɂ�������ː����ËZ�p�̐i�����X�����Âւ��݂₩�ɁC���K�ɔ��f������w�͂��]�܂��B
�� ���p����
1�j Moertel CG, Childs DS Jr, Reitemeier RJ, et al. Combined 5-fluorouracil and supervoltage radiation therapy of locally unresectable gastrointestinal cancer. Lancet 1969�G2�F865-867.
2�j Moertel CG, Frytak S, Hahn RG, et al. Therapy of locally unresectable pancreatic carcinoma�Fa randomized comparison of high dose�i6000 rads�jradiation alone, moderate dose radiation�i4000 rads�{5-fluorouracil�j, and high dose radiation�{5-fluorouracil�FThe Gastrointestinal Tumor Study Group. Cancer 1981�G48�F1705-1710.
3�j Gastrointestinal Tumor Study Group. Treatment of locally unresectable carcinoma of the pancreas�Fcomparison of combined-modality therapy�ichemotherapy plus radiotherapy�jto chemotherapy alone. J Natl Cancer Inst 1988�G80�F751-755.
4�j Mehta VK, Poen JC, Ford JM, et al. Protracted venous infusion 5-fluorouracil with concomitant radiotherapy compared with bolus 5-fluorouracil for unresectable pancreatic cancer. Am J Clin Oncol 2001�G24�F155-159.
5�j Kim HM, Bang S, Park JY, et al. Phase Ⅱ�Gtrial of S-1 and concurrent radiotherapy in patients with locally advanced pancreatic cancer. Cancer Chemother Pharmacol 2009�G63�F535-541.
6�j Sudo K, Yamaguchi T, Ishihara T, et al. Phase Ⅱ�Gstudy of oral S-1 and concurrent radiotherapy in patients with unresectable locally advanced pancreatic cancer. Int J Radiat Oncol Biol Phys, 2011�G80�F119-125.
7�j Shinchi H, Maemura K, Mataki Y, et al. A phaseⅡstudy of oral S-1 with concurrent radiotherapy followed by chemotherapy with S-1 alone for locally advanced pancreatic cancer. J Hepatobiliary Pancreat Sci 2012�G19�F152-158.
8�j Ikeda M, Ioka T, Ito Y, et al. A multicenter Phase Ⅱ�Gtrial of S-1 with concurrent radiation therapy for locally advanced pancreatic cancer. Int J Radiat Oncol Biol Phys 2013�G85�F163-169.
9�j Okusaka T, Okada S, Tokuuye K, et al. Lack of effectiveness of radiotherapy combined with cisplatin in patients with locally advanced pancreatic carcinoma. Cancer 2001�G91�F1384-1389.
10�j Blackstock AW, Tepper JE, Niedwiecki D, et al. Cancer and leukemia group B�iCALGB�j89805�FphaseⅡchemoradiation trial using gemcitabine in patients with locoregional adenocarcinoma of the pancreas. Int J Gastrointest Cancer 2003�G34�F107-116.
11�j Okusaka T, Ito Y, Ueno H, et al. PhaseⅡstudy of radiotherapy combined with gemcitabine for locally advanced pancreatic cancer. Br J Cancer 2004�G91�F673-677.
12�j Murphy JD, Adusumilli S, Griffith KA, et al. Full-dose gemcitabine and concurrent radiotherapy for unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 2007�G68�F801-808.
13�j Girard N, Mornex F, Bossard N, et al. Estimating optimal dose of twice-weekly gemcitabine for concurrent chemoradiotherapy in unresectable pancreatic carcinoma�Fmature results of GEMRT-01 Phase I trial. Int J Radiat Oncol Biol Phys 2010�G77�F1426-1432.
14�j Loehrer PJ Sr, Feng Y, Cardenes H, et al. Gemcitabine alone versus gemcitabine plus radiotherapy in patients with locally advanced pancreatic cancer�Fan Eastern Cooperative Oncology Group trial. J clin Oncol 2011�G29�F4105-4112.
15�j Shibuya K, Oya N, Fujii T, et al. Phase Ⅱstudy of radiation therapy combined with weekly low-dose gemcitabine for locally advanced, unresectable pancreatic cancer. Am J Clin Oncol 2011�G34�F115-119.
16�j Kurt E, Kurt M, Kanat O, et al. PhaseⅡstudy of induction chemotherapy with gemcitabine plus 5-fluorouracil followed by gemcitabine-based concurrent chemoradiotherapy for unresectable locally advanced pancreatic cancer. Tumori 2006�G92�F481-486.
- CQ 4-3
- �Ǐ��i�s�؏��s�\�X���ɑ���O�����ː��Ö@�ł́C�ǂ̂悤�ȗՏ��W�I�̐ς�ݒ肷��̂��悢���H
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ���O�����ː��Ö@�ł́C����I��ᇑ̐ςƓ]�ڕp�x�̍��������p�ߌQ�݂̂��܂Տ��W�I�̐ςɂ��邱�Ƃ����߂���i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�Ǐ��i�s�؏��s�\�X���ɑ��ẮC���w���ː��Ö@���s�����Ƃ���������Ă���iCQ4-1�j�B���̍ۂ̕��ː��Ö@�̗Տ��W�I�̐ρiclinical target volume�GCTV�j�Ƃ��āC����I��ᇑ̐ρigross tumor volume�GGTV�j�ɋǏ��̌������I�i�W�݂̂������邾���łȂ��C���̂Ȃ������p�ߗ̈�i�\�h�I�����p�ߗ̈�j���܂߂�K�v�����邩�ɂ��Č��������B
�X���̓����p�ǐZ����_�o���͐Z���̕p�x���������߁C���ɉ��Ăł͗\�h�I�����p�ߗ̈�Ƃ���Th11 ����L3 �t�߂܂ł̖T�哮�������p�ߗ̈���܂Ǝ˖�Ŏ��Â��s���Ă����B�p�㉻�w���ː��Ö@�̏ꍇ�́C���݂ł��\�h�I�����p�ߗ̈���܂߂��L���Ǝ˖삪�p�����邱�Ƃ������B
�������Ǐ��i�s�؏��s�\�X���ɑ��ẮC���������̂̐��䂪����ł���C�\�h�I�����p�ߗ̈�܂ŏƎ˖�Ɋ܂߂�Ӌ`�͖R�����Ƃ���l����������B���̂��ߓ��ɉ��w�Ö@�p����ꍇ�́CGTV �̂݁C�܂���GTV ���X���͂̃����p�߂݂̂Ɍ��ǂ����Ǝ˖@�����݂���悤�ɂȂ��Ă����B
CTV �ɗ\�h�I�����p�ߗ̈���܂߂邩�ǂ����Ɋւ��ẮC����܂őO������r�����͍s���Ă��炸�C�����ꂩ�̕��@��ϋɓI�Ɏx�����邾���̉Ȋw�I�����͂Ȃ��B���ۂ̃P�[�X�V���[�Y�̕ł�GTV �}�]�ڕp�x�̍��������p�ߌQ��CTV �Ƃ��ďƎ˂��s���C���Â͂قƂ�ǂ̏Ǘ�Ŋ����\�ŁC�Ǝ˖�O�����p�ߍĔ��͂Ȃ������C�Ƃ������U������� 1-3�j�i���x��Ⅳb�j�B
�܂��؏���̕a���g�D�w�I�ώ@�̕ł́C�]�ڕp�x�̍��������p�߂��X���͂Ɍ��ǂ��Ă����Ƃ�����̂� 4�j�i���x��Ⅴ�j�C�����p���͖T�哮�������p�ߗ̈��̎������i�W��������X���x���ɂƂǂ܂��Ă��邱�Ƃ������Ƃ�����̂����� 5�j�i���x��Ⅴ�j�B�킪���́w�X���戵���K��x�i��6 �Łj�ł́C�����p������p�ߓ]�ڗ��C�\��̐��тɊ�Â��C�������ʂɉ����ă����p�ߗ̈��3�Q�ɕ��ނ��Ă���i�\5�j 6�j�B
| ���� | �̔��� | |
|---|---|---|
| 1 �Q�����p�� | 13a�C13b�C17a�C17b |
8a�C8p�C10�C11p�C11d�C18 |
| 2 �Q�����p�� | 6�C8 a�C8 p�C12 a�C12 b�C12 p�C14 p�C14d |
7�C9�C14p�C14d�C15 |
| 3 �Q�����p�� | 1�C2�C3�C4�C5�C7�C9�C10�C11p�C11d�C |
5�C6�C12 a�C12 b�C12 p�C13 a�C13 b�C17 a�C |
����C�\�h�I�����p�ߗ̈���܂߂��L���Ǝ˖�̏ꍇ�͏Ǝˑ̐ϓ��Ɋ܂܂�钰�ǂ̑̐ς������C������Ő��������Ȃ�f�����b�g������B���������Z���^�[����̕ɂ��ƁC�Q���V�^�r�����_���p�������w���ː��Ö@�̏ꍇ�C�v��W�I�̐ρiplanning target volume�GPTV�j��500cm3 �ȏ��grade 3 �ȏ�̏�����Ő��̕p�x���L�ӂɍ����Ƃ������ʂł����� 7�j�i���x��Ⅳb�j�B
���̂悤�ɏ��Ȃ��Ƃ��L���\�h�I�����p�ߗ̈�ݒ�̕K�v���́C�Ǐ�����̖ʂ�����L�Q���ۂ̊ϓ_������������Ƃ����������B�wNCCN �K�C�h���C���x�i2012 �N�Łj�ł̓J�e�S���[2A�̐����x�ŁC�W���I��CTV��GTV�{0.5�`1.5cm �ł���Ƃ��C�����0.5�`2cm �̌ċz���ړ��Ȃǂ���������PTV �}�[�W���������邱�Ƃ��X���ߖT�̃����p�߁iperi-pancreatic nodes�j���T�ˊ܂܂��Ƃ��Ă���B�܂��ƎˋZ�p�I�ɂ͑̊�����ʕ��ː����ÁiSBRT�j 8�j�i���x��Ⅳb�j�⋭�x�ϒ����ː����ÁiIMRT�j 9�j�i���x��Ⅳb�j�Ƃ����Z�@�ɂĐ��ʂ̏W���������߂���@���p������悤�ɂȂ��Ă����BSBRT �ł�CTV �ɗ\�h�I�����p�ߗ̈��S���܂߂Ȃ��Ǝ˖@�CIMRT �ł͓]�ڂ̕p�x�����������p�ߌQ���܂ޏƎ˖@���p�����邱�Ƃ��������C�����Ǝ˖@��Ǝ˔͈͂̔�r�ɂ��Ă͍���̗Տ������ɂ�錟���K�v�ł���B
�ȏ���C�����_�ɂ����ẮC�Ǐ��i�s�؏��s�\�X���̉��w���ː��Ö@���ɂ́C���ː��Ö@�̐��ʑ����C����щ��w�Ö@�̕��p���l������ƁC�L�͂ȗ\�h�I�����p�ߗ̈�̐ݒ�͊��߂��邾���̍������Ȃ��CCT �ŔF�߂���GTV �Ɠ]�ڂ̕p�x�����������p�ߌQ�݂̂�CTV �Ɋ܂ނ��Ƃ����߂���B
�� �����ւ̒�
�����x���ː����ËZ�p�̓o��ɂ��C�X���ɑ��Ă����ʏW�����̍������ː��Ö@���s����悤�ɂȂ����B�K�ȏƎ˔͈͂ɂ��ẮC�����p�ߓ]�ڂ̕p�x�������ɂ���CTV ��ݒ肵���Ǝ˔͈͕ʂ̔�r�������s���C�K��������Ă������l������ƍl����B
�� ���p����
1�jKawakami H, Uno T, Isobe K, et al. Toxicities and effects of involved-field irradiation with concurrent cisplatin for unresectable carcinoma of the pancreas. Int J Radiat Oncol Biol Phys 2005�G62�F1357-1362.
2�jTokuuye K, Sumi M, Kagami Y, et al. Small-field radiotherapy in combination with concomitant chemotherapy for locally advanced pancreatic carcinoma. Radiother Oncol 2003�G67�F327-330.
3�jMurphy JD, Adusumilli S, Griffith KA, et al. Full-dose gemcitabine and concurrent radiotherapy for unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 2007�G68�F801-808.
4�jBrunner TB, Merkel S, Grabenbauer GG, et al. Definition of elective lymphatic target volume in ductal carcinoma of the pancreatic head based on histopathologic analysis. Int J Radiat Oncol Biol Phys 2005�G62�F1021-1029.
5�jNagakawa T, Kobayashi H, Ueno K, et al. Clinical study of lymphatic flow to the paraaortic lymph nodes in carcinoma of the head of the pancreas. Cancer 1994�G73�F1155-1162.
6�j���{�X���w��ҁD�X���戵���K��i��6�Łj�D�����o�ŁC2009
7�jIto Y, Okusaka T, Kagami Y, et al. Evaluation of acute intestinal toxicity in relation to the volume of irradiated small bowel in patients treated with concurrent weekly gemcitabine and radiotherapy for locally advanced pancreatic cancer. Anticancer Res 2006�G26�F3755-3759.
8�jMahadevan A, Miksad R, Goldstein M, et al. Induction gemcitabine and stereotactic body radiotherapy for locally advanced nonmetastatic pancreas cancer. Int J Radiat Oncol Biol Phys 2011�G81�Fe615-622.
9�jAbelson JA, Murphy JD, Minn AY, et al. Intensity-modulated radiotherapy for pancreatic adenocarcinoma. Int J Radiat Oncol Biol Phys 2012�G82�Fe595-601.
- CQ 4-4
- �Ǐ��i�s�؏��s�\�X���ɑ��C���w���ː��Ö@�O�̓������w�Ö@�̈Ӌ`�͂��邩�H
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ����w���ː��Ö@�O�ɓ������w�Ö@���s�����ƂŁC�������w���ː��Ö@���{�s���郁���b�g�̍����Ǘ�Q���I�ʂ���C�I�ʗ�ł͗ǍD�Ȏ��Ð��т�����Ă���_����Ӌ`������C���ÑI�����Ƃ��čl������Ă��悢�i�O���[�hC1�j�B |
|---|
�� �G�r�f���X
�Ǐ��i�s�؏��s�\�X���ɑ��āC���w���ː��Ö@���W�����ÁiCQ4-1�j�Ƃ��Đ�������Ă��邪�C�����ɉ��u�]�ڂ���Ǘ�͏��Ȃ��Ȃ��B���w���ː��Ö@�O�ɓ������w�Ö@���{�s����ړI�Ƃ��āC���w���ː��Ö@�̃����b�g�₷���Ǘ�̑I�ʁC���ݓI�ȉ��u�]�ڂ̗}���Ȃǂ�����B���w���ː��Ö@�O�̓������w�Ö@���Ǐ��i�s�؏��s�\�X���ɑ��ėL���Ȏ��Ö@�ł��邩�ǂ����̃G�r�f���X�����������B
����܂��X���ɑ��鉻�w���ː��Ö@�O�̓������w�Ö@�͑̕�Ⅰ�CⅡ�������Ɍ����Ă���C�����_������r�����ɂ���Ē����������Ȃǂ��r�E���������̂͂Ȃ��B �����̑�Ⅱ�������ŁC�������w�Ö@�ɂ����ݓI�ȉ��u�]�ڗႪ3�`33���I�ʂł��C�S�������Ԃ�10�`19 �J���ƁC��r�I�ǍD�Ȑ��т������Ă��� 1-9�j�i���x��Ⅲ�j�B�Ǐ��i�s�؏��s�\�X���ɑ��ăQ���V�^�r�����_����S-1 �ɂ�铱�����w�Ö@��C�Q���V�^�r�����_����p�����������w���ː��Ö@���{�s�����킪���ōs��ꂽ��Ⅱ�������ł́C�S��������14.4 �J���ƕ���Ă��� 6�j�i���x��Ⅲ�j�B�܂��Cborderline resectable ���܂ދǏ��i�s�X���ɑ��Q���V�^�r�����_���ƃV�X�v���`���ɂ�铱�����w�Ö@��C�������w���ː��Ö@���{�s������Ⅱ�������ł́C�S��������13 �J���ƕ���Ă��� 9�j�i���x��Ⅲ�j �B�������ΏۂƂ��������������ł́C�Q���V�^�r�����_���𒆐S�Ƃ���3 �J���Ԃ̓������w�Ö@�ɂ��29�����߂���ݓI�ȉ��u�]�ڗ��I�ʂ��邱�Ƃ��ł��C�܂��C�������w�Ö@��̓������w���ː��Ö@�{�s��́C�S��������15.0 �J���ƁC���w�Ö@�p�����11.7 �J���Ɣ�r���L�ӂɗǍD�Ȑ��т������Ă��� 10�j�i���x��Ⅳa�j�B
�ȏ�̂悤�ɁC��Ⅱ������������������̌��ʂ���C�������w�Ö@�ɂ�蓯�����w���ː��Ö@�������郁���b�g�̍����Ǘ�Q��I�ʂ�����\������������C�܂��I�ʂ��ꂽ�Ǘ�͓������w���ː��Ö@�ɂ���r�I�ǍD�Ȑ��т������Ă���B�������Ȃ���C��K�͂ȃ����_������r�����͂Ȃ��C���i�K�Ŗ{���Â̐����x��C1 �Ɣ��肷��B
�� �����ւ̒�
�Ǐ��i�s�؏��s�\�X���ɂ����ē������w�Ö@���s�����ƂŁC���ݓI�ȉ��u�]�ڂ�L����Ǘ��I�ʂ��C�������w���ː��Ö@�ɓK����Ǘ�Q��I�ʂ����郁���b�g������B���݁C�t�����X��Groupe Cooperateur Multidisciplinaire en Oncologie�iGERCOR�j�ɂ����āC�������w�Ö@��ɁC���w�Ö@�Q�Ɖ��w���ː��Ö@�Q�Ɋ���t���鍑�ۋ��������_������r�������i�s���ł���C���̌��ʂ����ڂ���Ă��� 10�j�B����C�����_������r�����̒~�ςȂǂɂ��C�������w���ː��Ö@�O�ɓ������w�Ö@���s�����ƂŎ��Ð��т����シ�邩�ۂ��𖾂炩�ɂ��Ă����K�v������B
�� ���p����
1�j Schneider BJ, Ben-Josef E, McGinn CJ, et al. Capecitabine and radiation therapy preceded and followed by combination chemotherapy in advanced pancreatic cancer. Int J Radiat Oncol Biol Phys 2005�G63�F1325-1330.
2�j Mishra G, Butler J, Ho C, et al. Phase Ⅱ�Gtrial of induction gemcitabine/CPT-11 followed by a twice-weekly infusion of gemcitabine and concurrent external beam radiation for the treatment of locally advanced pancreatic cancer. Am J Clin Oncol 2005�G28�F345-350.
3�j Ko AH, Quivey JM, Venook AP, et al. A phaseⅡstudy of fixed-dose rate gemcitabine plus low-dose cisplatin followed by consolidative chemoradiation for locally advanced pancreatic cancer. Int J Radiat Oncol Biol Phys 2007�G68�F809-816.
4�j Moureau-Zabotto L, Phélip JM, Afchain P, et al. Concomitant administration of weekly oxaliplatin, fluorouracil continuous infusion, and radiotherapy after 2 months of gemcitabine and oxaliplatin induction in patients with locally advanced pancreatic cancer�Fa Groupe Coordinateur Multidisciplinaire en Oncologie phaseⅡstudy. J Clin Oncol 2008�G26�F1080-1085.
5�j Kurt E, Kurt M, Kanat O, et al. Phase Ⅱstudy of induction chemotherapy with gemcitabine plus 5-fluorouracil followed by gemcitabine-based concurrent chemoradiotherapy for unresectable locally advanced pancreatic cancer. Tumori 2006�G92�F481-486.
6�j Nakachi K, Furuse J, Kinoshita T, et al. A phaseⅡstudy of induction chemotherapy with gemcitabine plus S-1 followed by chemoradiotherapy for locally advanced pancreatic cancer. Cancer Chemother Pharmacol 2010�G66�F527-534.
7�j Crane CH, Varadhachary GR, Yordy JS, et al. PhaseⅡtrial of cetuximab, gemcitabine, and oxaliplatin followed by chemoradiation with cetuximab for locally advanced�iT4�jpancreatic adenocarcinoma�Fcorrelation of Smad4�iDpc4�jimmunostaining with pattern of disease progression. J Clin Oncol 2011�G29�F3037-3043.
8�j Ch�fang HJ, Lin YL, Wang HP, et al. Induction chemotherapy with gemcitabine, oxaliplatin, and 5-fluorouracil/leucovorin followed by concomitant chemoradiotherapy in patients with locally advanced pancreatic cancer�Fa Taiwan cooperative oncology group Phase Ⅱ�Gstudy. Int J Radiat Oncol Biol Phys 2011�G81�Fe749-757.
9�j Marti JL, Hochster HS, Hiotis SP, et al. Phase�T/Ⅱtrial of induction chemotherapy followed by concurrent chemoradiotherapy and surgery for locoregionally advanced pancreatic cancer. Ann Surg Oncol 2008�G15�F3521-3531.
10�j Huguet F, André�GT, Hammel P, et al. Impact of chemoradiotherapy after disease control with chemotherapy in locally advanced pancreatic adenocarcinoma in GERCOR Phase Ⅱ�Gand Ⅲ�Gstudies. J Clin Oncol. 2007�G25�F326-331.
CQ 4-5�@�Ǐ��i�s�؏��s�\�X���ɑ��p�����ː��Ö@�̌��ʂ͂��邩�H
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ��p�����ː��Ö@�̗L�p�����x������͂��邪�C���ꂪ�\������P�����邩�ۂ��ɂ��ẲȊw�I�����͏\���ł͂Ȃ��i�O���[�hC1�j |
|---|
�� �G�r�f���X
�Ǐ��i�s�؏��s�\�X���ɑ���p�����ː��Ö@�́C�X���̊O�Ǝ˗Ö@�Ŗ��ƂȂ鏬���Ȃǂ̕��ː����̍����X���͂̐���g�D���J�����ɏƎ˖�O�ɑޔ������C1 ��ɑ���ʂ̓d�q����a�����邢�͐؏���̎�ᇏ��ɑ��ďƎ˂��鎡�Ö@�ł���B�C�O�ɂ����Ă͕��ː����ʌ��f����p���ɕa���Ɏh�����鎎�݂��s���Ă��� 1�j�i���x��Ⅳb�j�B
�Ǐ��i�s�؏��s�\�X���̎��ÂƂ��ẮC�p�����ː��Ö@�C�O�Ǝ˗Ö@�C���w�Ö@�i�S�g���^�C�����Ö@�j��3 ��ނ̎��Ö@���P�Ƃ܂��͑g�ݍ��킹�ėp�����Ă���B����ŁC���ꂼ��̗L�p���ڔ�r���邽�߂̗Տ������͍s���Ă��炸�C�W�����ÂɊւ��ẴR���Z���T�X�͌`������Ă��Ȃ��B
�p�����ː��Ö@�̏��Ɍ��ʂ̌����ł́C�p�����ː��Ö@�P�Ƃ܂��͊O�Ǝ˗Ö@�C���w�Ö@�Ƃ̕��p�ŁC50�`95�����x�̗L����������Ă��� 2-6�j�i���x��Ⅳb�j�C�p�����ː��Ö@��{�s��Ɣ�r���ď��ɗ��������Ƃ��������� 2�j�B
�p�����ː��Ö@�ɂ�鉄�����ʂɊւ��ẮC���Ɍ��ʂƓ��l�ɁC�p�����ː��Ö@�P�� 6�j�C�܂��͏p�����ː��Ö@�ƊO�Ǝ˗Ö@�� 5�j�C�ۑ��Ö@�ɔ�ׂĉ������ʂ����� 5, 6�j�C�p�����ː��Ö@��{�s��ɔ�ׂāC�����������\�ł���Ƃ���͂��� 1, 7�j�i���x��Ⅳb�j�B�������C�p�����ː��Ö@��{�s��̓����l�ł���C�O�Ǝ˗Ö@�}���w�Ö@�ȂǂƔ�r���āC���D�ꂽ�������ʂ����邩�ǂ����͕s���ł���B�܂��p���Ǝˁi�}�p��Ǝˁj�ɂ��Ǐ��̌��ʂɂ��Ă͕]��������ł͂��邪�C�U�������̕Ȃǂ��琄�����邱�Ƃ��\�ł��� 8�j�i���x��Ⅳb�j�B
�W�����ÂƂ��Ă̏p�����ː��Ö@�̈Ӌ`�͕s���Ȃ��̂́C�p�����ː��Ö@�ƊO�Ǝ˗Ö@�C�t���I���E���V����g�ݍ��킹���W�w���ẤC��Ⅰ���Տ������ŗǍD�Ȏ��Ð��тƈ��S��������Ă��� 9, 10�j�i���x��Ⅲ�j�B�p�����ː��Ö@���{�s����ۂɂ͊O�Ǝ˗Ö@�≻�w�Ö@�p���邱�Ƃɂ��C�������Ԃ̉����������邱�� 4, 11�j�i���x��Ⅳb�j�C�d�q���Ǝ˂͏��������Â�蕛��p�����Ȃ��C�������Ԃ��������� 1�j�Ȃǂ�����Ă���C�������Ԃ̉�����ړI�Ƃ���ۂɂ͊O�Ǝ˗Ö@�≻�w�Ö@�p���ׂ��ł���Ƃ����R���Z���T�X�͌`������Ă���B�܂��C�킪���̃����_������r�����ŏp�����ː��Ö@�ɒ�_�f�זE���ː������܂̃h���j�_�]�[���p���邱�ƂŗL�ӂȐ������Ԃ̉����������Ă��� 12�j�i���x��Ⅱ�j�B
���̂悤�ɏp�����ː��Ö@�͋Ǐ��i�s�؏��s�\�X���ɑ����̌��ʂ����邱�Ƃ͖��炩�ł��邪�C�W���I�ɏp�����ː��Ö@��p����ׂ����ǂ����������_�Ō��肷�邱�Ƃ͍���ł���B�܂��C�Ǐ��i�s�؏��s�\�X���̎������C�̓]�ڂȂNjǏ��ȊO�̕a�ς�����ł��邱�Ƃ��������Ƃ��C�p�����ː��Ö@�̉������ʂ��ؖ�����ɂ����v���ɂȂ��Ă���Ǝv����B�������Ȃ���C�����I�l�@�Ƃ͕ʂɁC�Ǐ��i�s�؏��s�\�X���Ńo�C�p�X��p���{�s����ۂɂ́C�p�����ː��Ö@��p���邱�Ƃɂ��1 ��ő���ʂ��Ǝ˂��邱�Ƃ��\�ŁC�o�C�p�X��p��̊O�Ǝ˗Ö@�̊��ԁC���@���Ԃ�Z�k�ł���Ƃ����Տ��I�ȗ��_�����邽�߁C���{�\�Ȏ{�݂ōs�����Ƃ͑Ó��ł���ƍl������B���̍ہC������ړI�Ƃ���̂ł���ΊO�Ǝ˗Ö@�≻�w�Ö@�Ƃ̕��p���]�܂����B
�ȏ���C�Ǐ��i�s�؏��s�\�X���ɑ��p�����ː��Ö@�̗L�p�����x������͂�����̂́C��K�͂ȃ����_������r�����͂Ȃ��C���i�K�Ŗ{���Â̐����x��C1 �Ɣ��肷��B
�� �����ւ̒�
�G�r�f���X�͒Ⴂ���̂́C�Ǐ��i�s�؏��s�\�X���Ńo�C�p�X��p���{�s����ۂɂ́C�p�����ː��Ö@��p���邱�Ƃɂ��1 ��ő���ʁi20�`25Gy ���x�j���Ǝ˂��邱�Ƃ��\�ƂȂ�C����Ɉ��������Ă̊O�Ǝ˗Ö@�̊��Ԃ���@���Ԃ�Z�k�ł���Ƃ����Տ��I�ȗ��_������B�܂��O�Ǝ˂ɂ�鉻�w���ː��Ö@�i40�`50Gy ���x�j�ɏp�����ː��Ö@��lj����C���ː��̑����ʂ���ᇂ̍����\�ƍl��������ʃ��x���ɂ܂ō��߂邱�Ƃɂ�蒷�������̉\�����J�����Ƃ����_������C���{�\�Ȏ{�݂Ŗ{���Ö@���s�����Ƃ͑I�����̂ЂƂƎv����B
�� ���p����
1�j Schuricht AL, Spitz F, Barbot D, et al. Intraoperative radiotherapy in the combined-modality management of pancreatic cancer. Am Surg 1998�G64�F1043-1049.
2�j �����N�v�C�ɓ��_�C������Y�C���D�X���ɑ���p���Ǝ˗Ö@�̐��тƍ����ǁD�����O�2001�G34�F459-464�D
3�j ���{�ĕ��C�ߓc�k��C�c���ǖ��C���D�؏��s�\�X���ɑ���p���Ǝ˂Əp�㌴�̏Ǝ˂̕��p�Ö@-����1 �N�ȏ㐶��13 ��̌���-�D�����O� 1992�G25�F1020-1026.
4�j Okamoto A, Matsumoto G, Tsuruta K, et al. Intraoperative radiation therapy for pancreatic adenocarcinoma�Fthe Komagome hospital experience. Pancreas 2004�G28�F296-300.
5�j Shibamoto Y, MaNabe T, Baba N, et al. High dose, external beam and intraoperative radiotherapy in the treatment of resectable and unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 1990�G19�F605-611.
6�j Miyamatsu A, Morinaga S, Yukawa N, et al. Intraoperative radiation therapy�iIORT�jfor locally unresectable pancreatic cancer. Gan To Kagaku Ryoho 1999�G26�F1846-1848�m. Article in Japanese�n
7�j �]��V��C���R�����C�������ՁC���D�y���Ǐ��Ö@������z�p�㉓�u���т���݂��X�̔������ɑ���p�����ː��Ö@�̌��ʂƈӋ`�D���Ɖ��� 1997�G24�F1687-1690�D
8�j Hoekstra HJ, Restrepo C, Kinsella TJ, et al. Histopathological effects of intraoperative radiotherapy on pancreas and adjacent tissues�Fa postmortem analysis. J Surg Oncol 1988�G37�F104-108.
9�j Furuse J, Kinoshita T, Kawashima M, et al. Intraoperative and conformal external-beam radiation therapy with protracted 5-fluorouracil infusion in patients with locally advanced pancreatic carcinoma. Cancer 2003�G97�F1346-1352.
10�j Tepper JE, Noyes D, Krall JM, et al. Intraoperative radiation therapy of pancreatic carcinoma�Fa report of RTOG-8505. Radiation Therapy Oncology Group. Int J Radiat Oncol Biol Phys 1991�G21�F1145-1149.
11�j Ogawa K, Karasawa K, Ito Y, et al. Intraoperative radiotherapy for unresectable pancreatic cancer�Fa multi-institutional retrospective analysis of 144 patients. Int J Radiat Oncol Biol Phys. 2011�G80�F111-118.
12�j Karasawa K, Sunamura M, Okamoto A, et al. Efficacy of novel hypoxic cell sensitiser doranidazole in the treatment of locally advanced pancreatic cancer�Flong-term results of a placebo-controlled randomised study. Radiother Oncol. 2008�G87�F326-330.
CQ 4-6�@���ː��Ö@�͋Ǐ��i�s�؏��s�\�X����QOL �����P���邩�H
| ����
|
�Ǐ��i�s�؏��s�\�X����QOL ���P�ɂ́C���w���ː��Ö@�i�O���[�hB�j����ː��Ö@�i�O���[�hC1�j�����߂���B |
|---|
�� �G�r�f���X
���ː��Ö@�́C�����u�ɂȂǂ̋�ɂȏǏ�̌����Ö@�Ƃ��āC���܂��܂Ȉ�����ᇂɗp�����Ă���B�Ǐ��i�s�؏��s�\�X���ɂ����Ă��C���ː��Ö@��QOL ���P�ɗL�p���ǂ����C�������s�����B
- Best supportive care�iBSC�j
�t���I���E���V�����p���w���ː��Ö@�Q��BSC �Q�Ƃ��r�������K�͂ȃ����_������r�����̌��ʁC���w���ː��Ö@�Q�̐������Ԓ����l��Karnofsky performance scale �́CBSC �Q�Ɣ�חL�ӂɉ��P����C�݉@���Ԃɂ��L�Ӎ����Ȃ����Ƃ�����Ă��� 1�j�i���x��Ⅱ�j�B
- ���w�Ö@
- ���ː��Ö@
�O���Ǝ˒P�Ƃł́C70�`72Gy ��68���̏Ǘ�ɁC�܂�30Gy/10 ���75���̏Ǘ�ɁC���Ɍ��ʂ�����ꂽ�Ƃ̕����� 3�j�i���x��Ⅳb�j 4�j�i���x��Ⅴ�j�B�p���Ǝ˒P�Ƃł́C77�`81���̏��Ɍ��ʂ�����Ă��� 5, 6�j�i���x��Ⅳb�j�B�O���Ǝ˂Əp���Ǝ˂̕��p�ł́C57�`90���̏��Ɍ��ʂ�����Ă��� 7-10�j�i���x��Ⅳb�j�C�O���Ǝ˒P�Ƃ����C�O���Ǝ˂Əp���Ǝ˂p�����ق����C�ǍD�ȏ��Ɍ��ʂ�������Ƃ̕����� 2�j�i���x��Ⅲ�j�B
- ���w���ː��Ö@
�O�q�̒ʂ�C�t���I���E���V�����p���w���ː��Ö@��QOL ���P���ʂ́CBSC ���D��Ă���Ƃ̏��K�̓����_������r�����̌��ʂ����� 1�j�i���x��Ⅱ�j�B�t���I���E���V�����p���w���ː��Ö@�ł́C80���̏Ǘ�ɏ��Ɍ��ʂ�����ꂽ�Ƃ̕� 1�j�i���x��Ⅴ�j�C76���̏Ǘ�Œ��ɖs�v�ɂȂ����Ƃ̕����� 11�j�i���x��Ⅳb�j�B
�V�X�v���`���ƃt���I���E���V���p�������w���ː��Ö@�ł́C52�`78���̏��Ɍ��ʂ�����Ă��� 12�j�i���x��Ⅴ�j 13�j�i���x��Ⅳb�j�B
�Q���V�^�r�����_�����p���w���ː��Ö@�ƁC�t���I���E���V�����p���w���ː��Ö@���r���������_������r�����̌��ʁCQOL ���P���ʂɂ͗L�Ӎ��͂Ȃ������ƕ���Ă��� 14�j�i���x��Ⅱ�j�B
- ���_
�����̌��ʂ𑍍�����ƁC���w���ː��Ö@���{�s�\�ȏǗ�ł���CBSC �ɓO���邱�Ƃ͊��߂��Ȃ��B���ː��Ö@�ɂ��ẮC�����_������r�����ɂ��m�F�͍s���Ă��炸�C���K���ʂɂ��ẴG�r�f���X���Ȃ����C�O���Ǝ˂Əp���Ǝ˂̂����ꂩ��������҂̕��p�ɂ��C���Ɍ��ʂ����҂ł���B���w�Ö@�ł�������x�̏��Ɍ��ʂ͊��҂ł��邪�C�����_������r�����ɂ��m�F�͍s���Ă��Ȃ����̂́C���ː��P�ƗÖ@�܂��͉��w���ː��Ö@�̂ق����C�ǍD�ȏ��Ɍ��ʂ�����Ă���B���w���ː��Ö@�̏��Ɍ��ʂ́CBSC ���D��Ă��萄���ł��邪�C���ː��P�ƗÖ@���D��Ă���Ƃ̃G�r�f���X�͂Ȃ��B���w���ː��Ö@�ɂ����镹�p���w�Ö@�܂́C�Q���V�^�r�����_���ł��t���I���E���V���ł��CQOL ���P���ʂɍ��͂Ȃ��Ƃ����G�r�f���X������B
�� �����ւ̒�
���ː��Ö@���C�����u�ɂȂǂ̏Ǐ�ɘa�ɗL���Ȃ��Ƃ́C����f�Âł悭�o�������B���ː��Ö@�́C���ɖ�Ȃǂ̑ΏǗÖ@�Ƃ͈قȂ�C�Ǐ�̌����ƂȂ��ᇂ��̂��̂��k�������錴���Ö@�ł��邽�߁C�L���Ȃ���ɖ�����ʂȂ������~���邱�Ƃ��ł��C�o�ϓI�ȃ����b�g�����҂ł��鎡�Ö@�ł���B
QOL ���P�ړI�̊ɘa�I���ː��Ö@�ɂ����ẮC�Ǝ˖�ɗ\�h���݂���K�v�͂Ȃ��C�Ǐ�̐ӔC�a���Ɍ��ǂ����Ǝ˖�ł悢�B���ʕ����ɂ��Ă��C��{�I�ɂ͏Ǐɘa�ł�����x�ł悢���C���u�]�ڂ̂Ȃ��ꍇ�́C���Â��t�����C������x�̊��Ԑ����������ꍇ�̔ӊ��L�Q���ۂɂ��z�����C50.4Gy/28 ����/5.5 �T��50Gy/25 ����/5 �T�Ȃǂ̒ʏ핪���Ǝ˂��]�܂����B
����C���u�]�ڂȂǂŒ������������҂��������ꍇ�́C40Gy/20 ����/4�T��C30Gy/10 ����/2 �T�Ȃǂ̂悤�ɁC���҂����\��ɉ����Ď��Ê��Ԃ��Z�k�����B
������ɂ���C���w�Ö@�����p����ꍇ�́C�L�Q���ۂ���������邨���ꂪ���邽�߁C���Ê��Ԃ�Z�k�������ꍇ�ł��C�����ʂ�3Gy �̂悤�ɂ͏グ���ɁC�ʏ핪���Ǝ˂͈͓̔��ɂƂǂ߂�̂�����ł���B
�� ���p����
1�j Shinchi H, Takao S, Noma H, et al. Length and quality of survival after external-beam radiotherapy with concurrent continuous 5-fluorouracil infusion for locally unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 2002�G53�F146-150.
2�j �������s�C�������v�C�R�c�Z���C���D�؏��s�\�iStage Ⅳb�j�X���ɑ���p���Ǝ˗Ö@�iIORT�j�D���Ɖ��w�Ö@ 2002�G29�F2221-2223.
3�j Ceha HM, van Tienhoven G, Gouma DJ, et al. Feasibility and efficacy of high dose conformal radiotherapy for patients with locally advanced pancreatic carcinoma. Cancer 2000�G89�F2222-2229.
4�j Morganti AG, Trodella L, Valentini V, et al. Pain relief with short-term irradiation in locally advanced carcinoma of the pancreas. J Palliat Care 2003�G19�F258-262.
5�j ���쐳�I�C�����O�@�C�������ՁC���D�X���̏W�w�I���ÁD������O�� 1994�G17�F199-205.
6�j �������v�C�����h��Y�C���c�p�j�D�X���؏��s�\��ɑ���p���Ǝ˗Ö@�D�_���X 1994�G15�F139-144.
7�j Shibamoto Y, MaNabe T, Baba N, et al. High dose, external beam and intraoperative radiotherapyin the treatment of resectable and unresectable pancreatic cancer. Int J Radiat Oncol Biol Phys 1990�G19�F605-611.
8�j ���{�ĕ��C�ߓc�k��C�c���ǖ��C���D�؏��s�\�X���ɑ���p���Ǝ˂Əp�㌴�̏Ǝ˂̕��p�Ö@�F����1�N�ȏ㐶��13��̌����D���{������O�Ȋw��G�� 1992�G25�F1020-1026.
9�j Okamoto A, Tsuruta K, Isawa T, et al. Okamoto A, Tsuruta K, Isawa T, Kamisawa T, Tanaka Y, Onodera T. Intraoperative radiation therapy for pancreatic carcinoma. The choice of treatment modality. Int J Pancreatol 1994�G16�F157-164.
10�j Okamoto A, Matsumoto G, Tsuruta K, et al. Intraoperative radiation therapy for pancreatic adenocarcinoma�Fthe Komagome hospital experience. Pancreas 2004�G28�F296-300.
11�j Morganti AG, Valentini V, Macchia G, et al. 5-fluorouracil-based chemoradiation in unresectable pancreatic carcinoma�FPhase�T-Ⅱdose-escalation study. Int J Radiat Oncol Biol Phys 2004�G59�F1454-1460.
12�j Azria D, Ychou M, Jacot W, et al. Treatment of unresectable, locally advanced pancreatic adenocarcinoma with combined radiochemotherapy with 5-fluorouracil and cisplatin. Pancreas 2002�G25�F360-365.
13�j Kawakami H, Uno T, Isobe K, et al. Toxicities and effects of involved-field irradiation with concurrent cisplatin for unresectable carcinoma of the pancreas. Int J Radiat Oncol Biol Phys 2005�G62�F1357-1362.
14�j Heras P, Kritikos K, Hatzopoulos A, et al. Effect of combined treatment methods on quality of life in patients with pancreatic cancer. Am J Ther 2009�G16�F316-318.
CQ 4-7�@�X�����]�ڂɑ�����ː��Ö@�͗L�p���H
| ����
|
���]�ڂɂ���u�Ɋɘa�ɕ��ː��Ö@�͗L�p�ł���i�O���[�hA�j�B |
|---|
�� �G�r�f���X
������ᇂɂ�鍜�]�ڂ�30�`70���̊����҂ł݂��邪�C�X���ɂ�鍜�]�ڂ̏Ǘᐔ�͂ق��̌Ō`���ɔ�ׂ�Ə��Ȃ��C�X���Ǘ�̂Ȃ��ł�������5�`20�����x�Ƃ���� 1�j�i���x��Ⅴ�j�B�������Ȃ���C�ߔN�X�����Ґ����������Ă������Ƃ�C�X���ɑ���S�g�Ö@�̐i���ɔ����ė\�オ�������Ă������Ƃɂ��C���]�ڂ����ƂȂ�Ǘ�̑������\�z�����B
�]�ڐ�����ᇂɑ�����ː��Ö@�͎�ᇂ̍����ړI�Ƃ�����̂ł͂Ȃ��C�Z���Ԃ̊O�Ǝ˂ɂ��Ǐ���ɘa����ړI�ōs���C�����̌Ō`���ɂ����ėL������������Ă���B���]�ڂɂ��Ǐ�Ƃ��čł������̂��u�ɂł��邪�C���ː��Ö@���u�Ɋɘa���ʂ����L�͂Ȏ��Ö@�ł���C�ŋߍL���s����悤�ɂȂ��Ă����I�s�I�C�h�Ȃǂ̒��ɍ܂�r�X�t�H�X�t�H�l�[�g�ɂ��Ö@�ƕ��p���邱�Ƃ��ł���B�܂��C���ː��Ö@���u�Ɋɘa�����łȂ������Ö@�ƂȂ闘�_��L���邽�߁C���]�ڂɂ��U�������a�I���܂�Ґ������̗\�h�C���P�����҂����B���]�ڂɂ������u�ɂ��͂��߂Ƃ��鏔�Ǐ�ɑ���C���ː��Ö@�̖�������ѐ��ʂ╪�����@����������B
�u�Ɋɘa�Ɋւ��Ă̗L������75�`90���ƍ����C20Gy/5 �����C30Gy/10 �����C35Gy/14 �����Ƃ����������̕��@���L���ł��� 2-5�j�i���x��Ⅰ�j�B�œK�Ȑ��ʂ╪�����@�ɂ��Ă͂���܂Ń����_������r�������܂ޑ����̌����ɂ�茟������Ă���C�č��ł�Radiation Therapy Oncology Group�iRTOG�j�ɂ�鑽�{���������̌��ʂ���C30Gy/10 �����̏Ǝ˂��W���Ƃ���Ă��� 6, 7�j�i���x��Ⅱ�j�B����C���B�𒆐S��8Gy/1 ��Ǝ˖@�̗L�p��������C���𗦁C���S���𗦂Ƃ��ɕ����Ǝ˂ƍ����Ȃ����� 8�j�i���x��Ⅰ�j�B���^�A�i���V�X�ɂ��ƁC�u�Ɋɘa���ʂƐ��ʂƂ̊W�ɂ��āC�����𑝂₵�����̐��ʂ��Ǝ˂���ق������ʂ������Ǐ�ɘa���Ԃ������Ƃ�������邪 3�j�i���x��Ⅰ�j�C���炩�ȊW�݂͂��Ȃ��Ƃ�������� 5, 9�j�i���x��Ⅰ�j�B�������C1 ��Ǝ˂ƕ����Ǝ˂ł͑O�҂ɂ����ē��ꕔ�ʂւ̍ďƎ˗����������ƁC���ҊԂ̊��𗦂⊮�S���𗦂ɍ����݂��Ȃ����Ƃ͕����̃��^�A�i���V�X�ň�v���Ă��� 8-10�j�i���x��Ⅰ�j�B�X�����]�ڏǗ�ɍi�����u�Ɋɘa���ʂɂ��āC13 �Ǘ�18 ���ʂ̍��]�ڂɑ���ɘa�I���ː��Ö@�i20�`30Gy�C�����l30Gy�j�ɂ��92���ƍ������u�Ɋɘa������ꂽ���̂́C�������Ԓ����l��3 �J���i95��CI�F1�`6 �J���j�ƒZ���\��ł��������Ƃ�����Ă��� 11�j�i���x��Ⅴ�j�B�ȏ���C�u�Ɋɘa�Ɋւ��Ă͂ǂ̐��ʕ����ɂ����ː��Ö@���L���ȑI�����ł��邪�C�����\�オ���҂ł��Ȃ��Ǘ�ɂ����ẮC20Gy/5 ������8Gy/1 ��Ȃǂ̏������ɂ��Z���Ǝ˂��܂߂����ʕ������@���l�����Ă������Ƃ��]�܂��B
�a�I���܂Ɋւ��ẮC�d���Ŕ玿��50���ȏ�ɔj�݂��邩�n���a�ς�2.5cm �ȏ�̏ꍇ�ɂ̓��X�N�������C�\�h��ړI�Ƃ������Œ�ƕ��ː��Ö@���K���ƂȂ� 2�j�i���x��Ⅰ�j�B���^�A�i���V�X�ɂ���1 ��Ǝ˖@�ƕ����Ǝ˖@�ł͑O�҂ŕa�I���ܗ��������Ȃ�X�� 8-10�j�ɂ��邱�Ƃ�����Ă��邽�߁C�����Ǝ˂��]�܂������C���ȊO�̕a����\��Ȃǂ����Ă������I�ɔ��f���邱�Ƃ��K�v�ł���B
���]�ڑ��̐Ғ��ǂւ̐i�W�ɔ����Ґ������Ǐ�Ɋւ��ẮC���ː��Ö@�P�Ƃ����O�ȓI�ɓ]�ڎ�ᇂ�؏����p��Ǝ˂�������ق����L���ł��邱�Ƃ��č��̑��{���������ŕ���Ă��邪 12�j�i���x��Ⅱ�j�C���̌����ɂ��Ă͏Ǘᐔ�����Ȃ����Ƃ���ː��Ö@�P�Ƃ̐��т��������邱�ƂȂǂ̖��_���w�E����Ă��� 13�j�i���x��Ⅲ�j�B���n�Տ��ł͎�p�Ö@���I������邱�Ƃ͏��Ȃ��C�����ʃX�e���C�h�ƕ��ː��Ö@���p�����邱�Ƃ������B���ʕ����ɂ��Ă�1 ��Ǝ˂ƕ����Ǝ˂Ƃ̊ԂŐ_�o�Ǐ���P�⎡�Ì���s���ɍ��͂Ȃ����̂́C�����Ǝ˂̂ق����Ǝ˖���̎�ᇍĔR�����Ȃ��X�� 14�j�i���x��Ⅳb�j�ɂ��邱�Ƃ�����Ă���B������x�\�オ�����߂�ꍇ�ɂ͕����Ǝ˂��]�܂������C��͂葍���I�Ȕ��f���K�v�ł���B
�����̍��]�ڂɑ�����ː��Ö@�̗L�Q���ۂ́C�q�C�ȂNj}�����̌y���Ȃ��̂Ɍ���ꔭ���p�x���Ⴂ�Ƃ���Ă��� 8-10�j�B���ʂ���ѕ���p�̗��ʂ���l���Ă��C���҂�QOL ��ۂ����ŗD�ꂽ���Ö@�ł���Ƃ�����B
�� �����ւ̒�
���u�]�ڂ�L�����X�����Â̎�̂͑S�g���w�Ö@�ł��邪�C���]�ڂɔ����Ǐ��݉����Ă����Ǘ�ɑ��ĕ��ː��Ö@���L���ł��邱�Ƃ͂����Όo�������B�a�Ԃɉ����ăI�s�I�C�h��r�X�t�H�X�t�H�l�[�g�ȂǖÖ@���g�ݍ��킹�C���ː��Ö@���\�Ȏ{�݂ł͐ϋɓI�Ɏ{�s���邱�Ƃ����������B�S�g���w�Ö@���ł���ꍇ�͗L�Q���ۂ�����邽�ߏƎ˖��傫���������Ȃ����ƁC�Q���V�^�r�����_�����p�����Ă���ꍇ�͋����Ǝ˂Ƃ̕��p�͋֊��Ƃ���Ă��邱�Ƃɒ��ӂ��K�v�ł���B�܂��C���ː��Ö@�̈��Ƃ���Sr-89 �ɂ��A�C�\�g�[�v���Âɂ��č����ő��{�����I�[�v������ 15�j�i���x��Ⅲ�j���s���L�����������ꂽ���Ƃ��C2007 �N�����ی����ÂƂ��Ď{�s�\�ƂȂ����B�����}���������ȏǗ����җ\�オ���ɒZ���Ǘ�ł͓��^�������ׂ��ŁC���w�Ö@�p�����̏Ǘ�ł��T�d�ȓK�����f�����߂��邪�C�O�Ǝˎ��Â�����ȏꍇ�ȂǏǗ�ɂ���Ă͑I�����̂ЂƂɂȂ蓾��B�Ǐ��\��Ȃǂ��܂߂đ����I�ɔ��f���C�œK�Ȏ��Â���Ă������Ƃ��]�܂��B
�� ���p����
1�j Hatfield DR, DeLand FH, Maruyama Y. Skeletal metastases in pancreatic carcinoma�Fstudy by isotopic bone scanning. Oncology 1976�G33�F44-47.
2�j Anderson PR, Coia LR. Fractionation and outcomes with palliative radiation therapy. Semin Radiat Oncol 2000�G10�F191-199.
3�j Ratanatharathorn V, Powers WE, Moss WT, et al. Bone metastasis�Freview and critical analysis of random allocation trials of local field treatment. Int J Radiat Oncol Biol Phys 1999�G44�F1-18.
4�j Rose CM, Kagan AR. The final report of the expert panel for the radiation oncology bone metastasis work group of the American College of Radiology. Int J Radiat Oncol Biol Phys 1998�G40�F1117-1124.
5�j McQuay HJ, Collins SL, Carroll D, et al. Radiotherapy for the palliation of painful bone metastases. Cochrane Database Syst Rev 2000�GCD001793.
6�j Tong D, Gillick L, Hendrickson FR. The palliation of symptomatic osseous metastases�Ffinal results of the Study by the Radiation Therapy Oncology Group. Cancer 1982�G50�F893-899.
7�j Blitzer PH. Reanalysis of the RTOG study of the palliation of symptomatic osseous metastasis. Cancer 1985�G55�F1468-1472.
8�j Sze WM, Shelley MD, Held I, et al. Palliation of metastatic bone pain�Fsingle fraction versus multifraction radiotherapy--a systematic review of randomised trials. Clin Oncol�iR Coll Radiol�j. 2003�G15�F345-352.
9�j Wu JS, Wong R, Johnston M, et al. Meta-analysis of dose-fractionation radiotherapy trials for the palliation of painful bone metastases. Int J Radiat Oncol Biol Phys 2003�G55�F594-605.
10�j Chow E, Harris K, Fan G, et al. Palliative radiotherapy trials for bone metastases�Fa systematic review. J Clin Oncol 2007�G25�F1423-1436.
11�j Harada H, Nishimura T, Kamata M, et al. Radiotherapy for bone metastases from hepatocellular carcinoma and pancreas cancer. Gan To Kagaku Ryoho 2006�G33�F1061-1064�m. Article in Japanese�n
12�j Patchell RA, Tibbs PA, Regine WF, et al. Direct decompressive surgical resection in the treatment of spinal cord compression caused by metastatic cancer�Fa randomised trial. Lancet 2005�G366�F643-648.
13�j Rades D, Huttenlocher S, Dunst J, et al. Matched pair analysis comparing surgery followed by radiotherapy and radiotherapy alone for metastatic spinal cord compression. J Clin Oncol 2010�G28�F3597-3604.
14�j Rades D, Stalpers LJ, Veninga T, et al. Evaluation of five radiation schedules and prognostic factors for metastatic spinal cord compression. J Clin Oncol 2005�G23�F3366-3375.
15�j Nishio M, Sano M, Tamaki Y, et al. A multicenter study to determine the efficacy and safety of strontium�i89Sr�jchloride for palliation of painful bony metastases in cancer patients. Nihon Igaku Hoshasen Gakkai Zasshi 2005 Oct�G65�F399-410.�mArticle in Japanese�n
5 ���w�Ö@
CQ 5-1�@���u�]�ڂ�L�����X�����҂ɑ��ĉ��w�Ö@�͐�������邩�H
| ����
|
���u�]�ڂ�L�����X�����҂ɑ��ĉ��w�Ö@��best supportive care �ɔ�ח\������P���邱�Ƃ��琄�������i�O���[�hA�j |
|---|
�� �G�r�f���X
�؏��s�\�i�s�X�����҂ɑ��鉻�w�Ö@��best supportive care�iBSC�j�ɔ䂵���҂̐����\������P����B
50 �����C7,043 ��̐؏��s�\�i�s�X�����҂�Ώۂɍs��ꂽ���^�A�i���V�X�̌��ʁC���w�Ö@��BSC �ɔ䂵�C1 �N�������iOR�F0.37, 95��CI�F0.25 �` 0.57�Cp��0.00001�j�����P���� 1�j�i���x��Ⅰ�j�B�؏��s�\�i�s�X�����邢�͓]�ڐ��a�ς�L�����X�����҂�ΏۂƂ���43 �̃����_������r����5,365 ��̉�͂̌��ʁC9 �̌����Ńt���I���E���V�����g�p�������w�Ö@�̐����\���BSC�ɔ䂵���P���� 2�j�i���x��Ⅰ�j�B�Ǐ��i�s�؏��s�\�X�����邢�͓]�ڐ��a�ς�L�����X�����҂�ΏۂƂ���51 �̃����_������r����9,970 ��̉�͂̌��ʁC���w�Ö@��BSC �ɔ䂵�����������P�iHR�F0.64�C95��CI�F0.42�`0.98�j���� 3�j�i���x��Ⅰ�j�B
�� �����ւ̒�
���u�]�ڂ�L�����X�����҂ɑ��ĉ��w�Ö@�͐�������邪�CPS ���ቺ���C���w�Ö@���{�s�����Ȃ����҂��邢�͉��w�Ö@�s�����̊��҂ɑ��ẮC��t���܂ފɘa�P�A�`�[�������҂���ъ��҉Ƒ��ɏ\���������C���ӂ������ŁC�u�ɏ����C�h�{���ÁC�������ÁC�������Â��܂߂�BSC���s���K�v������B
�� ���p����
1�j Yip D, Karapetis C, Strickland A, et al. Chemotherapy and radiotherapy for inoperable advanced pancreatic cancer. Cochrane Database Syst Rev 2006�G19�FCD002093.
2�j Fung MC, Takayama S, Ishiguro H, et al. Chemotherapy for advanced or metastatic pancreatic cancer�Fanalysis of 43 randomized trials in 3 decades�i1974-2002�j. Gan To Kagaku Ryoho 2003�G30�F1101-1111.�mArticle in Japanese�n
3�j Sultana A, Smith CT, Cunningham D, et al. Meta-analyses of chemotherapy for locally advanced and metastatic pancreatic cancer. J Clin Oncol 2007�G25�F2607-2615.
- CQ 5-2-1
- ���u�]�ڂ�L�����X���ɑ��Đ��������ꎟ���w�Ö@�͉����H
| ����
|
���u�]�ڂ�L�����X���ɑ���ꎟ���w�Ö@�Ƃ��ẮCFOLFIRINOX �Ö@�C�܂��̓Q���V�^�r�����_���{�i�u�p�N���^�L�Z�����p�Ö@�����������i�O���[�hA�j�B�������C���w�Ö@�ɏ\���Ȍo���̂����t�̂��ƂŁC�S�g��ԁiPS�j�⍜���@�\�Ȃǂ��C�����̎��Ö@���K�Ɣ��f�����Ǘ��I�����Ď��{����B�����̎��Ö@���K�Ɣ��f����Ȃ��ꍇ�́C�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_���{�G�����`�j�u���_�����p���ÁC�܂���S-1 �P���Â����������i�O���[�hA�j�B |
|---|
�� �G�r�f���X
�؏��s�\�X����7-8 ���͉��u�]�ڂ�L���Ă���C�c���2-3 �����Ǐ��i�s��ł���B�X���ɑ��鉻�w�Ö@�̊J���́C�]���C�؏��s�\�X����ΏۂƂ��Đi�߂��Ă������C�ߔN�ł͉��u�]�ڗ�݂̂�ΏۂƂ���Տ�����������Ă���B����܂łɕ��ꂽ�Տ������̌��ʂ���C���u�]�ڂ�L�����X���ɑ��Đ��������ꎟ���w�Ö@�ɂ��Č��������B
- �Q���V�^�r�����_���P����
1997 �NBurris ���Karnofsky performance status�iKPS�j50-70���̏Ǘ��70���܂ސ؏��s�\�X������126 ��ɑ��ăQ���V�^�r�����_���ƃt���I���E���V���̑�Ⅲ���������s�����B�Q���V�^�r�����_���Q�̐������Ԓ����l��5.65 �J���Ńt���I���E���V���Q�i4.41 �J���j�ɔ䂵�L�Ӂip=0.0025�j�ɉ������C�Q���V�^�r�����_���Q��1 �N��������18%�Ńt���I���E���V���Q�i2%�j�ɔ䂵�L�ӂɗǍD�ł������B�Q���V�^�r�����_���Q�̖������������Ԓ����l��2.33 �J���ł���C�t���I���E���V���Q�i0.92�J���j�ɔ䂵�L�ӁiP=0.0025�j�ɉ����������Ƃ𖾂炩�ɂ����B����ɁC�Q���V�^�r�����_���Q�̏Ǐ�ɘa���ʂ�23.8���ŁC�t���I���E���V���Q�i4.8%�j�ɔ䂵�L�Ӂip=0.0022�j�Ɍ��ʂ��F�߂�ꂽ���Ƃ���1�j�i���x��Ⅱ�j�C�Q���V�^�r�����_���P�܂��؏��s�\�X�����҂ɑ�����I���Ƃ��Ĉʒu�Â���ꂽ�B
���̌�C�}�g���b�N�X���^���v���e�A�[�[�ł���}���}�X�^�b�g* 2�j�CBAY12-9566* 3�j�C�G�L�T�e�J��* 4�j�ƃQ���Q�V�^�r�����_���Ƃ��e�X��r�����III���������s��ꂽ�� 2-4�j�i���x��Ⅱ�j�C�����̎����ɂ����Ă��Q���V�^�r�����_���̐������Ԃ��L�ӂɉ������邢�͉�������X����������Ă���B
- �Q���V�^�r�����_�����x�[�X�Ƃ������p�Ö@�i�\6�j
�Q���V�^�r�����_���͎�X�̍R���܂ƕ��p����C�Q���V�^�r�����_���P�܂Ɣ�r��������Ă���5-23,25-30)�i���x��Ⅱ�j�B���̂����C�Q���V�^�r�����_���P�܂ɑ��Đ������Ԃɂ�����D�z���������ꂽ�̂́C�Q���V�^�r�����_���{�G�����`�j�u���_�����p�Ö@23)�i���x��Ⅱ�j�ƃQ���V�^�r�����_���{�i�u�p�N���^�L�Z��*���p�Ö@20)�i���x��Ⅱ�j��2 �̎��Ö@�݂̂ł������i��q�j�B
�����̎����ł͗L�ӂȉ������ʂ͎�����Ȃ��������C�����̎����̃��^�A�i���V�X�����{����Ă���B�Q���V�^�r�����_��+�v���`�i���܁i�I�L�T���v���`�����邢�̓V�X�v���`��*�j�̕��p�Ö@�ƃQ���V�^�r�����_���P�܂�pooled analysis �ł́C�������Ԃ�HR��0.81�ip = 0.031�j�ł���C���̂���PS=0 �̊��҂ɂ����Ă�HR�F0.72�ip = 0.063�j�ŁC���L�p�ł��������Ƃ����炩�ɂ��ꂽ32)�i���x��Ⅰ�j�B���̑��̃��^�A�i���V�X�ł�
- �Q���V�^�r�����_��+�R����܁i�J�y�V�^�r��*�C�t���I���E���V���C�v���`�i���܁C�C���m�e�J�����_���̂����ꂩ�j���p33)�i���x��Ⅰ�j
- �Q�Q���V�^�r�����_��+�J�y�V�^�r��*���p34)�i���x��Ⅰ�j
- �Q���V�^�r�����_��+�I�L�T���v���`�����p34)�i���x��Ⅰ�j
- �Q���V�^�r�����_��+�v���`�i���ܕ��p35, 36)�i���x��Ⅰ�j
- �Q���V�^�r�����_��+�t���I���E���V�����p35,37)�i���x��Ⅰ�j
�č��ł͊��̉Ƒ����C�����X���̉Ƒ���������]�ڕa�ς�L�����X�����҂Ƀv���`�i���܂��܂މ��w�Ö@���s���ƁC�X���̉Ƒ����̂Ȃ����҂ɔ䂵�L�ӂɐ������Ԃ���������Ƃ̕��Ȃ��ꂽ38)�i���x��Ⅳb�j�B�wNCCN �K�C�h���C���x�i2014 �N�Łj�ł���`���X���̉\��������]�ڕa�ς�L�����X�����҂ɑ��ăQ���V�^�r�����_���{�V�X�v���`��*�̕��p�̐����x���J�e�S���[2A �ɕύX����Ă���C�ꕔ�̈�`�q�ψق�L���銳�҂ɂ����ăV�X�v���`��*���p���Â��L�p�Ȏ��Â̂ЂƂƂ��ċ������Ă���B����C�킪���ɂ����Ă������Ă����K�v������ƍl������B
- �Q���V�^�r�����_���{�G�����`�j�u���_�����p�Ö@
�G�����`�j�u���_���͏�琬�����q��e�̂̃`���V���L�i�[�[��I��I�ɑj�Q���镪�q�W�I���Ö�ł���B�؏��s�\�X��569 ����ΏۂɁC�Q���V�^�r�����_���{�G�����`�j�u���_�����p�Q�C�Q���V�^�r�����_���P�܌Q��2�Q�ɕ�������Ⅲ������23)�i�\6�j�ł́C�Q���V�^�r�����_���{�G�����`�j�u���_�����p�Q�̐������Ԓ����l��6.2 �J���ŁC�Q���V�^�r�����_���P�܌Q�i5.9 �J���j���L�ӂɐ������Ԃ̉������F�߂�ꂽ�B����C�G�����`�j�u���_���ɂ͗L�Q���ۂƂ��Ĕ��]�Ȃǂ̔畆�Ǐ��p�x�ɕ���Ă���B���Ăł̃����_������d�ӌ���Ⅲ���Տ������ɂ�����282 �ᒆ203 ��i72���j�ɔ��]���F�߂��23)�i���x��Ⅱ�j�C�؏��s�\�X����ΏۂƂ����Q���V�^�r�����_���{�G�����`�j�u���_�����p�̍�����Ⅱ���Տ������ɂ����āC106 �ᒆ99 ��i93.4���j�ɔ��]���F�߂�ꂽ���C93.8%��grade2 �ȉ��ł�����39)�i���x��Ⅲ�j�B����C���]��grade 2 �ȏ�̌Q�̕��ϐ������ԁC1 �N��������grade 1 �ȉ��̌Q�ɔ䂵�L�ӂɗǍD�ł�����23)�B�Q���V�^�r�����_���{�G�����`�j�u���_�����p�Ö@�̉������ʂ͑傫���Ȃ��C�܂��L�Q���ۂ���������X����F�߂邱�Ƃ���C�Q���V�^�r�����_���P�ܗÖ@�����S�ɗ��킷��V���ȕW�����ÂƂ��ẴR���Z���T�X�͓����Ă��Ȃ��B�킪���ɂ����Ă��؏��s�\�X������107 ��ɑ��č�����Ⅱ���������s���C�Q���V�^�r�����_���{�G�����`�j�u���_�����p�Ö@�̐������Ԓ����l��9.23 �J���Ɣ�r�I�ǍD�ł���E�e���������ꂽ���߁C�킪���ł��ی��K�p�����F����Ă���39)�i���x��Ⅲ�j�B
- S-1�P����
�킪���ɂ�����S-1 �͎�X�̊��ɑ��ėp�����Ă��邪�C�X���ɑ��Ă����������Ⅱ�����������{����C�t������37.5���ŁC�������������Ԓ����l��3.7 �J���C�������Ԓ����l��9.2 �J���ł����� 40)�i���x��Ⅲ�j�B����ɁC���{����ё�p�̐؏��s�\�X���ɑ���Q���V�^�r�����_���{S-1 ���p�Ö@�iGS �Ö@�j�C�Q���V�^�r�����_���P�܁CS-1 �P�܂̑�Ⅲ�������iGEST �����j���s���C�Q���V�^�r�����_���P�܂�S-1 �P�܂̔�r�ł͐������Ԃ�HR ��0.96�C97.5��CI��0.78�`1.18 �ł���C�Q���V�^�r�����_���P�܂ɑ���S-1 �P�܂̔�������ꂽ�BQOL �̓Q���V�^�r�����_���P�܂�S-1 �P�܂ō����F�߂��Ȃ�����9)�i���x��Ⅱ�j�B
S-1 �P���Â̗L�Q���ۂƂ���GEST �����ł͐H�~�s�U�C�����C�������Ȃǂ̏�����Ǐ��p�x�ɔF�߂�Ă���C�܂��C�t�@�\��Q�̂��銳�҂ł͗L�Q���ۂ��o�₷�����Ƃ���T�d���^���]�܂��B
- �Q���V�^�r�����_���{S-1 ���p�Ö@�iGS �Ö@�j
�؏��s�\�X���ɑ��� �Q���V�^�r�����_���P�܂��邢��S-1 �P���Â̗L�p��������Ă������Ƃ���C�Q���V�^�r�����_���{S-1 ���p�Ö@�̗L�p���ɂ��Ă킪���Ō�������Ă���41)�i���x��Ⅲ�j42, 43)�i���x��Ⅱ�j�BGEST �����ł� �Q���V�^�r�����_���{S-1 ���p�Ö@�iGS �Ö@�j�C�Q���V�^�r�����_���P�܂̐������Ԓ����l�͂��ꂼ��10.1 �J���C8.8 �J���ŁCHR�F0.88 �ł���CGS �Ö@�̐������Ԃ̓Q���V�^�r�����_���P�܂Ɣ�r���ėL�ӂȉ��P�͔F�߂��Ȃ�����9)�i���x��Ⅱ�j�B
- �I�L�T���v���`���C�C���m�e�J�����_���C�t���I���E���V���C�z���i�[�g�J���V�E�����p�Ö@�iFOLFIRINOX �Ö@�j
PS0-1 �̉��u�]�ڂ�L�����X������324���ΏۂɃI�L�T���v���`���C�C���m�e�J�����_���C�t���I���E���V���C�z���i�[�g�J���V�E��*���p�Ö@(FOLFIRINOX �Ö@)�Q�C�Q���V�^�r�����_���P�܌Q�ɖ���ׂɕ������������BFOLFIRINOX �Ö@�̐������Ԃ�11.1 �J���C�Q���V�^�r�����_���P�܂�6.8 �J���ł���CHR��0.57(95��CI�F0.45�`0.73�Cp<0.001)��FOLFIRINOX �Ö@�ɂ����ėL�ӂȐ������Ԃ̉�����F�߂��BFOLFIRINOX �Ö@��grade 3 �ȏ�̗L�Q���ۂƂ��ẮC�D���������i45.7���j�C���M���D���������ǁi5.4���j�C���������i9.1���j�C�����i12.7���j�C�����_�o��Q�i9.0���j���C�Q���V�^�r�����_���P�܂�荂�p�x�ɏo�����Ă���31)�i���x��Ⅱ�j�B�킪���ł�FOLFIRINOX �Ö@�̑�Ⅱ���������s���C�������Ԓ����l10.7 �J���C�������������Ԓ����l5.6 �J���C�t����38.9���ƊC�O�̎����Ƒ��F�Ȃ����т�����Ă���44)�i���x��Ⅲ�j�C2013 �N12 ���Ɂu�����؏��s�\���X���v�ɑ�����F���擾�����B�������Cgrade 3 �ȏ�̔�����������44.4���C�D��������77.8���C���M���D����������22.2���Ƃ���ɋ����Ő�������Ă���_��C�����ɂ͌��i�ȓK�i����݂��������̗ǂ��X�����҂݂̂��o�^����Ă���_�ɗ��ӂ���K�v������B����āCFOLFIRINOX �Ö@�̓K���Ɋւ��ẮC�S�g��ԁiPS�j�C�N��C�����@�\�i�D�������C�������j�C���t�≺���̗L���ȂǏ\���ɍl�����C�K�Ɣ��f�����Ǘ��I�����Ď��{����B�C���m�e�J�����_���̑�ӂɊ֗^����UGT1A1 �̈�`�q���^�Ɋւ��Ă��C�C���m�e�J�����_���ɂ��d�Ăȕ���p�i���ɍD�����������j�����̉\���������Ȃ邽�߁C���O�Ɍ������ׂ��ł���B�܂��C�C���m�e�J�����_���͒_�`�r���^�̖�܂ł���C�_���̕ǂ�_�ǃX�e���g�g���u���ɂ��L�Q���ۂ����������\�������邽�߁C�X�������Ǘ��_�ǃX�e���g���u��ł͒��ӂ��K�v�ł���B���ÊJ�n����C�����}���C���M���D���������ǁC������Ő��i�����C�H�~�s�U�C���S�E�q�f�j�C�����_�o��Q�Ȃǂ̗L�Q���ۂɏ\�����ӂ��C�K���v���ɑΉ�����K�v������B
FOLFIRINOX �Ö@�́C���̋����Ő������O����C2014 �N�̖{�K�C�h���C���������ɂ͑��̎��Ö@�ƕ���ł̐����Ƃ��Ă������C�L�����̖ʂł̓Q���V�^�r�����_���P�܂�L�ӂɏ��鎡�Ö@�ł���C���F��̎��Տ��ł̌o�����~�ς�����邱�Ƃ���C���I���ł̐����Ƃ����B
*���F�{�M�ł͊����̂���L �݂̂̂̃��{�z���i�[�g�J���V�E���Ƃ��ĊJ������C�ی��K�p�ƂȂ��Ă���B
- �Q���V�^�r�����_���{�i�u�p�N���^�L�Z�����p�Ö@
�i�u�p�N���^�L�Z���̓A���u�~���Ƀp�N���^�L�Z�������������i�m���q���������܂ł���B���u�]�ڂ�L�����X������861 ���Ώۂɍs��ꂽ��Ⅲ�������̌��ʁC�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Q�̐������Ԓ����l��8.5 �J���C�Q���V�^�r�����_���P�܌Q��6.7 �J���ł���CHR ��0.72(95%CI:0.62~0.83�Cp<0.001)�Ɨ��Q�ԂɗL�ӂȍ���F�߂��B�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@��grade 3 �ȏ�̗L�Q���ۂ́C�Q���V�^�r�����_���P�܂ɔ�ׁC�D��������(38%)�C����������(31%)�C��J(17%)�C�����_�o��Q(17%)�C����(6%)�����p�x�ɏo�����Ă������C���� ����(13%)�C�n��(13%)�C���M���D����������(3%)�̕p�x�͓����x�ł����� 20)�i���x��Ⅱ�j�B�킪���ōs��ꂽ��Ⅰ/Ⅱ�������ł��C�t����44.1%�C�������������Ԓ����l5.6 �J���C�������Ԓ����l13.5 �J���ƗǍD�Ȑ��т�����Ă���Cgrade 3 �ȏ�̗L�Q���ۂƂ��Ĕ���������(52.9%)�ƍD��������(67.6%)���C�O�̎�����荂�p�x�ɂ݂�ꂽ���̂́C���M���D���������ǂ�2.9%�ƊC�O�����Ɠ��p�x�ł���C�E�e����������Ă��� 45)�i���x��Ⅲ�j�B���̌��ʂɂ��C2014 �N12 ���Ɂu�����؏��s�\���X���v�ɑ��Ė��F���擾���Ă���B
�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@�̃Q���V�^�r�����_���P�܂ɑ��鐶�����Ԃ�HR ��0.72(FOLFIRINOX �Ö@��0.57)�ł��������C������Ő��┭�M���D���������ǂ̓_����E�e����FOLFIRINOX �Ö@�ɗD��ƍl�����C�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@�͉��u�]�ڂ�L�����X�����҂ɑ���L�͂Ȏ��Ö@�̂ЂƂƈʒu�Â�����B�ȏ���C�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@��FOLFIRINOX �Ö@�Ɠ��l�ɑ��I���ł̐����Ƃ����B
| �� �N |
�R����� | ���Ґ� | �������Ԓ����l�i���j | �n�U�[�h�� (95%CI) | p �l |
|---|---|---|---|---|---|
| Burris 1�j 1997 |
GEM |
63 |
5.7 |
NA |
<0.01 |
| Berlin 5�j 2002 |
GEM |
162 |
5.4 |
NA |
0.09 |
| Riess 6�j 2005 |
GEM |
236 |
6.2 |
NA |
0.68 |
| Herrmann 7�j 2007 |
GEM |
159 |
7.2 |
NA |
0.23 |
| Cunningham 8�j 2009 |
GEM |
266 |
6.2 |
0.86 (0.72-1.02) |
0.08 |
| Ueno 9�j 2013 |
GEM |
277 |
8.8 |
||
S-1 |
280 |
9.7 |
0.96 (0.78-1.18) |
<0.01 |
|
GEM�{S-1 |
275 |
10.1 |
0.88 (0.71-1.08) |
0.15 |
|
| Colucci 10�j 2002 |
GEM |
54 |
4.6 |
NA |
0.48 |
| Heinemann 11�j 2006 |
GEM |
97 |
6.0 |
0.80 (NA) |
0.15 |
| Colucci 12�j 2010 |
GEM |
199 |
8.3 |
1.10 (0.89-1.35) |
0.38 |
| Louvet 14�j 2005 |
GEM |
156 |
7.1 |
0.83 (0.65-1.05) |
0.13 |
GEM(FDR)�{�I�L�T���v���`�� |
157 |
9.0 |
|||
| Poplin 15�j 2009 |
GEM |
275 |
4.9 |
||
GEM(FDR) |
277 |
6.2 |
0.83 (0.69-1.00) |
0.04 |
|
GEM(FDR)�{�I�L�T���v���`�� |
272 |
5.7 |
0.88 (0.73-1.05) |
0.22 |
|
| Rocha Lima 16�j 2004 |
GEM |
180 |
6.6 |
NA |
0.79 |
| Stathopoulos 17�j 2006 |
GEM |
70 |
6.5 |
NA |
0.97 |
| Abou-Alfa 18�j 2006 |
GEM |
174 |
6.2 |
NA |
0.52 |
| Oettle 19�j 2005 |
GEM |
282 |
6.3 |
0.98 (0.82-1.18) |
0.85 |
| Von Hoff 20�j 2013 |
GEM |
430 |
6.7 |
0.72 (0.62-0.83) |
<0.01 |
| Bramhall 21�j 2002 |
GEM |
119 |
5.4 |
0.99 (0.76-1.30) |
0.95 |
| Van Cutsem 22�j 2004 |
GEM |
347 |
6.0 |
1.03 (0.86-1.23) |
0.75 |
6.3 |
|||||
| Moore 23�j 2007 |
GEM |
284 |
5.9 |
0.82 (0.69-0.99) |
0.04 |
| Van Cutsem 24�j 2009 |
GEM�{�G�����`�j�u���_�� |
301 |
6.0 |
0.89 (0.74-1.07) |
0.21 |
| Kindler 25�j 2010 |
GEM |
300 |
5.9 |
1.04 (0.88-1.24) |
0.95 |
| Philip 26�j 2010 |
GEM |
371 |
5.9 |
1.06 (0.91-1.23) |
0.23 |
| Kindler 27�j 2011 |
GEM |
316 |
8.3 |
1.01 (0.79-1.30) |
0.54 |
| Gonçalves 28�j 2012 |
GEM |
52 |
9.2 |
1.27 (0.84-1.93) |
0.23 |
| Rougier 29�j 2013 |
GEM |
275 |
7.8 |
1.17 (0.92-1.47) |
0.20 |
| Reni 30�j 2005 |
GEM |
47 |
NA |
0.65 (0.43-0.99) |
0.047 |
| Conroy 31�j 2011 |
GEM |
171 |
6.8 |
0.57 (0.45-0.73) |
<0.01 |
GEM�F�Q���V�^�r�����_��, FDR�F�葬�Ò��@�ifixed dose rate infusion�j, GFF�F�Q���V�^�r�����_��+�t���I���E���V��+�z���i�[�g�J���V�E��, PEFG�F�Q���V�^�r�����_��+�V�X�v���`��*+�t���I���E���V��+�G�s���r�V��*, FOLFIRINOX�F�I�L�T���v���`��+�C���m�e�J�����_��+�t���I���E���V��+�z���i�[�g�J���V�E��
�� �����ւ̒�
���u�]�ڂ�L�����X���ɑ��Đ��������ꎟ���w�Ö@�Ƃ��āC�]���̃Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�CS-1 �P���Âɉ����C2013 �N12 ����FOLFIRINOX �Ö@�C2014 �N12 ���ɃQ���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@���ی����ڂ��ꂽ�B�X���f�ÃK�C�h���C���̐�����2013 �łł́u�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p���ÁC�܂���S-1 �P���Â����������i�O���[�hA�j�B�v�C�����łł́uFOLFIRINOX �Ö@�C�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p���ÁC�܂���S-1 �P���Â����������i�O���[�hA�j�B�������CFOLFIRINOX �Ö@�́C���w�Ö@�ɏ\���Ȍo���̂����t�̂��ƂŁC�S�g���(PS)�C�N��C�����@�\�C���t�E�����̗L���CUGT1A1 �̈�`�q���^�Ȃǂ��l�����C���{�ɍۂ��ẮC�ً}���ɂ��K�ȑΉ����ł���悤�C�L�Q���ۂɑ���\���Ȋώ@�ƑK�v�ł���B�v�C����̍ĉ����łł́uFOLFIRINOX �Ö@�C�܂��̓Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@�����������i�O���[�hA�j�B�������C���w�Ö@�ɏ\���Ȍo���̂����t�̂��ƂŁC�S�g���(PS)�⍜���@�\�Ȃǂ��C�����̎��Ö@���K�Ɣ��f�����Ǘ��I�����Ď��{����B �����̎��Ö@���K�Ɣ��f����Ȃ��ꍇ�́C�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p���ÁC�܂���S-1 �P���Â����������i�O���[�hA�j�B�v�ƕύX����C���ÑI�������L�������B����C�ǂ̎��Ö@���ǂ̂悤�Ȋ��҂ɓK�����ׂ����͏\���ɖ��炩�ɂ���Ă��炸�C����̗Տ��f�[�^�̒~�ς�O�����Տ������Ȃǂɂ�薾�m�ɂ���邱�Ƃ����҂������B
�� ���p����
1�j Burris HA 3rd, Moore MJ, Andersen J, et al. Improvements in survival and clinical benefit with gemcitabine as first-line therapy for patients with advanced pancreas cancer�Fa randomized trial. J Clin Oncol 1997�G15�F2403-2413.
2�j Bramhall SR, Rosemurgy A, Brown PD, et al�GMarimastat Pancreatic Cancer Study Group. Marimastat as first-line therapy for patients with unresectable pancreatic cancer�Fa randomized trial. J Clin Oncol 2001�G19�F3447-3455.
3�j Moore MJ, Hamm J, Dancey J, et al�GNational Cancer Institute of Canada Clinical Trials Group. Comparison of gemcitabine versus the matrix metalloproteinase inhibitor BAY 12-9566 in patients with advanced or metastatic adenocarcinoma of the pancreas�Fa Phase Ⅲ�Gtrial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 2003�G21�F3296-3302.
4�j Cheverton P, Friess H, Andras C, et al. Phase Ⅲ�Gresults of exatecan�iDX-8951f�jversus gemcitabine�iGem�jin chemotherapy-naïve patients with advanced pancreatic cancer�iAPC�j. J Clin Oncol 2004�G22�isuppl abstr 4005�j.
5�j Berlin JD, Catalano P, Thomas JP, et al. Phase Ⅲ�Gstudy of gemcitabine in combination with fluorouracil versus gemcitabine alone in patients with advanced pancreatic carcinoma�FEastern Cooperative Oncology Group Trial E2297. J Clin Oncol 2002�G20�F3270-3275.
6�j Riess H, Helm A, Niedergethmann M, et al. A randomised, prospective, multicenter, phase III trial of gemcitabine, 5-fluorouracil (5-FU), folinic acid vs. gemcitabine alone in patients with advanced pancreatic cancer. J Clin Oncol 2005�G23(16S)�F1092s(abstr 4009).
7�j Herrmann R, Bodoky G, Ruhstaller T, et al�GCentral European Cooperative Oncology Group. Gemcitabine plus capecitabine compared with gemcitabine alone in advanced pancreatic cancer�Fa randomized, multicenter, Phase Ⅲ�Gtrial of the Swiss Group for Clinical Cancer Research and the Central European Cooperative Oncology Group. J Clin Oncol 2007�G25�F2212-2217.
8�j Cunningham D, Chau I, Stocken DD, et al. Phase Ⅲ�Grandomized comparison of gemcitabine versus gemcitabine plus capecitabine in patients with advanced pancreatic cancer. J Clin Oncol 2009�G27�F5513-5518.
9�j Ueno H, Ioka T, Ikeda M, et al. Randomized Phase Ⅲ�Gstudy of gemcitabine plus S-1, S-1 alone, or gemcitabine alone in patients with locally advanced and metastatic pancreatic cancer in Japan and Taiwan�FGEST study. J Clin Oncol 2013�G31�F1640-1648.
10�j Colucci G, Giuliani F, Gebbia V, et al. Gemcitabine alone or with cisplatin for the treatment of patients with locally advanced and/or metastatic pancreatic carcinoma�Fa prospective, randomized Phase Ⅲ�Gstudy of the Gruppo Oncologia dell�fItalia Meridionale. Cancer 2002�G94�F902-910.
11�j Heinemann V, Quietzsch D, Gieseler F, et al. Randomized Phase Ⅲ�Gtrial of gemcitabine plus cisplatin compared with gemcitabine alone in advanced pancreatic cancer. J Clin Oncol 2006�G24�F3946-3952.
12�j Colucci G, Labianca R, Di Costanzo F, et al. Randomized phase III trial of gemcitabine plus cisplatin compared with singlecompared with single-agent gemcitabine as first-line treatment of patients with advanced pancreatic cancer�Fthe GIP-1 study. J Clin Oncol 2010�G28�F1645-1651.
13�j Chao Y, Wu CY, Wang JP, et al. A randomized controlled trial of gemcitabine plus cisplatin versus gemcitabine alone in the treatment of metastatic pancreatic cancer. Cancer Chemother Pharmacol 2013�G72�F637-642.
14�j Louvet C, Labianca R, Hammel P, et al�GGERCOR�GGISCAD. Gemcitabine in combination with oxaliplatin compared with gemcitabine alone in locally advanced or metastatic pancreatic cancer�Fresults of a GERCOR and GISCAD Phase Ⅲ�Gtrial. J Clin Oncol 2005�G23�F3509-3516.
15�j Poplin E, Feng Y, Berlin J, et al. Phase Ⅲ, randomized study of gemcitabine and oxaliplatin versus gemcitabine�ifixed-dose rate infusion�jcompared with gemcitabine�i30-minute infusion�jin patients with pancreatic carcinoma E6201�Fa trial of the Eastern Cooperative Oncology Group. J Clin Oncol 2009�G27�F3778-3785.
16�j Rocha Lima CM, Green MR, Rotche R, et al. Irinotecan plus gemcitabine results in no survival advantage compared with gemcitabine monotherapy in patients with locally advanced or metastatic pancreatic cancer despite increased tumor response rate. J Clin Oncol 2004�G22�F3776-3783.
17�j Stathopoulos GP, Syrigos K, Aravantinos G, et al. A multicenter Phase Ⅲ�Gtrial comparing irinotecan-gemcitabine�iIG�jwith gemcitabine�iG�jmonotherapy as first-line treatment in patients with locally advanced or metastatic pancreatic cancer. Br J Cancer 2006�G95�F587-592.
18�j Abou-Alfa GK, Letourneau R, Harker G, et al. Randomized Phase Ⅲ�Gstudy of exatecan and gemcitabine compared with gemcitabine alone in untreated advanced pancreatic cancer. J Clin Oncol 2006�G24�F4441-4447.
19�j Oettle H, Richards D, Ramanathan RK, et al. A Phase Ⅲ�Gtrial of pemetrexed plus gemcitabine versus gemcitabine in patients with unresectable or metastatic pancreatic cancer. Ann Oncol 2005�G16�F1639-1645.
20�j Von Hoff DD, Ervin T, Arena FP, et al. Increased survival in pancreatic cancer with nab-paclitaxel plus gemcitabine. N Engl J Med 2013�G369�F1691-1703.
21�j Bramhall SR, Schulz J, Nemunaitis J, et al. A double-blind placebo-controlled, randomised study comparing gemcitabine and marimastat with gemcitabine and placebo as first line therapy in patients with advanced pancreatic cancer. Br J Cancer 2002�G87�F161-167.
22�j Van Cutsem E, van de Velde H, Karasek P, et al. Phase Ⅲ�Gtrial of gemcitabine plus tipifarnib compared with gemcitabine plus placebo in advanced pancreatic cancer. J Clin Oncol 2004�G22�F1430-1438.
23�j Moore MJ, Goldstein D, Hamm J, et al�GNational Cancer Institute of Canada Clinical Trials Group. Erlotinib plus gemcitabine compared with gemcitabine alone in patients with advanced pancreatic cancer�Fa Phase Ⅲ�Gtrial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 2007�G25�F1960-1966.
24�j Van Cutsem E, Vervenne WL, Bennouna J, et al. Phase Ⅲ�Gtrial of bevacizumab in combination with gemcitabine and erlotinib in patients with metastatic pancreatic cancer. J Clin Oncol 2009�G27�F2231-2237.
25�j Kindler HL, Niedzwiecki D, Hollis D, et al. Gemcitabine plus bevacizumab compared with gemcitabine plus placebo in patients with advanced pancreatic cancer�FPhase Ⅲ�Gtrial of the Cancer and Leukemia Group B�iCALGB 80303�j. J Clin Oncol 2010�G28�F3617-3622.
26�j Philip PA, Benedetti J, Corless CL, et al. Phase Ⅲ�Gstudy comparing gemcitabine plus cetuximab versus gemcitabine in patients with advanced pancreatic adenocarcinoma�FSouthwest Oncology Group-directed intergroup trial S0205. J Clin Oncol 2010�G28�F3605-3610.
27�j Kindler HL, Ioka T, Richel DJ, et al. Axitinib plus gemcitabine versus placebo plus gemcitabine in patients with advanced pancreatic adenocarcinoma�Fa double-blind randomised phase 3 study. Lancet Oncol 2011�G12�F256-262.
28�j Gonçalves A, Gilabert M, François E, et al. BAYPAN study�Fa double-blind phase Ⅲ�Grandomized trial comparing gemcitabine plus sorafenib and gemcitabine plus placebo in patients with advanced pancreatic cancer. Ann Oncol 2012�G23�F2799-2805.
29�j Rougier P, Riess H, Manges R, et al. Randomised, placebo-controlled, double-blind, parallel-group phase III study evaluating aflibercept in patients receiving first-line treatment with gemcitabine for metastatic pancreatic cancer. Eur J Cancer 2013�G49�F2633-2642.
30�j Reni M, Cordio S, Milandri C, et al. Gemcitabine versus cisplatin, epirubicin, fluorouracil, and gemcitabine in advanced pancreatic cancer�Fa randomised controlled multicentre phase III trial. Lancet Oncol 2005�G6�F369-376.
31�j Conroy T, Desseigne F, Ychou M, et al�GGroupe Tumeurs Digestives of Unicancer�GPRODIGE Intergroup. FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer. N Engl J Med 2011�G364�F1817-1825.
32�j Heinemann V, Labianca R, Hinke A, et al. Increased survival using platinum analog combined with gemcitabine as compared to single-agent gemcitabine in advanced pancreatic cancer�Fpooled analysis of two randomized trials, the GERCOR/GISCAD intergroup study and a German multicenter study. Ann Oncol 2007�G18�F1652-1659.
33�j Sultana A, Smith CT, Cunningham D, et al. Meta-analyses of chemotherapy for locally advanced and metastatic pancreatic cancer. J Clin Oncol 2007�G25�F2607-2615.
34�j Xie DR, Yang Q, Chen DL, et al. Gemcitabine-based cytotoxic doublets chemotherapy for advanced pancreatic cancer�Fupdated subgroup meta-analyses of overall survival. Jpn J Clin Oncol 2010�G40�F432-441.
35�j Heinemann V, Boeck S, Hinke A, et al. Meta-analysis of randomized trials�Fevaluation of benefit from gemcitabine-based combination chemotherapy applied in advanced pancreatic cancer. BMC Cancer 2008�G8�F82.
36�j Bria E, Milella M, Gelibter A, et al. Gemcitabine-based combinations for inoperable pancreatic cancer�Fhave we made real progress�H A meta-analysis of 20 phase 3 trials. Cancer 2007�G110�F525-533.
37�j Sultana A, Ghaneh P, Cunningham D, et al. Gemcitabine based combination chemotherapy in advanced pancreatic cancer-indirect comparison. BMC Cancer 2008�G8�F192.
38�j Oliver GR, Sugar E, Laheru D, et al. Family history of cancer and sensitivity to platinum chemotherapy in pancreatic adenocarcinoma. ASCO Meeting Abstracts, 2010�F180.
39�j Okusaka T, Furuse J, Funakoshi A, et al. Phase Ⅱ�Gstudy of erlotinib plus gemcitabine in Japanese patients with unresectable pancreatic cancer. Cancer Sci 2011�G102�F425-431.
40�jO kusaka T, Funakoshi A, Furuse J, et al. A late Phase Ⅱ�Gstudy of S-1 for metastatic pancreatic cancer. Cancer Chemother Pharmacol 2008�G61�F615-621.
41�j Ueno H, Okusaka T, Furuse J, et al. Multicenter Phase Ⅱ�Gstudy of gemcitabine and S-1 combination therapy�iGS Therapy�jin patients with metastatic pancreatic cancer. Jpn J Clin Oncol 2011�G41�F953-958.
42�j Ozaka M, Matsumura Y, Ishii H, et al. Randomized Phase Ⅱ�Gstudy of gemcitabine and S-1 combination versus gemcitabine alone in the treatment of unresectable advanced pancreatic cancer�iJapan Clinical Cancer Research Organization PC-01 study�j. Cancer Chemother Pharmacol 2012 69�F1197-1204.
43�j Isayama H, Nakai Y, Sasaki T, et al�GGEMSAP study group. The final analysis of a multicenter randomized controlled trial of gemcitabine�iG�jalone versus gemcitabine and S-1 combination therapy�iGS�jin patients with unresectable advanced pancreatic cancer�iPC�j�FGEMSAP study. J Clin Oncol 2011�G29�F�isuppl abstr 4040�j.
44�j Okusaka T, Ikeda M, Fukutomi A, et al. Phase Ⅱ study of FOLFIRINOX for chemotherapy-naïve Japanese patients with metastatic pancreatic cancer. Cancer Sci. 2014 ; 105 : 1321-6.
45�j Kasuga A, Ueno H, Ikeda M, et al. Efficacy, safety and pharmacokinetics (PK) of weekly nab-paclitaxel (P) plus Gemcitabine (G) in Japanese patients (pts) with metastatic pancreatic cancer (MPC): phase Ⅰ/Ⅱ trial. APA/JPS 45th Anniversary Meeting (abstr 14200)
- CQ 5-2-2
- �Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���w�Ö@�͉���?
| ����
|
�Ǐ��i�s�؏��s�\�X���ɑ���ꎟ���w�Ö@�Ƃ��āC�Q���V�^�r�����_���P���ÁC�܂���S-1 �P���Â����������i�O���[�hA�j�B |
|---|
�� �G�r�f���X
CQ5-2-1 �q�ׂ��Ă���悤�ɁC�X���ɑ��鉻�w�Ö@�̊J���́C�]���C�؏��s�\�X����ΏۂƂ��Đi�߂��Ă����B���Ȃ킿�C�Ǐ��i�s�؏��s�\��Ɖ��u�]�ڗ�̗��҂��܂��ҏW�c���؏��s�\�X���Ƃ��ėՏ������ɓo�^����C���̗Տ������ɂ���ĉ������ʂ����������Ö@�́C�Ǐ��i�s�؏��s�\��Ɖ��u�]�ڗ�̗��҂ɑ���W�����Âƈʒu�Â����Ă����B
���̂悤�Ȍo�܂��{CQ�i�Ǐ��i�s�؏��s�\�X���j�Ɋւ���G�r�f���X�̑����́CCQ5-2-1 �ɋL�q����Ă��邽�߁C�����ł͂ł��邾���d���������āC����̂��镔���𒆐S�ɋL�q�������B
- �؏��s�\�X��(���u�]�ڗ���܂�)�ɑ����Ⅲ����������̃G�r�f���X
CQ5-2-1 �ɏڏq����Ă���悤�ɁC�؏��s�\�X���i���u�]�ڗ���܂ށj�ɑ����Ⅲ�������ɂ���ē��v�w�I�ɗD�z�����邢�͔���ؖ�����Ă��鉻�w�Ö@���W�����́C�Q���V�^�r�����_���P����1�j�C�Q���V�^�r�����_��+�G�����`�j�u���p�Ö@2�j�C S-1 �P����3�j�C�I�L�T���v���`���C�C���m�e�J�����_���C�t���I���E���V���C���{�z���i�[�g�J���V�E�����p�Ö@�iFOLFIRINOX �Ö@�j4�j�C�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@5�j��5 ���W�����ł���B���̂���FOLFIRINOX �Ö@�ƃQ���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@�ɂ��ẮC�����̗L�p������������Ⅲ�����������u�]�ڗ�̂݁i�Ǐ��i�s�؏��s�\����܂܂Ȃ��j��ΏۂƂ��Ď��{����Ă��邽�߁C�Ǐ��i�s�؏��s�\��ɑ��鐄���Ɋւ��Ă̓G�r�f���X���s�����Ă���B����C�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�CS-1 �P���Âɂ��Ă̑�Ⅲ�������ɂ́C�Ǐ��i�s�؏��s�\��Ɖ��u�]�ڗ�̗��҂��ΏۂƂ���Ă���C�{�K�C�h���C��2013 �N�łɂ����Ă͋Ǐ��i�s�؏��s�\�X���E���u�]�ڂ�L�����X���ɑ���ꎟ���w�Ö@�Ƃ��āC����3 ���W��������������Ă���B
�؏��s�\�X���ɑ��Ď��{���ꂽ��Ⅲ�������̂����C�Ǐ��i�s�؏��s�\��݂̂̐��сi�T�u�O���[�v��́j������Ă�����̂��\�P�Ɏ����B
�\1�@�؏��s�\�X���ɑ����Ⅲ�������ɂ�����Ǐ��i�s�X���݂̂̐��сi�T�u�O���[�v��́j ��
�N�R����� ���Ґ� �������Ԓ����l �n�U�[�h�� (95%CI) p �l Ueno 3�j
2012GEM
S-166
6812.7 ��
13.8 ��
0.84(0.57-1.12)
NAUeno 3�j
2012GEM
GEM+S-166
6812.7 ��
15.9 ��
0.67(0.46-0.99)
NAHeinemann 11�j
2006GEM
GEM�{�V�X�v���`��20
2010.4 ��
10.3 ��
NA
NALouvet 12�j
2005GEM
GEM�{�I�L�T���v���`��47
5010.3 ��
10.3 ��
NA
NARocha Lima 13�j
2004GEM
GEM�{�C���m�e�J��24
2711.7 ��
9.8 ��
NA
NAVan Cutsem 14�j
2004GEM
GEM�{�e�B�s�t�@�j�u80
82264 ��
335 ��
NA
0.2Bramhal 15�j
2002GEM
GEM�{�}���}�X�^�b�g32
36290 ��
266 ��
1.13(0.66-1.94)
0.67Moore 2�j
2007GEM
GEM�{�G�����`�j�u71
67NA
NA
0.94(0.63-1.39)
NAKindler 16�j
2011GEM
GEM�{�A�L�V�`�j�u73
7710.6 ��
9.5 ��
NA
NANA�Fnot applicapable
�����̒̕��ŁC�Q���V�^�r�����_��+S-1 ���p�Ö@���Ǐ��i�s�؏��s�\��ɂ����Ă͗B��ǍD�ȌX�����F�߂��Ă��邪�C���̌�̒ǐՒ����ł͗L�Ӎ��͏������Ă���6�j�B����C�i�s�X��(�Ǐ��i�s+���u�]��)�ɑ���3 �̃����_���������CGEST ����3�j�CJACCRO PC-01 �����i��Ⅱ�������j7�j�CGEMSAP �����i��Ⅱ�������j8�j����ɋǏ��i�s�X���T�u�O���[�v�ɑ���Q���V�^�r�����_��+S-1 ���p�Ö@�̗L�p����������ړI�ōs��ꂽ������͂��s��ꂽ�B���̌��ʁC�Q���V�^�r�����_���P�ƗÖ@�ɑ���Q���V�^�r�����_��+S-1 ���p�Ö@�̃n�U�[�h��i95%�M����ԁj��0.708�i0.527-0.951�j�ŗL�ӂɗǍD�ł���ƕ��ꂽ9�j�B�{�͓�����͂ł���C���̈ʒu�Â��m�ɂ��邽�߂ɁC�X�Ȃ錟�����K�v�ł���B
�Q���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�͑S�Ǘ�i�Ǐ��i�s�؏��s�\��Ɖ��u�]�ڗ�j�ɂ����Ă͐������Ԃɂ����ėL�Ӎ����F�߂�ꂽ���C�Ǐ��i�s�؏��s�\��݂̂̉�͂ɂ����Ă͗��Q�Ԃ̍��͂قƂ�ǂ݂��Ȃ�����2�j�B
FOLFIRINOX �Ö@����уQ���V�^�r�����_��+�i�u�p�N���^�L�Z���Ö@�͑O�q�̂悤�ɑ�Ⅲ�����������u�]�ڗ�݂̂�ΏۂƂ��Ď��{���ꂽ���߁C�Ǐ��i�s�X���ɑ��鎡�Ì��ʂ͏\���ɂ͖��炩�ɂ���Ă��Ȃ����̂́CNCCN �̃K�C�h���C���ł͋Ǐ��i�s�X���ɑ��鎡�ÑI�����Ƃ��ċ������Ă���B�킪���ł��u�؏��s�\�X���v�ɑ��ĕی��K�p���F�߂��Ă���C�Ǐ��i�s�X���ɓK�p���邱�Ƃ��\�ƂȂ��Ă���B����̗Տ��f�[�^�̒~�ς�O�����Տ������Ȃǂɂ��C�Ǐ��i�s�X���ɂ�����ʒu�Â��m�ɂ��Ă����K�v������B
- �Ǐ��i�s�؏��s�\�X���݂̂ɑ����Ⅲ����������̃G�r�f���X
2013 �N��ASCO �ɂ����ċǏ��i�s�؏��s�\�X���݂̂�ΏۂƂ�����Ⅲ�������ł���LAP 07 �����̌��ʂ����\���ꂽ10�j�B�{�����ł͋Ǐ��i�s�؏��s�\�X�����҂��C�Q���V�^�r�����_���P���ÌQ�ƃQ���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�Q�Ƀ����_���Ɋ���t����4 �����Ԃ̎��Â��s���iR1 �t�F�[�Y�j�C���̊Ԃ̕a���̃R���g���[�����\�ł��������҂�����ɉ��w�Ö@�p���i2 �����j�Q�Ɖ��w���ː��Ö@�Q�Ƀ����_���Ɋ���t���Ă���iR2 �t�F�[�Y)�BR2 �t�F�[�Y�̉��w�Ö@�܂��͉��w���ː��Ö@�I����́CR1 �t�F�[�Y�ŃQ���V�^�r�����_���P���Â����{���ꂽ���҂͖����Ìo�ߊώ@�Ƃ���CR1 �t�F�[�Y�ŃQ���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�����{���ꂽ���҂ɂ̓G�����`�j�u���_���݂̂��p������Ă���B�{�����̎�v�]�����ڂ́CR2 �t�F�[�Y�Ɉڍs�������҃O���[�v�ɂ����鐶�����ԂŁC���w���ː��Ö@�̗D�z�����������Ă��邪�C�����]�����ڂƂ��āC�G�����`�j�u���_���̐������Ԃɑ����悹���ʂ��������Ă���B���̌��ʁC�������Ԓ����l�̓Q���V�^�r�����_���P���ÌQ��13.6 �����C�Q���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@��11.9 �����ł���C�G�����`�j�u���_���̐������Ԃɑ����悹���ʂ͔F�߂�ꂸ�C�ނ���G�����`�j�u���_�����^�Q���s�ǂȌX���ł������iHR=1.19�Cp=0.09�j�B����ɁC�G�����`�j�u�ɂ͗L�Q���ۂƂ��Ĕ��]�Ȃǂ̔畆�Ǐ��p�x�ɕ���Ă��邵2�j�C�����z�Ŋ��҂ւ̌o�ϓI���S���傫���B
�O�Łi2013 �N�Łj�ɂ����Ă͋Ǐ��i�s�؏��s�\�X���E���u�]�ڂ�L�����X���ɑ���ꎟ���w�Ö@�Ƃ��āC�Q���V�^�r�����_���P���ÁC�Q���V�^�r�����_��+�G�����`�j�u���_�����p���ÁC�܂��� S-1 �P���Â� 3 ���W�����𐄏�(�O���[�hA)�Ƃ������C2013 �N12 ���Ɏ����؏��s�\�X���ɑ��鉻�w�Ö@�Ƃ���FOLFIRINOX �Ö@���ی����ڂ��ꂽ���Ƃ��ӂ܂���2014 �N7 ���̉����ł́C�Ǐ��i�s�؏��s�\�X���݂̂�ΏۂƂ��Ď��{���ꂽLAP 07 �����ɂ����āC�G�����`�j�u���_���̐������Ԃɑ����悹���ʂ��F�߂��Ȃ��������Ƃ���C�Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���w�Ö@�Ƃ��ăQ���V�^�r�����_��+�G�����`�j�u���_�����p�Ö@�͐������珜�O�����B����ɁCFOLFIRINOX �Ö@�͑�Ⅲ�����������u�]�ڂ�L�����X�����҂�Ώۂɍs���Ă���C�Ǐ��i�s�؏��s�\�X���ɑ���G�r�f���X���Ȃ��C�Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���w�Ö@�Ƃ��Ă̐������珜�O�����B
2014 �N12 ���Ɏ����؏��s�\�X���ɑ��鉻�w�Ö@�Ƃ��ăQ���V�^�r�����_��+�i�u�p�N���^�L�Z���Ö@���ی����ڂ��ꂽ���Ƃ��ӂ܂��C����ĉ������s�����B�Q���V�^�r�����_��+�i�u�p�N���^�L�Z���Ö@����Ⅲ�����������u�]�ڂ�L�����X�����҂�Ώۂɍs���Ă���C�Ǐ��i�s�؏��s�\�X���ɑ���G�r�f���X�͂Ȃ��C����̍ĉ����ł��C�Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���w�Ö@�Ƃ��Ă̐������珜�O�����B�܂��C�Q���V�^�r�����_��+S-1 ���p�Ö@�ɂ��ẮC������Ǐ�Ȃǂ̕���p����������\��������C���̗L�p���ɂ��Ă͂���Ȃ錟���K�v�ł���B
�� �����ւ̒�
FOLFIRINOX �Ö@�C�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@�͉��u�]�ڂ�L�����X�����҂�Ώۂɑ�Ⅲ���������s���Ă���C�Ǐ��i�s�؏��s�\�X���ɑ���G�r�f���X���Ȃ����Ƃ���C����̉����ł͋Ǐ��i�s�؏��s�\�X���ɑ��Đ��������ꎟ���w�Ö@�Ƃ��Ă̐������珜�O�����B�������C�����؏��s�\�X���ɑ��鉻�w�Ö@�Ƃ��Ċ��ɕی����ڂ���Ă���C����FOLFIRINOX �Ö@�C�Q���V�^�r�����_��+�i�u�p�N���^�L�Z�����p�Ö@���Ǐ��i�s�؏��s�\�X���ɑ��Ă��C���L���ŁC���S�Ȏ��Ö@�Ƃ��Ċm�����邱�Ƃ��]�܂��B
�� ���p����
1�j Burris HA 3rd, Moore MJ, Andersen J, Green MR, Rothenberg ML, Modiano MR, Cripps MC, Portenoy RK, Storniol AM, Tarassoff P, Nelson R, Dorr FA, Stephens CD, Von Hof DD. Improvements in survival and clinical benefit with gemcitabine as first-line therapy for patients with advanced pancreas cancer�Fa randomized trial.J Clin Oncol 1997�G15�F2403-13.
2�j Moore MJ, Goldstein D, Hamm J, Figer A, Hecht JR, Gallinger S, Au HJ, Murawa P, Walde D, Wolff RA, Campos D, Lim R, Ding K, Clark G, Voskoglou-Nomikos T, Ptasynski M, Parulekar W�GNational Cancer Institute of Canada Clinical Trials Group. Erlotinib plus gemcitabine compared with gemcitabine alone in patients with advanced pancreatic cancer�Fa phase III trial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 2007�G25�F1960-6.
3�j Ueno H, Ioka T, Ikeda M, Ohkawa S, Yanagimoto H, Boku N, Fukutomi A, Sugimori K, Baba H, Yamao K, Shimamura T, Sho M, Kitano M, Cheng AL, Mizumoto K, Chen JS, Furuse J, Funakoshi A, Hatori T, Yamaguchi T, Egawa S, Sato A, Ohashi Y, Okusaka T, Tanaka M. Randomized phase Ⅲ�Gstudy of gemcitabine plus S-1 (GS) versus S-1 versus gemcitabine (GEM) in unresectable advanced pancreatic cancer (PC) in Japan and Taiwan�FGEST study. J Clin Oncol, 2013�G31�F1640-8.
4�j Conroy T, Desseigne F, Ychou M, Bouché�GO, Guimbaud R, Bécouarn Y, Adenis A, Raoul JL, Gourgou-Bourgade S, de la Fouchardiére C, Bennouna J, Bachet JB, Khemissa-Akouz F, Péré-Vergé�GD, Delbaldo C, Assenat E, Chauffert B, Michel P, Montoto-Grillot C, Ducreux M�GGroupe Tumeurs Digestives of Unicancer�GPRODIGE Intergroup.FOLFIRINOX versus Gemcitabine for Metastatic Pancreatic Cancer. N Engl J Med. 2011�G364�F1817-25.
5�j Von Hoff DD, Ervin T, Arena FP, Chiorean EG, Infante J, Moore M, Seay T, Tjulandin SA, Ma WW, Saleh MN, Harris M, Reni M, Dowden S, Laheru D, Bahary N, Ramanathan RK, Tabernero J, Hidalgo M, Goldstein D, Van Cutsem E, Wei X, Iglesias J, Renschler MF. Increased survival in pancreatic cancer with nab-paclitaxel plus gemcitabine. N Engl J Med 2013�G369�F1691-1703.
6�j Fukutomi A, Okusaka T, Sugimori K, Ueno H, Ioka T, Ohkawa S, Boku N, Yamao K, Mizumoto K, Furuse J, Funakoshi A, Hatori T, Yamaguchi T, Egawa S, Sato A, Ohashi Y, Cheng A, Tanaka M. Updated results of the GEST study�FRandomized phase Ⅲ�Gstudy of gemcitabine plus S-1 (GS) versus S-1 versus gemcitabine (GEM) in unresectable advanced pancreatic cancer in Japan and Taiwan. J Clin Oncol 2012 30, (suppl�Gabstract 4035).
7�j OzakaM, Matsumura Y, Ishii H, Omuro Y, Itoi T, Mouri H, Hanada K, Kimura Y, Maetani I, Okabe Y, Tani M, Ikeda T, Hijioka S, Watanabe R, Ohoka S, Hirose Y, Suyama M, Egawa N, Sofuni A, Ikari T, Nakajima T.Randomized phase Ⅱ�Gstudy of gemcitabine and S-1 combination versus gemcitabine alone in the treatment of unresectable advanced pancreatic cancer (Japan Clinical Cancer Research Organization PC-01 study). Cancer Chemother Pharmacol. 2012 69�F1197-1204.
8�j Nakai Y, Isayama H, Sasaki T, Sasahira N, Tsujino T, Toda N, Kogure H, Matsubara S, Ito Y, Togawa O, Arizumi T, Hirano K, Tada M, Omata M, Koike K. A multicentre randomised phase Ⅱ�Gtrial of gemcitabine alone vs gemcitabine and S-1 combination therapy in advanced pancreatic cancer�FGEMSAP study. Br J Cancer 2012�G106�F1934-1939.
9�j Nakai Y, Okusaka T, Ikari T, Isayama H, Furuse J, Ishii H, Imai S, Okamura S, Hamada C. Analysis of prognostic factors in locally advanced and metastatic pancreatic cancer treated with gemcitabine or gemcitabine and S-1 chemotherapy using individual patient data from three randomized studies. J Clin Oncol 32, 2014 (suppl 3�Gabstr 223)
10�j Hammel P, Huguet F, Laethem, D JV, et al. Comparison of chemoradiotherapy (CRT) and chemotherapy (CT) in patients with a locally advanced pancreatic cancer (LAPC) controlled after 4 months of gemcitabine with or without erlotinib�FFinal results of the international phase Ⅲ�GLAP 07 study. J Clin Oncol 31, 2013 (suppl�Gabstr LBA4003)
11�j Heinemann V, Quietzsch D, Gieseler F, Gonnermann M, Schönekäs H, Rost A, Neuhaus H, Haag C, Clemens M, Heinrich B, Vehling-Kaiser U, Fuchs M, Fleckenstein D, Gesierich W, Uthgenannt D, Einsele H, Holstege A, Hinke A, Schalhorn A, Wilkowski R.Randomized phase Ⅲ�Gtrial of gemcitabine plus cisplatin compared with gemcitabine alone in advanced pancreatic cancer.J Clin Oncol. 2006�G24�F3946-52.
12�j Louvet C, Labianca R, Hammel P, Lledo G, Zampino MG, André T, Zaniboni A, Ducreux M, Aitini E, Taïeb J, Faroux R, Lepere C, de Gramont A�GGERCOR�GGISCAD. Gemcitabine in combination with oxaliplatin compared with gemcitabine alone in locally advanced or metastatic pancreatic cancer�Fresults of a GERCOR and GISCAD phase Ⅲ trial. J Clin Oncol. 2005�G23�F3509-16.
13�j Rocha Lima CM, Green MR, Rotche R, Miller WH Jr, Jeffrey GM, Cisar LA, Morganti A, Orlando N, Gruia G, Miller LL. Irinotecan plus gemcitabine results in no survival advantage compared with gemcitabine monotherapy in patients with locally advanced or metastatic pancreatic cancer despite increased tumor response rate. J Clin Oncol. 2004�G22�F3776-83.
14�j Van Cutsem E, van de Velde H, Karasek P, Oettle H, Vervenne WL, Szawlowski A, Schoffski P, Post S, Verslype C, Neumann H, Safran H, Humblet Y, Perez Ruixo J, Ma Y, Von Hoff D. Phase Ⅲ trial of gemcitabine plus tipifarnib compared with gemcitabine plus placebo in advanced pancreatic cancer. J Clin Oncol. 2004�G22:1430-8.
15�j Bramhall SR, Schulz J, Nemunaitis J, Brown PD, Baillet M, and Buckels JAC. A double-blind placebo-controlled, randomised study comparing gemcitabine and marimastat with gemcitabine and placebo as first line therapy in patients with advanced pancreatic cancer. Br J Cancer. 2002�G87�F161-7.
16�j Kindler HL, Ioka T, Richel DJ, Bennouna J, Létourneau R, Okusaka T, Funakoshi A, Furuse J, Park YS, Ohkawa S, Springett GM, Wasan HS, Trask PC, Bycott P, Ricart AD, Kim S, Van Cutsem E. Axitinib plus gemcitabine versus placebo plus gemcitabine in patients with advanced pancreatic adenocarcinoma�Fa double-blind randomised phase 3 study. Lancet Oncol. 2011�G12�F256-62.
CQ 5-3�@�؏��s�\�X���ɑ��Đ�������鉻�w�Ö@�̓��^���Ԃ͂ǂꂭ�炢���H
�����؏��s�\�X���ɑ��鉻�w�Ö@�́C���^�p������ȗL�Q���ۂ̔������Ȃ���C�a�Ԃ����炩�ɐi�s����܂œ��^���p������i�O���[�hB�j�B �� �G�r�f���X
���w�Ö@�͈�ʓI�ɂ͒����Ɍp�����邱�Ƃɂ��C�~�ϓŐ����o�����C���Ì��ʂ����シ��X�����F�߂���B�K�ȓ��^���Ԃ́C���^�����܂����ɂ��قȂ�ƍl�����Ă���B�؏��s�\�X���ɑ��鉻�w�Ö@�̓��^���Ԃɂ��Č��������C���w�Ö@�̓��^���Ԃ𖾂炩�ɂ��邱�Ƃ�ړI�Ƃ��������_���݂͂��Ȃ������B�����̓Q���V�^�r�����_���Ƃق��̎��Â��r������K�͂ȃ����_������r�����̕ł��邪�C����܂ł��ׂāC�a�Ԃ����炩�ɐi�s����܂ŁC�܂��͌p��������ȗL�Q���ۂ���������܂Ŏ��Â��p������C�L�p����������Ă��� 1-15, 19, 21, 23�j�i���x��Ⅱ�j16-18, 20, 22, 24�j�i���x��Ⅲ�j�B����āC�����_�ł͂����Ɠ��l�ȓ��^���Ԃ�ݒ肷�邱�Ƃ����������B
�� ���p����
1�j Burris HA 3rd, Moore MJ, Andersen J, et al. Improvements in survival and clinical benefit with gemcitabine as first-line therapy for patients with advanced pancreas cancer�Fa randomized trial. J Clin Oncol 1997�G15�F2403-2413.
2�j Bramhall SR, Rosemurgy A, Brown PD, et al�GMarimastat Pancreatic Cancer Study Group Marimastat as first-line therapy for patients with unresectable pancreatic cancer�Fa randomized trial. J Clin Oncol 2001�G19�F3447-3455.
3�j Moore MJ, Hamm J, Dancey J, et al. Comparison of gemcitabine versus the matrix metalloproteinase inhibitor BAY 12-9566 in patients with advanced or metastatic adenocarcinoma of the pancreas�Fa Phase Ⅲ�Gtrial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 2003�G21�F3296-3302.
4�j Gansauge F, Ramadani M, Pressmar J, et al. NSC-631570�iUkrain�jin the palliative treatment of pancreatic cancer. Results of a Phase Ⅱ�Gtrial. Langenbecks Arch Surg 2002�G386�F570-574.
5�j Berlin JD, Catalano P, Thomas JP, et al. Phase Ⅲ�Gstudy of gemcitabine in combination with fluorouracil versus gemcitabine alone in patients with advanced pancreatic carcinoma�FEastern Cooperative Oncology Group Trial E2297. J Clin Oncol 2002�G20�F3270-3275.
6�j Herrmann R, Bodoky G, Ruhstaller T, et al�GSwiss Group for Clinical Cancer Research�GCentral European Cooperative Oncology Group. Gemcitabine plus capecitabine compared with gemcitabine alone in advanced pancreatic cancer�Fa randomized, multicenter, Phase Ⅲ�Gtrial of the Swiss Group for Clinical Cancer Research and the Central European Cooperative Oncology Group. J Clin Oncol 2007�G25�F2212-2217.
7�j Oettle H, Richards D, Ramanathan RK, et al. A Phase Ⅲ�Gtrial of pemetrexed plus gemcitabine versus gemcitabine in patients with unresectable or metastatic pancreatic cancer. Ann Oncol 2005�G16�F1639-1645.
8�j Colucci G, Giuliani F, Gebbia V, et al. Gemcitabine alone or with cisplatin for the treatment of patients with locally advanced and/or metastatic pancreatic carcinoma�Fa prospective, randomized Phase Ⅲ�Gstudy of the Gruppo Oncologia dell�fItalia Meridionale. Cancer 2002�G94�F902-910.
9�j Heinemann V, Quietzsch D, Gieseler F, et al. Randomized Phase Ⅲ�Gtrial of gemcitabine plus cisplatin compared with gemcitabine alone in advanced pancreatic cancer. J Clin Oncol 2006�G24�F3946-3952.
10�j Louvet C, Labianca R, Hammel P, et al�GGERCOR�GGISCAD. Gemcitabine in combination with oxaliplatin compared with gemcitabine alone in locally advanced or metastatic pancreatic cancer�Fresults of a GERCOR and GISCAD Phase Ⅲ�Gtrial. J Clin Oncol 2005�G23�F3509-3516.
11�j Rocha Lima CM, Green MR, Rotche R, et al. Irinotecan plus gemcitabine results in no survival advantage compared with gemcitabine monotherapy in patients with locally advanced or metastatic pancreatic cancer despite increased tumor response rate. J Clin Oncol 2004�G22�F3776-3783.
12�j Stathopoulos GP, Syrigos K, Aravantinos G, et al. A multicenter Phase Ⅲ�Gtrial comparing irinotecan-gemcitabine�iIG�jwith gemcitabine�iG�jmonotherapy as first-line treatment in patients with locally advanced or metastatic pancreatic cancer. Br J Cancer 2006�G95�F587-592.
13�j Bramhall SR, Schulz J, Nemunaitis J, et al. A double-blind placebo-controlled, randomised study comparing gemcitabine and marimastat with gemcitabine and placebo as first line therapy in patients with advanced pancreatic cancer. Br J Cancer 2002�G87�F161-167.
14�j Reni M, Cordio S, Milandri C, et al. Gemcitabine versus cisplatin, epirubicin, fluorouracil, and gemcitabine in advanced pancreatic cancer�Fa randomised controlled multicentre Phase Ⅲ�Gtrial. Lancet Oncol 2005�G6�F369-376.
15�j Moore MJ, Goldstein D, Hamm J, et al�GNational Cancer Institute of Canada Clinical Trials Group. Erlotinib plus gemcitabine compared with gemcitabine alone in patients with advanced pancreatic cancer�Fa Phase Ⅲ�Gtrial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 2007�G25�F1960-1966.
16�j Kim H, Park JH, Shin SJ, et al. Fixed dose rate infusion of gemcitabine with oral doxifluridine and leucovorin for advanced unresectable pancreatic cancer�Fa Phase Ⅱ�Gstudy. Chemotherapy 2008�G54�F54-62.
17�j Ina S, Tani M, Kawai M, et al. Phase 2 trial of oral S-1 combined with low-dose cisplatin for unresectable advanced pancreatic cancer. Anticancer Res 2008�G28�F2373-2377.
18�j Lee GW, Kim HJ, Ju JH, et al. Phase Ⅱ�Gtrial of S-1 in combination with gemcitabine for chemo-naïve patients with locally advanced or metastatic pancreatic cancer. Cancer Chemother Pharmacol2009�G64�F707-713.
19�j Philip PA, Benedetti J, Corless CL, et al. Phase Ⅲ�Gstudy comparing gemcitabine plus cetuximab versus gemcitabine in patients with advanced pancreatic adenocarcinoma�FSouthwest Oncology Group-directed intergroup trial S0205. J Clin Oncol 2010�G28�F3605-3610.
20�j Nakachi K, Furuse J, Kinoshita T, et al. A Phase Ⅱ�Gstudy of induction chemotherapy with gemcitabine plus S-1 followed by chemoradiotherapy for locally advanced pancreatic cancer. Cancer Chemother Pharmacol 2010�G66�F527-534.
21�j Spano JP, Chodkiewicz C, Maurel J, et al. Efficacy of gemcitabine plus axitinib compared with gemcitabine alone in patients with advanced pancreatic cancer�Fan open-label randomised Phase Ⅱ�Gstudy. Lancet 2008�G371�F2101-2108.
22�j Oh DY, Cha Y, Choi IS, et al. A multicenter Phase Ⅱ�Gstudy of gemcitabine and S-1 combination chemotherapy in patients with unresectable pancreatic cancer. Cancer Chemother Phamacol 2010�G65�F527-536.
23�j Chabot JA, Tsai WY, Fine RL, et al. Pancreatic proteolytic enzyme therapy compared with gemcitabine-based chemotherapy for the treatment of pancreatic cancer. J Clin Oncol 2010�G28�F2058-2063.
24�j Okusaka T, Furuse J, Funakoshi A, et al. Phase Ⅱ�Gstudy of erlotinib plus gemcitabine in Japanese patients with unresectable pancreatic cancer. Cancer Sci 2011�G102�F425-431.
CQ 5-4�@�؏��s�\�X���ɑ��ē��w�Ö@�͐�������邩�H
�����C�O�ɂ�������Ẫ����_������r�����ɂ��C�x���Ö@�ɔ���w�Ö@�̗L�p����������Ă���C���w�Ö@�̎��{�����������i�O���[�hB�j�B
���w�Ö@�̃��W�����͈ꎟ���Âɉ����āC�ꎟ���Â��Q���V�^�r�����_���x�[�X�̎��Âł���t�b���s���~�W����𒆐S�Ƃ������Â��C�ꎟ���Â��t�b���s���~�W���x�[�X�̎��Âł���Q���V�^�r�����_���𒆐S�Ƃ������Â�I������i�O���[�hC1�j�B�� �G�r�f���X
�Q���V�^�r�����_�����邢��S-1 ���؏��s�\�X���ɑ���ꎟ���w�Ö@�Ƃ��ėp�����邪�C������]�߂���̂ł͂Ȃ��C�a��̑����͕K���ł���B���������āC�؏��s�\�X�����҂̗\��̉��P�ɂ͗L���ȓ��Â̊m�����K�v�ł���C�����̗Տ����������{����Ă����B
����܂Ő؏��s�\�X���ɑ�����Ẫ����_������r�����́C①�����`�g���L�Z�h* �P�܂ƃC���m�e�J�����_+�����`�g���L�Z�h *���p�Ɓi���x��Ⅱ�j1�j�C②modified FOLFIRI.3��modified FOLFOX�i���x��Ⅱ�j2�j�C③�x���Ö@�ƃI�L�T���v���`���{�z���i�[�g�J���V�E���{�t���I���E���V���iOFF�j�Ö@+�x���Ö@�i���x��Ⅱ�j3�j④�z���i�[�g�J���V�E��+�t���I���E���V�iFF�j�Ö@ ��OFF�C⑤S-1�P�܂�S-1+�I�L�T���v���`�����p�i���x��Ⅱ�j5�j �C⑥S-1 �P�܂�S-1�{�C���m�e�J�����_���p�i���x��Ⅱ�j6�j�C⑦S-1 �P�܂�S-1+�z���i�[�g �J���V�E�����p�i���x��Ⅱ�j7�j������Ă���i�\�P�j�B①�`③�Ǘᐔ�͂��ꂼ��38 ��C61 ��C46 ��Ə��K�͂Ȃ��̂ł���C�����G�r�f���X�������Ă���Ƃ͂����Ȃ��B①�ł̓C���m�e�J�����_���{�����`�g���L�Z�h*�̗L�p������������C②�ł�FOLFIRI.3 ��FOLFOX �̂�������E�e���̂���L���Ȏ��ÂƂȂ蓾��ƌ��_����Ă��邪 1�C2�j�C���̌��K�͂Ȕ�r�����͍s���Ă��Ȃ��B③�͎x���Ö@�ɑ���OFF �Ö@��p�������w�Ö@�̗L�p�����������Ⅲ�������ł���C�h�C�c��CONKO-study group �Ŏ��{���ꂽ�B�{�����͎x���Ö@�ւ̎��ꂪ������ߓo�^���i�܂��C46 ��œo�^�����~����Ă���B�{�����ł�Karnofsky performance Status�iKPS�j�� 60���C��v���킪�ۂ���Ă��銳�҂�ΏۂƂ��Ď��{���ꂽ�B�S�������Ԃ���v�]�����ڂƐݒ肳��C�Ǘᐔ�͏��Ȃ����̂́COFF �Ö@�Q�̃n�U�[�h�䂪0.45�i95���M����ԁF0.24-0.83�j�ƗL�ӂȐ������Ԃ̉������F�߂��Ă���i���x��Ⅱ�j3�j�B�{�����Ɉ��������āCFF �Ö@��OFF �Ö@�Ƃ̔�r������160 ��ōs���C�������Ԓ����l��FF �Ö@�Q13 �T�ɑ��COFF �Ö@�Q26 �T��OFF �Ö@�Q�ł̗ǍD�Ȑ��т�2008 �NASCO �ɂĕ���Ă���i���x��Ⅱ�j4�j�B⑤�C⑥�͂킪���ŕی��f�ÂƂ��Ď��{�\��S-1 �P�܂�S-1 ���p�Ö@�Ƃ̔�r�������Ď��{���ꂢ��B ⑤�̌��ʁC�I�L�T���v���`���̏�悹���ʂ͔F�߂�ꂸ 5�j�C⑥�ł�S-1+�C���m�e�J�����_���p�Ŏ�v�]�����ڂł��閳�����������Ԃ̉�����F�߂����̂̓��v�w�I�L�Ӎ��͂Ȃ��C���̌��Ⅲ�������͎��{����Ă� 6�j�B⑦�� S-1 �P�܂ɔ�ׁCS-1+�z���i�[�g �J���V�E�����p�ŗL�ӂȖ������������Ԃ̉�����F�� 7�j�C���ݑ�Ⅲ�����������{����Ă���B
�P�A�[���̑�Ⅱ�������ł͂��܂��܂ȃ��W���������݂��Ă��� 8-17�j�i���x��Ⅲ�j�B�킪���ł̓Q���V�^�r�����_����S-1 ���X���ɓK�������F����Ă���C���w�Ö@�Ƃ���S-1 �𒆐S�Ƃ������Â��J������Ă���BS-1 �P�܂ł͑t������15���C�������Ԓ����l4.5 �J���ƕ���Ă���i���x��Ⅲ�j16�j�C����̐V�������Ö@�̊J���ɂ����ĎQ�l�ƂȂ鐬�тł���B�葬�Ò��@��p�����Q���V�^�r�����_����S-1 �̕��p�ɂ�鎡�Â̑�Ⅱ�������ł́C�t������18���C�������Ԓ����l7.0 �J���ƕ���Ă���i���x��Ⅲ�j17�j�C�Q���V�^�r�����_���ϐ�����Q���V�^�r�����_�����p������Ӌ`����������Ă���B
�؏��s�\�X���ɑ���ꎟ���ÂƂ��āC�Q���V�^�r�����_���P�܁CS-1 �P�܁C�Q���V�^�r�����_���{S-1 ���p�̑�K�͂ȑ�Ⅲ�������iGEST �����j�����{�Ƒ�p�̋��������Ƃ��Ď��{���ꂽ 18�j�B���̌��ʁC�������Ԓ����l�̓Q���V�^�r�����_���P�܌Q8.8 �J���CS-1 �P�܌Q9.7 �J���C�Q���V�^�r�����_���{S-1 ���p�Q10.1 �J���ł���C�Q���V�^�r�����_���ɑ���S-1 �̔���ؖ����ꂽ���C�Q���V�^�r�����_���{S-1 ���p�̗D�z���͎�����Ȃ������i���x��Ⅱ�j�B���̎����ɂ����ē��Â̓Q���V�^�r�����_���Q66. 4���CS-1 �Q66.1���C�Q���V�^�r�����_���{S-1 ���p�Q62.5���ƍ����Ɏ��{����Ă���B�܂��C���Ẫ��W�����Ƃ��ẮC�Q���V�^�r�����_���Q�ł�50.5����S-1 ��p�������ÁCS-1�Q�ł�57.9���ŃQ���V�^�r�����_����p�������ÂƃN���X�I�[�o�[�ł̎��Â������s���Ă���B���̌��ʁCGEST �����ɂ�����Q���V�^�r�����_���P�܂Ȃ�т�S-1 �P�܌Q�̐������Ԃ́C�C�O�Ŏ��{���ꂽ����܂ł̒P�܂ɂ��Տ������̌��ʂƔ�חǍD�ł���C���Â��������Ԃ̉����Ɋ�^�������̂Ɛ��@����Ă��� 18�j�B
�ȏ���C�؏��s�\�X���ł́C�S�g��Ԃ��ǍD�ł���C����v����@�\���ۂ��ꂽ��Ԃł���C���Â����{���邱�Ƃ����߂���B��̓I�ȃ��W�����Ƃ��ẮC�G�r�f���X�̂���W���I���Ö@�͊m�����Ă��Ȃ��C�ꎟ���Â��Q���V�^�r�����_�x�[�X�̎��Âł���t�b���s���~�W����𒆐S�Ƃ������W������p���邱�Ƃ��Ó��ƍl������B
2013 �N 12 ���C FOLFIRINOX �Ö@�̎����т����ƂɁC�z���i�[�g�J���V�E���C�I�L�T���v���`���C�C���m�e�J�����_���X���ɕی��K�p�����F���ꂽ�B�t���I���E���V�C�z���i�[�g�J���V�E���C�I�L�T���v���`����p����OFF �Ö@�͂킪���ł͂قƂ�ǎ��{����Ă��炸�C����L�����ƈ��S�̊m�F���K�v�l����B
�\1�@�؏��s�\�X���ɑ���2 �����w�Ö@�̎�Ȏ����� ��
�N���Ã��W���� ���Ґ� �t������ ��������������
�����l(��)�S��������
�����l(��)�n�U�[�h�� (95%CI) p �l Ulrich-Pur 1�j
2003�C���m�e�J�����_��+�����`�g���L�Z�h
19
16%
4
6.5
NA
NA
�����`�g���L�Z�h
19
0
2.5
4.3
Yoo 2�j
2009FOLFIRI
31
23%
1.9
3.8
NA
NA
Modified FOLFOX
30
17%
1.4
3.4
Pelzer 3�j
2011�x���Ö@
23
—
—
2.3
0.45
0.008
OFF
23
—
—
4.8
(0.24-0.83)
Pelzer 4�j
2008FF
91
—
2.1
3.0
NA
0.014
OFF
77
—
3
6.0
Okusaka 5�j
2012S-1
130
11.5%
2.8
6.9
1.03
0.82
S-1+�I�L�T���v���`��
134
20.9%
3.0
7.4
(0.79-1.34)
Mizuno 6�j
2013S-1
67
6.0%
1.9
5.8
0.77
0.175
S-1+�C���m�e�J�����_��
60
8.3%
3.5
6.8
(0.53-1.11)
Okusaka 7�j
2013S-1
71
19.7%
2.7
6.1
0.82
0.463
S-1+�z���i�[�g�J���V�E��
69
27.5%
3.8
6.3
NA
FOLFIRI: �t���I���E���V��+�z���i�[�g�J���V�E��+�C���m�e�J�����_��, FOLFOX: �t���I���E���V��+�z���i�[�g�J���V�E��+�I�L�T���v���`��, OFF: �I�L�T���v���`��+�z���i�[�g�J���V�E��+�t���I���E���V��, FF: �z���i�[�g�J���V�E��+�t���I���E���V��, CI: confidence interval, NA: not assessed
�� �����ւ̒�
�X���ɑ���ꎟ���w�Ö@�̓Q���V�^�r�����_�������łȂ��CS-1 ��Q���V�^�r�����_�����܂܂Ȃ����Ö@���m��������C����ɔ������w�Ö@���I��������������̂Ɨ\�z�����B�܂��C���q�W�I����܂߂��V�K��܂̊J�������͓I�ɐi�߂��Ă���C���w�Ö@���܂߁C�X���̐����w�I�����Ɋ�Â��L���Ȏ��Ö@�̊m�������҂����B
�� ���p����
1�j Ulrich-Pur H, Raderer M, Verena Kornek G, Schüll B, Schmid K, Haider K, Kwasny W, Depisch D, Schneeweiss B, Lang F, Scheithauer W. Irinotecan plus raltitrexed vs raltitrexed alone in patients with gemcitabine-pretreated advanced pancreatic adenocarcinoma. Br J Cancer 2003�G88�F1180-1184.
2�j Yoo C, Hwang JY, Kim JE, Kim TW, Lee JS, Park DH, Lee SS, Seo DW, Lee SK, Kin MH, Han DJ, Kim SC, Lee JL. A randomised Phase Ⅱ�Gstudy of modified FOLFIRI.3 vs modified FOLFOX as second-line therapy in patients with gemcitabine-refractory advanced pancreatic cancer. Br J Cancer 2009�G101�F1658-1663.
3�j Pelzer U, Schwaner I, Stieler J, Stieler J, Adler M, Seraphin Dörken B, Riess H, Oettle H. Best supportive care�iBSC�jversus oxaliplatin, folinic acid and 5-fluorouracil�iOFF�jplus BSC in patients for second-line advanced pancreatic cancer�FA Phase Ⅲ-study from the German CONKO-study group. Eur J Cancer 2011�G47�F1676-1681.
4�j Pelzer U, Kubica K, Stieler J, Schwaner I, Heil G, Görner M, Mölle M, Hilbig A, Dörken B, Riess H, Oettle H. A randomized trial in patients with gemcitabine refractory pancreatic cancer. Final results of the CONKO 003 study. J Clin Oncol 26 suppl�F215s�iabstr 4508�j, 2008.
5�j Okusaka T, Ohkawa S, Isayama H, et al: Randomized phase Ⅱ trial of S-1 versus S-1 plus oxaliplatin (SOX) in patients with gemcitabine refractory pancreatic cancer. European Socie for Medical Oncology 2012 Congress. Ann Oncol 23 suppl 9 : (abstr 728), 2012
6�j Mizuno N, Yamao K, Komatsu Y, et al: Randomized phase Ⅱ trial of S-1 versus S-1 plus irinotecan (IRIS) in patients with gemcitabine-refractory pancreatic cancer. 2013 Gastrointestinal Cancers Symposium. J Clin Oncol 31 suppl : (abstr 263), 2013
7�j Okusaka T, Ueno M, Omuro Y, et al: Randomized phase Ⅱ study comparing S-1 plus Leucovorin (SL) versus S-1 alone in patients with gemcitabine-refractory advanced pancreatic cancer (APC). European Cancer Congress 2013. Eur J Cancer 49 suppl 2: S611 (abstr 2578), 2013
8�j Burris HA 3rd, Rivkin S, Reynolds R, Harris J, Wax A, Gerstein H, Mettinger KL, Staddon A. Phase Ⅱ trial of oral rubitecan in previously treated pancreatic cancer patients. Oncologist 2005�G10�F183-190
9�j Androulakis N, Syrigos K, Polyzos A, Aravantinos G, Stathopoulos GP, Ziras N, Mallas K, Vamvakas L, Georgoulis V; Hellenic Oncology Research Group. Oxaliplatin for pretreated patients with advanced or metastatic pancreatic cancer: a multicenter phase Ⅱ study. Cancer Invest 2005�G23�F9-12
10�j Reni M, Pasetto L, Aprile G, Cordio S, Bonetto E, Dell'Oro S, Passoni P, Piemonti L, Fugazza C, Luppi G, Milandri C, Nicoletti R, Zerbi A, Balzano G, Di Carlo V, Brandes AA.. Raltitrexed-eloxatin salvage chemotherapy in gemcitabine-resistant metastatic pancreatic cancer. Br J Cancer 2006�G94�F785-791
11�j Demols A, Peeters M, Polus M, Marechal R, Gay F, Monsaert E, Hendlisz A, Van Laethem JL. Gemcitabine and oxaliplatin (GEMOX) in gemcitabine refractory advanced pancreatic adenocarcinoma: a phase Ⅱ study. Br J Cancer 2006�G94�F481-485
12�j Boeck S, Weigang-Köhler K, Fuchs M, Kettner E, Quietzsch D, Trojan J, Stötzer O, Zeuzem S, Lordick F, Köhne CH, Kröning H, Steinmetz T, Depenbrock H, Heinemann V. Second-line chemotherapy with pemetrexed after gemcitabine failure in patients with advanced pancreatic cancer: a multicenter phase Ⅱ trial. Ann Oncol 2007�G18�F745-751
13�j Xiong HQ, Varadhachary GR, Blais JC, Hess KR, Abbruzzese JL, Wolff RA. Phase 2 trial of oxaliplatin plus capecitabine (XELOX) as second-line therapy for patients with advanced pancreatic cancer. Cancer 2008�G113�F2046-2052
14�j Yi SY, Park YS, Kim HS, Jun HJ, Kim KH, Chang MH, Park MJ, Uhm JE, Lee J, Park SH, Park JO, Lee JK, Lee KT, Lim HY, Kang WK. Irinotecan monotherapy as second-line treatment in advanced pancreatic cancer. Cancer Chemother Pharmacol 2009;63:1141-1145
15�j Brell JM, Matin K, Evans T, Volkin RL, Kiefer GJ, Schlesselman JJ, Dranko S, Rath L, Schmotzer A, Lenzner D, Ramanathan RK. Phase Ⅱ study of docetaxel and gefitinib as second-line therapy in gemcitabine pretreated patients with advanced pancreatic cancer. Oncology 2009;76: 270-274
16�j Morizane C, Okusaka T, Furuse J, Ishii H, Ueno H, Ikeda M, Nakachi K, Najima M, Ogura T, Suzuki E. A phase II study of S-1 in gemcitabine-refractory metastatic pancreatic cancer. Cancer Chemother Pharmacol 2009�G63�F313-319
17�j Morizane C, Okusaka T, Ueno H, Kondo S, Ikeda M, Furuse J, Shinichi O, Nakachi K, Mitsunaga S, Kojima Y, Suzuki E, Ueno M, Yamaguchi T. Phase Ⅰ/Ⅱ study of gemcitabine as a fixed dose rate infusion and S-1 combination therapy (FGS) in gemcitabine-refractory pancreatic cancer patients. Cancer Chemother Pharmacol 2012;69:957-964
18�j Ueno H, Ioka T, Ikeda M, Ohkawa S, Yanagimoto Boku N, Fukutomi A, Sugimori K, Baba H, Yamao Shimamura T, Sho M, Kitano Cheng AL, Mizumoto K, Chen JS, Furuse J, Funakoshi A, Hatori T, Yamaguchi T, Egawa S, Sato A, Ohashi Y, Okusaka T, Tanaka M. Randomized Phase Ⅲ Study of Gemcitabine Plus S-1, S-1 Alone, or Gemcitabine Alone in Patients With Locally Advanced and Metastatic Pancreatic Cancer in Japan and Taiwan: GEST Study. J Clin Oncol 2013; 31: 1640-1648
6 �X�e���g�Ö@
CQ 6-1�@�ǐ����t���؏��s�\��ɒ_���h���i�[�W�͐�������邩�H
�����؏��s�\�X���ɑ���_���h���i�[�W�́C���������i�O���[�hB�j�B
�؏��s�\�X���ɑ���_���h���i�[�W�́C�J���ɂ��O�ȓI�����p���������I�����p�����������i�O���[�hB�j�� �G�r�f���X
- �_���h���i�[�W�ɂ��\��̉��P����
�ǐ����t���؏��s�\�X���Ǘ�̑����́C���w�Ö@���s�����ߒ_���h���i�[�W�ɂ�錸����K�v�Ƃ���B�������C�����p�ɂ��\��̉��P��Տ���̗��_���q�ׂ��_���͏��Ȃ��B�_���h���i�[�W�ɂ��\��ւ̌��ʂ��L�ڂ����_���́C1960 �N�ォ��1980 �N��ɕ���Ă���B��������摜�f�f�����B���Ă��Ȃ����̘_���ŁC���t�Ǘ�ɑ��J���p���{�s���X���Ɛf�f����؏����s��Ȃ������ꍇ�C�_���h���i�[�W�{�s�Q�Ɣ�{�s�Q�ŗ\����r�����_���������BSarr ��́C1965 �N����1980 �N�܂ł̕���45 �_��8,571 ����W�ς��C�؏��s�\�X�����҂̌Ƒ��I��p���������� 1�j�i���x��Ⅴ�j�B�_���o�C�p�X�Ɋւ��ẮC10 �_��912 �Ⴊ��͂��ꂽ�B�e�_���̏Ǘ���W�ς��C�_���o�C�p�X�Q�ƒP�J���Q�ɕ����Đ����\����r���������Ƃ���C5.4 �J�� vs 3.5 �J���Œ_���o�C�p�X�Q�̂ق����\��ǍD�ł������B�܂��C�_���o�C�p�X�Q������ɒ_�ǃh���i�[�W�Q�ƒ_嚢�h���i�[�W�Q�ɕ�����r���������Ƃ���C6.5 �J�� vs 5.3 �J���ƒ_�ǃh���i�[�W�Q�ł��\�オ�ǍD�ł������B
- �_���h���i�[�W�ɂ��QOL �̉��P����
�؏��s�\�X���̉��t���P�̖ړI�̂ЂƂɏǏ��QOL �̉��P���������邪�C�����̌������s�����_���͂قƂ�ǂȂ��BBallinger ��͕ǐ����t���X���������҂ɑ��C�������I�������͌o��o�̓I�ɒ_���h���i�[�W���{�s���C�Ǐ�ւ̉e�����������Ɍ������� 2�j�i���x��Ⅳb�j�B�_���h���i�[�W���{�s����19 ��S��ʼn��t�͉��P���C11 ��i57.9���j�Ŕ畆�~�y�������P�C16 ��i84.2���j�ŐH�v�s�U�����P�����B����C�u�ɂ�q�C�͉��P���Ȃ������B
- �O�ȓI�_���h���i�[�W�Ɠ������I�_���h���i�[�W�̔�r
�O�ȓI�_���h���i�[�W�Ɠ������I�_���h���i�[�W�̔�r�������_���͑������邪 3-12�j�CRCT ��4 �� 4-7�j�i���x��Ⅱ�j�C���^�A�i���V�X��2 �� 8, 9�j�i���x��Ⅰ�j�BMoss ��͂��̂���RCT3 �҂�p�������^�A�i���V�X����Ă��� 8�j�B���̃��^�A�i���V�X�ɂ�����O�ȓI�_���h���i�[�W�Ɠ������I�_���h���i�[�W�iplastic stent�j�̔�r�ł́C�����ǂ̑����X�N�͓������I�_���h���i�[�W�Q�ŗL�ӂɒႭ�ip��0.0007�j�C30 ����̎��S���͓������I�_���h���i�[�W�Q�ŒႢ�X���ɂ��������C�L�Ӎ���F�߂Ȃ������ip��0.07�j�B�ĕǂ̑����X�N�͓������I�_���h���i�[�W�Q�̂ق����L�ӂɍ����������ip��0.00001�j�C���Q�ŗ\���QOL �ɍ���F�߂Ȃ������BTaler ���RCT3 �҂�p�������^�A�i���V�X����Ă��� 9�j�B�������I�_���h���i�[�W�Q�ƊO�ȓI�_���h���i�[�W�Q�̗��Q�Ԃɂ����āC�����s�����C�d�Ǎ����ǁC30 �����S���iOR�F0.522�C95��CI�F0.263�`1.036�j�Ɋւ��Ă͗L�Ӎ����Ȃ������B����C�������I�_���h���i�[�W�Q�͊O�ȓI�_���h���i�[�W�Q�Ɣ�r���C�L�Ӎ��������Ēlj����Â�K�v�Ƃ����iOR�F7.23�C95��CI�F3.73�`13.98�j�B
Watanapa ��́C1971�`90 �N�ɔ��\���ꂽ�O�ȓI�_���h���i�[�W�Ɋւ���23 �_��1,807 ��ƌo��o�̓I�_���h���i�[�W�ipercutaneous transhepatic biliary drainage�GPTBD�j�Ɋւ���7 �_��490 ��C����ѓ������I�_���h���i�[�W�iendoscopic biliary drainage�GEBD�j�Ɋւ���9 �_��689 ����r���C�p�O�f�f�̕��@�C�������u�̔�r�C�\��w������ɑ�����@�C�u�ɁC�⏕�Ö@�Ȃǂɂ��Ă܂Ƃ߂� 10�j�i���x��Ⅴ�j�B�؏��s�\�X���̌����ɂ��āC���������ǂ͊O�ȓI�_���h���i�[�W�Q�ő����������C�_�lj��C�`���[�u�ǂȂǂ̌�������ǂ�PTBD �Q��EBD �Q�ő������Ƃ���C�؏��s�\�X���ɑ��ɘa�ړI�̂��߂ɒ����I�Ȍ��������҂���ꍇ�ɂ͊O�ȓI�_���h���i�[�W���悢���@�ł���Əq�ׂĂ���B
Raikar ��́C�؏��s�\�X�����҂ɓ������I�_���h���i�[�W���{�s����34 ��ƊO�ȓI�_���h���i�[�W���{�s����32 ��ɕ����C�������Ɍ����̌��ʂƒ_���h���i�[�W�ɂ������p���r���� 11�j�i���x��Ⅳb�j�B�p�㍇���ǂ͊O�ȓI�_���h���i�[�W�Q33���C�������I�_���h���i�[�W�Q21���ƍ��͂Ȃ������B�ŏ��̍݉@�����͊O�ȓI�_���h���i�[�W�Q14 ���C�������I�_���h���i�[�W�Q7 ���ip��0.001�j�ƗL�Ӎ��������ē������I�h���i�[�W�Q�ŒZ���C��p��$18,325 ��$9,663 �ł���������h���i�[�W�Q�̂ق������Ȃ������B
Brandabur ��́C���t���؏��s�\�X���Ǘ�ɑ���O�ȓI�_���h���i�[�W�Q�i�O�ȌQ�j�Ɣ�O�ȓI�_���h���i�[�W�Q�i��O�ȌQ�F17 ��͓������I�_���h���i�[�W�C15 ��͌o��o�̓I�_���h���i�[�W�j�̍݉@�����C�����ǁC���S���C��p�ɂ��Ē��ׂĂ���C�݉@�����C�����ǁC���S���ɍ���F�߂Ȃ��������C��p�͔�O�ȌQ�̂ق������Ȃ������ƕ��Ă��� 12�j�i���x��Ⅳb�j�B
�� �����ւ̒�
�ǐ����t���؏��s�\�X���ɑ���_���h���i�[�W�́C���w�Ö@�O�̌����ړI�݂̂Ȃ炸�C�\���QOL �̉��P�����҂ł��邽�߁C�ϋɓI�ɍs���ׂ��ł���B�O�ȓI�_���h���i�[�W�͒����J�������҂ł��C�������I�_���h���i�[�W���܂ޔ�O�ȓI�_���h���i�[�W�͍����ǂ̔��������Ⴍ��p�����Ȃ��Ƃ������ʂ��������C���͉̕ߋ��̂��̂������C���݂̈�Ïf���Ă��Ȃ��B�X�e���g�̐��\��������I�Z�p�̐i���͒��������߁C���݂̈�Ã��x���ɑ������_���h���i�[�W�̗L�p���̌������K�v�ł���B
�� ���p����
1�j Sarr MG, Cameron JL. Surgical management of unresectable carcinoma of the pancreas. Surgery 1982�G91�F123-133.
2�j Ballinger AB, McHugh M, Catnach SM, et al. Symptom relief and quality of life after stenting for malignant bile duct obstruction. Gut 1994�G35�F467-470.
3�j van den Bosch RP, van der Schelling GP, Klinkenbijl JH, et al. Guidelines for the application of surgery and endoprostheses in the palliation of obstructive jaundice in advanced cancer of the pancreas. Ann Surg 1994�G219�F18-24.
4�j Smith AC, Dowsett JF, Russell RC, et al. Randomised trial of endoscopic stenting versus surgical bypass in malignant low bileduct obstruction. Lancet 1994�G344�F1655-1660.
5�j Shepherd HA, Royle G, Ross AP, et al. Endoscopic biliary endoprosthesis in the palliation of malignant obstruction of the distal common bile duct�Fa randomized trial. Br J Surg 1988�G75�F1166-1168.
6�j Artifon EL, Sakai P, Cunha JE, et al. Surgery or endoscopy for palliation of biliary obstruction due to metastatic pancreatic cancer. Am J Gastroenterol 2006�G101�F2031-2037.
7�j Andersen JR, Sørensen SM, Kruse A, et al. Randomised trial of endoscopic endoprosthesis versus operative bypass in malignant obstructive jaundice. Gut 1989�G30�F1132-1135.
8�j Moss AC, Morris E, Leyden J, et al. Malignant distal biliary obstruction�Fa systematic review and meta-analysis of endoscopic and surgical bypass results. Cancer Treat Rev 2007�G33�F213-221.
9�j Taylor MC, McLeod RS, Langer B. Biliary stenting versus bypass surgery for the palliation of malignant distal bile duct obstruction�Fa meta-analysis. Liver Transpl 2000�G6�F302-308.
10�j Watanapa P, Williamson RC. Surgical palliation for pancreatic cancer�Fdevelopments during the past two decades. Br J Surg1992�G79�F8-20.
11�j Raikar GV, Melin MM, Ress A, et al. Cost-effective analysis of surgical palliation versus endoscopic stenting in the management of unresectable pancreatic cancer. Ann Surg Oncol 1996�G3�F470-475.
12�j Brandabur JJ, Kozarek RA, Ball TJ, et al. Nonoperative versus operative treatment of obstructive jaundice in pancreatic cancer�Fcost and survival analysis. Am J Gastroenterol 1988�G83�F1132-1139.
- CQ 6-2
- �؏��s�\�X���ɑ���_���h���i�[�W�̃A�v���[�`���[�g�́C�o��I�Ɠ������I�̂ǂ��炪�悢���H
�����؏��s�\�X���ɑ���_���h���i�[�W�͓������I�ɍs�����Ƃ����߂���i�O���[�hB�j�B �� �G�r�f���X
�Ǐ��i�s�؏��s�\�X���݂̂Ɍ��肵���o��I�h���i�[�W����ѓ������I�h���i�[�W�̑I���Ɋւ���RCT �͂Ȃ����C�����_���ǂɑ���RCT �ł͓������I�h���i�[�W���o��I�h���i�[�W�ɔ�ׂĎ�Z�������͓����i89��vs 76���j�����C�������i81��vs 61���Cp �� 0.017�j�͗L�ӂɗD��Ă��� 1�j�i���x��Ⅱ�j�B�܂������ǔ�������19��vs 67���ƌo��I�h���i�[�W�ō����C30 ���ȓ����S���i15��vs 33���Cp��0.016�j���L�ӂɌo��I�h���i�[�W�ō����C���ɍ���̊��҂ɂ͓������I�h���i�[�W�����߂��Ă���B1987 �N�ɔ��\���ꂽ�{�_���ȍ~�C�Ǘ�W�ό������܂߂��o��I�h���i�[�W����ѓ������I�h���i�[�W�̑I���Ɋւ���͂Ȃ��������C2002 �N�ɔ�؏������_���Ǘ�ɑ���8�`10mm �a�̎��Ȋg���^���^���b�N�X�e���g��p�����o��I�h���i�[�W��12Fr �̃v���X�`�b�N�X�e���g��p�����������I�h���i�[�W��RCT �����ꂽ 2�j�i���x��Ⅱ�j�B��Z�������͓����Łi75��vs 58���Cp��0.29�j�C�������i71��vs 42���Cp��0.03�j�C�������Ԓ����l�i3.7 �J�� vs 2.0 �J���Cp �� 0.02�j�͗L�ӂɌo��I�h���i�[�W�ŗD��Ă����B����C�����ǂ͌o��I�h���i�[�W�ő����݂�ꂽ���i61��vs 35���Cp �� 0.09�j�C30 ���ȓ����S���i36��vs 42���Cp �� 0.83�j�͕ς��Ȃ������B���̂Ȃ��ŕM�҂���q�ׂĂ��邪�C�ߔN�؏��s�\�X���ɑ��ă��^���b�N�X�e���g��p�����������I�h���i�[�W�͕W���I�Ȏ��ÂƂȂ��Ă���C����̃X�e���g��p�����ꍇ�̔�r�������]�܂��B
�� �����ւ̒�
�o��I�_���h���i�[�W�͓������I�h���i�[�W�ɔ�ׂĐN�P�x���������Ƃ���C���݂ł͌�҂��W���I�Ȏ��ÂƂȂ��Ă���B�������C�������I�_���h���i�[�W�̐�������100���łȂ����Ƃɒ��ӂ��C�������I�h���i�[�W�ł̓R���g���[��������Ȋ̖啔����ȂǂɊւ��Ă͕K�v�ɉ����Čo��I�_���h���i�[�W���s�����Ƃ��]�܂����B
�� ���p����
1�j Speer AG, Cotton PB, Russell RC, et al. Randomised trial of endoscopic versus percutaneous stent insertion in malignant obstructive jaundice. Lancet 1987�G2�F57-62.
2�j Piñol V, Castells A, Bordas JM, et al. Percutaneous self-expanding metal stents versus endoscopic polyethylene endoprostheses for treating malignant biliary obstruction�Frandomized clinical trial. Radiology 2002�G225�F27-34.
CQ 6-3�@�X���ɂ��ǐ����t�ɑ���X�e���g�̎�ނ͉�����������邩�H
�����X���؏��s�\��ɂ��ǐ����t�ɑ��ẮC�v���X�`�b�N�X�e���g�iplastic stent�GPS�j�����J�����Ԃ̒������Ȋg���^���^���b�N�X�e���g�iself-expandable metallic stent�GSEMS�j�����������i�O���[�hC1�j�BSEMS �̂Ȃ��ł͔핢�^�icovered type�j�̊J�����Ԃ�uncovered type ��蒷�����Ƃ�����Ă���i�O���[�hC1�j�B�{�݂��Ƃ̋Z�p�C�f�Ñ̐��C���҂̏�Ԃɂ����uncovered type ��PS �̑I�����l�����Ă��悢�B �� �G�r�f���X
- �X�e���g�̎��
�X�e���g�̎�ނɂ͑傫�������ăv���X�`�b�N�X�e���g�iplastic stent�GPS�j�Ǝ��Ȋg���^���^���b�N�X�e���g�iself-expandable metallic stent�GSEMS�j������i�}2�`5�j�BSEMS �͋������C���[�ŕ҂Ԗڏ�̍\�������Ă���C�ׂ����Ԃł̎��[���\�ł���C����������q�`�����l����ʉ߉\�ŁC���_�ǕǕ��ɂ����Ċg�������10mm ���x�̓��o���m�ۂł���i�}3�`5�j�B�������CSEMS �͖Ԗڏ�̂��߁C�Ǖ��Ŋ��g�D���N�����čĕǂ��邱�Ƃ��m���Ă���C�����h�����߂ɔ핢�^��covered type ���J�����ꂽ�i�}4�j�B���̂��ߏ]���^�̖Ԗڏ��SEMS ��uncovered type �ƌď̂���Ă���B
�X�e���g�̗Տ������͒ʏ풆���_�ǕǗ�Ɗ̖啔�_�ǕǗ�͋�ʂ���Ď{�s����Ă��邪�C����������肵�Č��������Տ������͋ɂ߂ď��Ȃ��B�������_�Ǖǂɑ���Տ������̑������X����60�`80�����߂Ă��邪�C�������Ƃɂ��̔䗦�͈قȂ�B�����������肵�Ă��Ȃ��؏��s�\�����������_�Ǖǂɑ���RCT �͂���������Ă���B�܂��Cuncovered type ��SEMS ��PS �̔�r�ł́Cuncovered SEMS �̂ق����L�ӂɐ��їǍD�Ƃ���RCT ������Ă��� 1, 2�j�i���x��Ⅱ�j�Ccovered SEMS vs PS ��2 �҂��� 3, 4�j�i���x��Ⅱ�j�B�������SEMS �̊J�����Ԃ������C��؏������������_�Ǖǂł͍����ǁC�R�X�g�̖ʂ����SEMS �̂ق������������B���̂����X���Ɍ��肵����covered SEMS vs PS ��1 �҂ł����� 4�j�B�������CSEMS �̗��u�ɂ͐��I�Ȓm���ƋZ�p���v������C���ɕǎ��C�����ǔ������₻�̑�ɂ͓�a���邱�Ƃ�����B���̂��߁C���I�Ȓm����Z�p��L���Ȃ��p�҂ł́C�J�����Ԃ������S����D�悵��PS ��I�����̂ЂƂƂ��čl�����邱�Ƃ���ނȂ��B���̂��߁CPS ��SEMS �̑I���Ɋւ��Ă̐����x���O���[�hC1 �Ƃ����B�܂��CSEMS �̃^�C�v�Ɋւ��Ă��C�X���Ɍ�������r���������Ȃ��C�G�r�f���X�����s�����Ă���ƍl�����C���݂̐����x���O���[�hC1 �Ƃ����B����h���i�[�W���ɂ�PS ���g�p���C����I��SEMS �𗯒u���Ă���{�݂�����̂ŁC�����܂ł��������u��O���ɒu�����I���ł��邱�Ƃ�lj����Ă����B
SEMS �̂Ȃ��ł�covered type��uncovered type ������C�������r����RCT ��6 �҂���Ccovered type �̗D�ʐ��v�w�I�Ɏ��������̂�4 �҂��� 5-10�j�i���x��Ⅱ�j�B�X���Ɍ��肵��RCT ��2 �҂����Ȃ��C�������covered SEMS �̐��т��ǍD�ł����� 6, 7�j�B�����ʂ̑w�ʉ����Ȃ���Ă���RCT ��1 �҂���C�T�u�O���[�v��͂��X���ł͗L�ӂ�covered SEMS �̊J�����Ԃ������Ƃ������ʂł����� 5�j�B�܂��C���^�A�i���V�X��2 �ҕ���Ă���Ccovered SEMS �̊J�����Ԃ��L�ӂɒ����Ƃ������̂ƁC�����Ȃ��Ƃ�����͂ł��������C��������������X���Ɍ��肵�Ă��Ȃ��ł��� 11, 12�j�i���x��Ⅰ�j�BKitano ��́C�Ώۂ��X���Ɍ��肵�����{����RCT �̐��т�2012 �N��ASGE �Ŕ��\���� 7�j�B�킪����22 �{�݂ōs��ꂽRCT �ł���C���ݍ����Ŏg�p�\�ȃX�e���g��p���ē��v�w�I��covered type �̊J�����Ԃ�uncovered type �����������Ƃ������Ă���C����ɍł��������G�r�f���X����Ă�����̂ƍl������B�ȏ���CSEMS �̎�ނł́C�X���Ɍ��肵���͏��Ȃ����̂́C�J�����Ԃ̒���covered type �����������B
�X�e���g���g�p����ۂɏd�v�Ȃ͕̂ǁE�J�����Ԃ����łȂ��C�����ǂ��܂߂����S���ł���B��ȍ����ǂ͈�E�C�_嚢���C�X���ł���BPS �ł̓X�e���g�ǂ������C�����ň�E�������BSEMS�ł͒_嚢���C�X���Ccovered type �ł͈�E���뜜�����B�_嚢���C�X����covered type �ő����Ƃ���Ă������C���^�A�i���V�X�ł͍����Ȃ����Ƃ������ꂽ 11�j�i���x��Ⅰ�j�B�܂��C�_嚢�����댯�Q�ɂ��Ă̌�����2 �ҕ���Ă��� 13, 14�j�i���x��Ⅳb�j�B������̕ł��_嚢�ǂ����_�ǂɍ������镔�ʂɊ�������C���Z����������̂����댯�Q�ƍl�����Ă���C1 �҂ł͒_嚢�������댯�Q�ł���ƕ���Ă���B�������C�\�h�@�Ɋւ��Ă̗L�p�ȕ͂Ȃ��B�X���Ɋւ��Ă��X���ł͏��Ȃ����Ƃ�������Ă��� 15�j�i���x��Ⅳa�j�B�\�h�@�Ƃ��Ă͓�������ؐ؊J�p�iendoscopic sphincterotomy�GEST�j���L�p�Ƃ��������邪 16�j�i���x��Ⅳb�j�CRCT �ɂ�錟���͂Ȃ��C�������̉�͂ł́C�K���������̗L�p���͎�����Ă��Ȃ� 17�j�i���x��Ⅳb�j�BSEMS�̕����w�I�����ł���radial force ��axial force ����������Ă��� 18�j�i���x��Ⅲ�j�Caxial force ���X������ 19�j�i���x��Ⅲ�j�ɊW���Ă��邱�Ƃ��ŋ߂̘_���Ŏ�������Ă���B��E��covered type �ɓ��L�̍����ǂł���Cfin ������covered SEMS �ŏ��Ȃ����Ƃ�����Ă���i�}5�j 6�j�B�܂��Caxial force �̈Ⴄcovered SEMS �̔�r����C��E�ւ̊֗^��Տ������̌��ʂ��玦�����Ă���_�������\����Ă��� 20�j�i���x��Ⅲ�j�C��E�̖h�~�ɂ�SEMS �̕����w�I�����̉��ǂ�fin �ɑ�\�����h�~���u�̍H�v�����߂���B�ȏ�̂��Ƃ���C�����ǂ̖ʂ����SEMS �����covered type �̐����͑Ó��ƍl������B
- ���w�Ö@�C���w���ː��Ö@�{�s��ɑ���X�e���g�Ö@�̈��S��
���w�Ö@�{�s���̃X�e���g�Ö@�̐��т͏\���Ɍ�������Ă���Ƃ͂����Ȃ��BHoffman ����X���ɑ���p�O���w���ː��Ö@�̑O���������ɂ����āC������Z�Ɋ֘A�����d�Ăȍ����ǂ������ɔF�߂�ꂽ�ƕ� 21�j�i���x��Ⅳa�j���Ă���B���̌�Pisters ��͏p�O���w���ː��Ö@�̑O���������ɂ����āC�X�e���g�Ɋ֘A�����L�Q���ۂ̔����p�x�͂ނ���Ⴉ�����ƕ� 22�j�i���x��Ⅳb�j���Ă���BNakai ��̌������̌����ł́C���^���b�N�X�e���g���u�̓Q���V�^�r���ɂ��Ő�������_�����������������ǂ̕p�x�ɉe�����Ȃ������ƕ� 23�j�i���x��Ⅳb�j���Ă���B���w�Ö@���X�e���g�̐��тɗ^����e���͖��炩�ł͂Ȃ��C����Ǘ�̏W�ς��K�v�ƍl������B



�}2�F�v���X�`�b�N�X�e���g�iplastic stent�GPS�j�B�X�e���g�̐����ɂ��Ă͖{�����Q�Ƃ̂���
- a�F�X�g���[�g�^�i�A���X�e���_���^�Ƃ������j�CFlexima�FBoston Scientific �А�
���[�Ƀt���b�v��L���C�t���b�v�쐬���ʂɂ��E���J���Ă���B - b�F�_�u���s�b�O�e�[���^�C�N�b�N�А�
���[���s�b�O�e�[����ɂȂ��Ă���C��E��h���\���ɂȂ��Ă���B�ʏ�ۂ܂��������̓����ɑ��E��L���Ă���B - c�F�^�l���o�E���^�CDouble Layer stent�FOlympus �А�
���[�Ƀt���b�v��L���Ă��邪���E���Ȃ��B
�� �����ւ̒�
���݂܂ŕ���Ă��鑽���̗Տ������͕a�Ԃ��قȂ錴�����i�X�������C�_�NJ��C�����p�ߓ]�ڂȂǁj�����肹���Ɏ{�s����Ă���C�܂��C���̕]���̕��@���قȂ�B���̂���RCT ���̂̕]���E���߂ɂ͌��E������C��������RCT �����Ƃɂ������^�A�i���V�X�̌��ʂ̕]���E���߂ɂ����ӂ�v����B����C�X���ɂ��ǐ����t�݂̂ɑΏۂ��i�����Տ��������K�v�ł���B���w�Ö@�C���w���ː��Ö@�̐i���ƂƂ����X���؏��s�\��̗\����������Ă��Ă��邪�C�����̎��Â��X�e���g�̐��тɗ^����e���̌������\���ł͂Ȃ��C�܂��C���������\��ɑ���X�e���g�Ö@�̉��ǂ��ׂ��_�����炩�ɂ͂Ȃ��Ă��Ȃ��B
Uncovered SEMS ��covered SEMS �̔�r�]���Ɋւ��āC�O�q�̌��E�̂Ȃ��ł͂��邪�C2012 �N��ASGE �Ŕ��\���ꂽ�i����̉����ł͐T�d�ȍ��ǂ��Ȃ��ꂽ�w��̏��^�͈��p�����Ƃ��č̗p�j�k���̘_���́C�킪����30 ���鑽�{�݂��X����ΏۂɌ��肵�s��ꂽ���{���������ł��邱�ƂƁC�킪���ōł������g�p����Ă���X�e���g���g�p���Ă��邱�Ɠ����C���݂̂킪���̗Տ��̎���ɍł�������RCT �ƍl������B���̌��ʂ�covered SEMS ��uncovered SEMS ���͊J�����Ԃ������Ƃ������̂ł������B�������C�ЂƂ�RCT �݂̂ŋ��͂ȃG�r�f���X�Ƃ͌����ꂸ�C�X���Ƃق��̊��킪�������C�O�̗Տ������ł͗L�Ӎ����o�Ă��Ȃ����ƂȂǂ��C�ア�����ɂƂǂ߂Ă����̂������_�ł͑Ó��ƍl���C�����ψ���ł͐����x��C1 �Ƃ����B����̉����ߒ��ɂ����āC����uncovered SEMS ��covered SEMS �̖��Ɋւ��ẮCRCT ��^�A�i���V�X�̕]���E���߂̈Ⴂ����C�������public comments �ɂ�����covered SEMS �ɑ��Ĕے�I�Ȍ����̈ӌ����������B���̂��߁C�킪���ł̎��f�ÂɎx�Ⴊ�����Ȃ��悤�ɐ������e�C�����x�ɂ����x�̏C����������ꂽ�BCovered SEMS ��uncovered SEMS �̖��Ɋւ��ẮC����̃K�C�h���C�������ɂ����čČ��������邽�߂ɁC���w�Ö@�C���w���ː��Ö@�̐i���܂��ẴG�r�f���X���x���̍������ʂ̕����҂������B
�� ���p����
1�j Davids PH, Groen AK, Rauws EA, et al. Randomised trial of self-expanding metal stents versus polyethylene stents for distal malignant biliary obstruction. Lancet 1992�G340�F1488-1492.
2�j Knyrim K, Wagner HJ, Pausch J, et al. A prospective, randomized, controlled trial of metal stents for malignant obstruction of the common bile duct. Endoscopy 1993�G25�F207-212.
3�j Soderlund C, Linder S. Covered metal versus plastic stents for malignant common bile duct stenosis�Fa prospective, randomized, controlled trial. Gastrointest Endosc 2006�G63�F986-995.
4�j Isayama H, Yasuda I, Ryozawa S, et al. Results of a Japanese multicenter, randomized trial OF endoscopic stenting for non-resectable pancreatic head cancer�iJM-TEST�j�FCovered Wallstent versus Doublelayer stent. Dig Endosc. 2011�G23�F310-315.
5�j Isayama H, Komatsu Y, Tsujino T, et al. A prospective randomised study of �gcovered�h versus �guncovered�h diamond stents for the management of distal malignant biliary obstruction. Gut 2004�G53�F729-734.
6�j Krokidis M, Fanelli F, Orgera G, et al. Percutaneous palliation of pancreatic head cancer�Frandomized comparison of ePTFE/FEP-covered versus uncovered nitinol biliary stents. Cardiovasc Intervent Radiol 2011�G34�F352-361.
7�j Kitano M, Yamashita Y, Tanaka K, et al. 146 Drastic Improvement of Patency of Covered Self-Expandable Metal Stents for Distal Biliary Obstruction Caused by Pancreatic Carcinomas�FA Randomized Multicenter Study Comparing Covered and Uncovered Stents. Gastrointest Endosc 2012�G75�FAB123.
8�j Krokidis M, Fanelli F, Orgera G, et al. Percutaneous treatment of malignant jaundice due to extrahepatic cholangiocarcinoma�Fcovered Viabil stent versus uncovered Wallstents. Cardiovasc Intervent Radiol 2010�G33�F97-106.
9�j Telford JJ, Carr-Locke DL, Baron TH, et al. A randomized trial comparing uncovered and partially covered self-expandable metal stents in the palliation of distal malignant biliary obstruction. Gastrointest Endosc 2010�G72�F907-914.
10�j Kullman E, Frozanpor F, Söderlund C, et al. Covered versus uncovered self-expandable nitinol stents in the palliative treatment of malignant distal biliary obstruction�Fresults from a randomized, multicenter study. Gastrointest Endosc 2010�G72�F915-923.
11�j Saleem A, Leggett CL, Murad MH, et al. Meta-analysis of randomized trials comparing the patency of covered and uncovered self-expandable metal stents for palliation of distal malignant bile duct obstruction. Gastrointest Endosc 2011�G74�F321-327 e1-3.
12�j Almadi MA, Barkun AN, Martel M. No benefit of covered vs uncovered self-expandable metal stents in patients with malignant distal biliary obstruction�Fa meta-analysis. Clin Gastroenterol Hepatol 2013�G11�F27-37. e1.
13�j Isayama H, Kawabe T, Nakai Y, et al. Cholecystitis after metallic stent placement in patients with malignant distal biliary obstruction. Clin Gastroenterol Hepatol. 2006�G4�F1148-1153.
14�j Suk KT, Kim HS, Kim JW, et al. Risk factors for cholecystitis after metal stent placement in malignant biliary obstruction. Gastrointest Endosc 2006�G64�F522-529.
15�j Nakai Y, Isayama H, Komatsu Y, et al. Efficacy and safety of the covered Wallstent in patients with distal malignant biliary obstruction. Gastrointest Endosc 2005�G62�F742-748.
16�j Tarnasky PR, Cunningham JT, Hawes RH, et al. Transpapillary stenting of proximal biliary strictures�Fdoes biliary sphincterotomy reduce the risk of postprocedure pancreatitis�H Gastrointest Endosc 1997�G45�F46-51.
17�j Coté�GGA, Kumar N, Ansstas M, et al. Risk of post-ERCP pancreatitis with placement of self-expandable metallic stents. Gastrointest Endosc 2010�G72�F748-754.
18�j Isayama H, Nakai Y, Toyokawa Y, et al. Measurement of radial and axial forces of biliary self-expandable metallic stents. Gastrointest Endosc. 2009�G70�F37-44.
19�j Kawakubo K, Isayama H, Nakai Y, et al. Risk factors for pancreatitis following transpapillary self-expandable metal stent placement. Surg Endosc 2012�G26�F771-776.
20�j Isayama H, Mukai T, Itoi T, et al. Comparison of partially covered nitinol stents with partially covered stainless stents as a historical control in a multicenter study of distal malignant biliary obstruction�Fthe WATCH study. Gastrointest Endosc 2012�G76�F84-92.
21�j Hoffman JP, Lipsitz S, Pisansky T, et al. PhaseⅡtrial of preoperative radiation therapy and chemotherapy for patients with localized, resectable adenocarcinoma of the pancreas�Fan Eastern Cooperative Oncology Group Study. J Clin Oncol 1998�G16�F317-323.
22�j Pisters PW, Hudec WA, Lee JE, et al. Preoperative chemoradiation for patients with pancreatic cancer�Ftoxicity of endobiliary stents. J Clin Oncol 2000�G18�F860-867.
23�j Nakai Y, Isayama H, Kawabe T, et al. Efficacy and safety of metallic stents in patients with unresectable pancreatic cancer receiving gemcitabine. Pancreas 2008�G37�F405-410.
CQ 6-4�@�ݏ\��w���ǂ����������؏��s�\��ɑ��鎡�Ö@�͉�����������邩�H
�����S�g��Ԃ��ǍD�Ŕ�r�I�����̗\�オ���҂����Ǘ�ɂ͊O�ȓI�����p�C����ȊO�̏Ǘ�ɂ͓������I�\��w���X�e���g�}���p�����������i�O���[�hB�j�B �� �G�r�f���X
�؏��s�\�X���ł�70�`80���ɒ_���ǂ��C20���ɏ\��w���ǂ��������ƕ���Ă��� 1�j�i���x��Ⅴ�j�B�X�������ł͏\��w���������牺�s�r�C�X�b�����ł͉��s�r���琅���r�C�̕�����������ł͐����r�ȉ��ɕǂ��������₷���B�X���ł͊O�ȓI�؏���ړI�Ƃ��ĊJ�����Ă��؏��s�\�ƂȂ邱�Ƃ���������C���̍ۂ̗\�h�I�����͈Ӌ`������Ƃ���Ă��� 2�j�i���x��Ⅱ�j�B
����C1990 �N�O������\��w���X�e���g�̕Ⴊ�݂��C��������p�������тɂ�������S���ƗL����������Ă��� 3-5�j�i���x��Ⅳb�j 6�j�i���x��Ⅳa�j�B�����p�Ƃ̔�r�ł́C�������̌����ɂ����āC��Z�������C�H���ێ�\���͂قړ����ł���C�\��w���X�e���g�̒����Ƃ��āC�Ǐ�̉��P���v���C�o���ێ�J�n�܂ł̎��Ԃ̒Z�k�C���@���Ԃ̒Z�k�C���S���̒ቺ�C��ÃR�X�g�̍팸���������Ă���B����C�Z���Ƃ��Ĉ�E�C�ǁC�Ď��ÁC���Ǖǂ̑����̖�肪�������Ă��� 7-9�j�i���x��Ⅳb�j�B�X�e���g���u��ɔ�������overgrowth �͖�4���ł���C�\��w�������C����������C�����Ǖǂ܂��͋���̒������댯���q�Ƃ���Ă��� 10�j�i���x��Ⅲ�j�B�܂��C�X�e���g���u��̉��w�Ö@���o���ێ���Ԃ̉����Ɋ�^����\��������Ă��� 11�j�i���x��Ⅴ�j�B
�킪���ł͓������I�\��w���X�e���g�}���p��2010 �N4 ���ɕی����ڂ��ꂽ�B�X�����܂ވ݁E�\��w���ǏǗ�ɂ�����O�����Ȍ����ł́CGOOSS�igastric outletobstruction scoring system�j�̌p���I���P�Ǝ�Z�������͂Ƃ���94�`96���C��Z�֘A�̓��@���Ԓ����l��2 ���C�J�����Ԃ̒����l��270 ���C�������Ԓ����l��82�`99 ���ƕ���Ă���B�܂������ǂ�21�`23���ŁC��Ȃ��̂��u�ɁC��E�C���ǐ��E�C�n���Covergrowth �܂���ingrowth �ł������B�܂��C�X�e���g�}����̉��w�Ö@���J�����Ԃ̉����Ɋ�^����\��������Ă��� 12�j�i���x��Ⅲ�j13�j�i���x��Ⅱ�j�B�����p�Q�Ɠ������I�\��w���X�e���g�Q�̑O������r�����ł́C�o���ێ�J�n�\�܂ł̊��Ԃ͓������I�\��w���X�e���g�Q���L�ӂɑ����C�����̏Ǐ���P���ʂ͈����Q���D��B�d�Ăȍ����ǂ���ѕǏǏ�̍Ĕ��C�Ď��Â͓������I�\��w���X�e���g�Q�ɗL�ӂɑ����B�������Ԃɂ͍����Ȃ��C���ÂɊւ����ÃR�X�g�͈�������⍂���X���ɂ��邪���͂킸���ł���C���Ö@�̌���ɑ傫�ȉe����^���Ȃ��ƕ��ꂽ 14, 15�j�i���x��Ⅱ�j�B�ȏ�̌��ʂ���C�S�g��Ԃ��ǍD�ŗ\�オ���J�����x���҂ł���Ǘ�ɂ͈����p�C����ȊO�̏Ǘ�ɂ͓������I�\��w���X�e���g�}���p����������� 16�j�i���x��Ⅰ�j�B
�� �����ւ̒�
2010 �N4 ���ɍ����ŔF���ꂽ�������I�\��w���X�e���g�}���p�́C�����ƕ���ŏ\��w���ǂ����������X���؏��s�\�Ǘ�ɑ���V���Ȏ��ÑI�����ł���B���݂܂łɕ���Ă�������p�Ɠ������I�\��w���X�e���g�Q�̔�r�����̐��т͑Ώۂ����ׂ��X���ł͂Ȃ��C�݊������̊����Ŋ܂�Ō�������Ă��邱�Ƃɒ��ӂ��ׂ��ł���C����؏��s�\�X���݂̂�ΏۂƂ��������p�Ɠ������I�\��w���X�e���g�}���p��O�����ɔ�r�������{�����������]�܂��B�܂��C�\��w���X�e���g��axial force�C�}����̒Z�k�̗L���Ȃǂ��X�e���g�̎�ނɂ���đ傫���قȂ邽�߁C�p����X�e���g�̎�ނɂ���đ傫�����т��قȂ�\�������邱�Ƃɗ��ӂ��ׂ��ł���B�X�e���g���u��̉��w�Ö@���J�����Ԃɉe����^���邩�ǂ����̘_�͏\���Ȃ���Ă��炸����̉ۑ�ł���B
�� ���p����
1�j Andtbacka RH, Evans DB, Pisters PW. Surgical and endoscopic palliation for pancreatic cancer. Minerva Chir 2004�G59�F123-126.
2�j Van Heek NT, De Castro SM, van Eijck CH, et al. The need for a prophylactic gastrojejunostomy for unresectable periampullary cancer�Fa prospective randomized multicenter trial with special focus on assessment of quality of life. Ann Surg 2003�G238�F894-905�Gdiscussion 902-5.
3�j Adler DG, Baron TH. Endoscopic palliation of malignant gastric outlet obstruction using self-expanding metal stents�Fexperience in 36 patients. Am J Gastroenteol 2002�G97�F72-78.
4�j Kaw M, Singh S, Gagneja H, et al. Role of self-expandable metal stents in the palliation of malignant duodenal obstruction. Surg Enodsc 2003�G17�F646-650.
5�j Graber I, Dumas R, Filoche B, et al. The efficacy and safety of duodenal stenting�Fa prospective multicenter study. Endoscopy 2007�G39�F784-787.
6�j Shaw JM, Bornman PC, Krige JE, et al. Self-expanding metal stents as an alternative to surgical bypass for malignant gastric outlet obstruction. Br J Surg 2010�G97�F872-876.
7�j Wong YT, Brams DM, Munson L, et al. Gastric outlet obstruction secondary to pancreatic cancer�Fsurgical vs endoscopic palliation. Surg Endosc 2002�G16�F310-312.
8�j Maetani I, Tada T, Ukita T, et al. Comparison of duodenal stent placement with surgical gastrojejunostomy for palliation in patients with duodenal obstructions caused by pancreaticobiliary malignancies. Endoscopy 2004�G36�F73-78.
9�j Del Piano M, Ballare` M, Montino F, et al. Endoscopy or surgery for malignant GI outlet obstruction�H Gastrointest Endosc 2005�G61�F421-426.
10�j Jang JK, Song HY, Kim JH, et al. Tumor overgrowth after expandable metallic stent placement�Fexperience in 583 patients with malignant gastroduodenal obstruction. AJR 2011�G196�FW 831-836.
11�j Telford JJ, Carr-Locke DL, Baron TH, et al. Palliation of patients with malignant gastric outlet obstruction with the enteral Wallstent�Foutcomes from a multicenter study. Gastrointest Endosc 2004�G60�F916-920.
12�j Kim JH, Song HY, Shin JH, et al. Metallic stent placement in the palliative treatment of malignant gastroduodenal obstructions�Fprospective evaluation of results and factors influencing outcome in 213 patients. Gastrointest Endosc 2007�G66�F256-264.
13�j van Hooft JE, van Montfoort ML, Jeurnink SM, et al. Safety and efficacy of a new non-foreshortening nitinol stent in malignant gastric outlet obstruction�iDUONITI study�j�Fa prospective, multicenter study. Endoscopy 2011�G43�F671-675.
14�j Jeurnink SM, Steyerberg EW, van Hooft JE, et al. Surgical gastrojejunostomy or endoscopic stent placement for the palliation of malignant gastric outlet obstruction�iSUSTENT study�j�Fa multicenter randomized trial. Gastrointest Endosc 2009�G71�F490-499.
15�j Jeurnink SM, Polinder S, Steyerberg EW, et al. Cost comparison of gastrojejunostomy versus duodenal stent placement for malignant gastric outlet obstruction. J Gastroenterol 2010�G45�F537-543.
16�j Jeurnink SM, van Eijck CH, Steyerberg EW, et al. Stent versus gastrojejunostomy for the palliation of gastric outlet obstruction�Fa systematic review. BMC Gastroenterol 2007�G7�F18.
- �Ǐ��i�s�؏��s�\�X���݂̂ɑ����Ⅲ����������̃G�r�f���X


